Clear Sky Science · fr
Spécificité antigénique des cellules T CD8 clonaly enrichies dans la sclérose en plaques
Pourquoi cette recherche compte pour les personnes
La sclérose en plaques (SEP) est une maladie dans laquelle le système immunitaire attaque le cerveau et la moelle épinière, mais les déclencheurs exacts de cette attaque restent mystérieux. Un suspect de longue date est le virus Epstein–Barr (VEB), un virus très courant qui infecte la plupart des personnes au cours de leur vie. Cette étude examine directement le liquide qui baigne le cerveau pour identifier quelles cellules immunitaires y sont présentes, ce qu’elles font et, de manière cruciale, à quoi elles réagissent. Comprendre ce lien pourrait transformer la façon dont nous diagnostiquons, surveillons et, finalement, traitons la SEP.
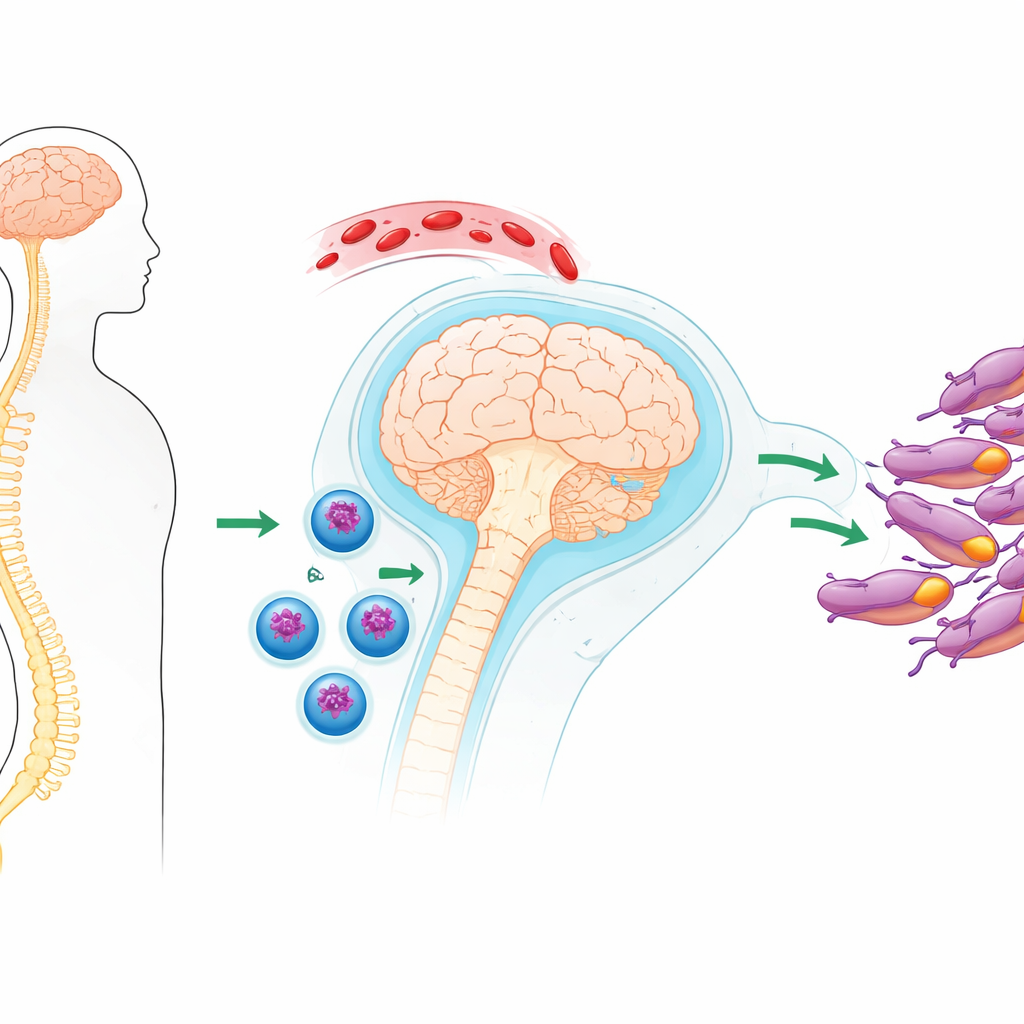
Les cellules immunitaires sur place
Les chercheurs ont analysé des échantillons de sang et de liquide céphalorachidien de 18 personnes : des patients présentant une SEP précoce ou une première attaque apparentée, des personnes atteintes d’autres affections inflammatoires du cerveau et des volontaires sains. Grâce au séquençage unicellulaire à haute résolution, ils ont catalogué des dizaines de milliers de cellules T individuelles, un type de globule blanc capable de reconnaître et de détruire les cellules infectées ou anormales. Ils ont constaté que, dans le liquide entourant le cerveau, les cellules T des patients SEP semblaient plus activées et mieux équipées pour pénétrer les tissus et exercer des fonctions destructrices que les cellules T des participants témoins.
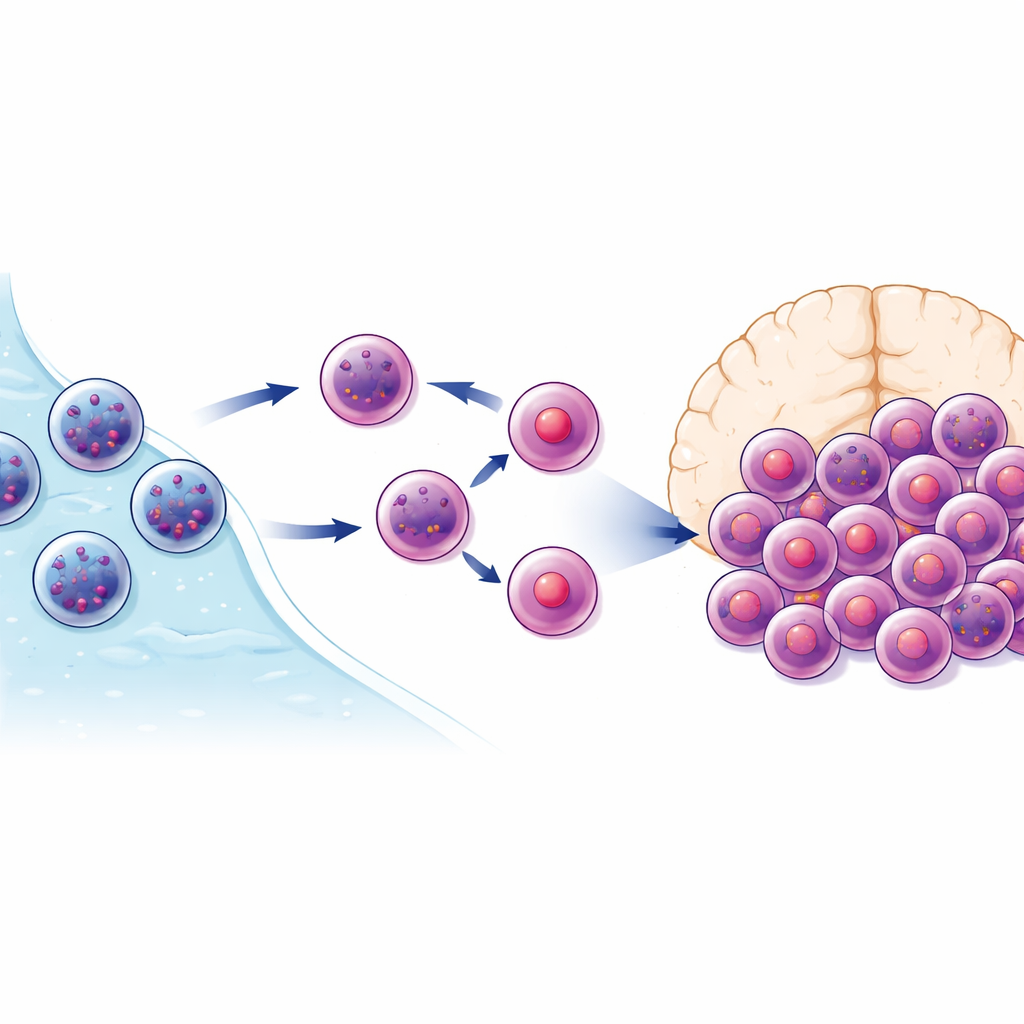
Un petit groupe mais puissant et récurrent
Les cellules T qui rencontrent à plusieurs reprises leur cible se développent en clones — de grandes familles de cellules presque identiques. Lorsque l’équipe a examiné les séquences des récepteurs des cellules T, qui servent de marqueurs d’identification pour chaque clone, elle a trouvé un petit sous‑ensemble de clones de cellules T CD8 fortement étendus et exceptionnellement enrichis dans le liquide céphalorachidien comparé au sang. Plus de 70 % de ces clones enrichis étaient des cellules T CD8, la sous‑population spécialisée dans la cytotoxicité. Ces cellules portaient des signatures génétiques d’éléments expérimentés du combat : elles exprimaient des molécules liées à l’entrée dans les tissus, à la résidence dans le système nerveux central et à une machinerie de destruction cellulaire puissante. Chez certains patients SEP, une poignée de ces clones représentait une fraction remarquable de toutes les cellules T présentes dans le liquide céphalorachidien.
Suivre la piste d’un virus commun
La question clé était de savoir ce que reconnaissaient ces clones T dominants. Les auteurs ont cloné les récepteurs de 23 des clones CD8 les plus enrichis et les ont testés contre d’immenses bibliothèques de fragments candidats provenant de virus et de protéines humaines. Plusieurs peptides « mimétiques » artificiels se liaient à certains récepteurs mais ne déclenchaient pas de réponse fiable, ce qui suggère qu’ils n’étaient pas leurs véritables cibles. Cependant, trois clones CD8 indépendants provenant de trois patients différents atteints de SEP ont réagi de manière forte et spécifique à des protéines connues du VEB. Ces clones centrés sur le virus n’étaient pas seulement abondants dans le liquide céphalorachidien ; leurs profils génétiques indiquaient qu’ils étaient activement engagés dans le contrôle de l’infection plutôt que simplement au repos.
Signes d’activité virale dans le liquide cérébral
Pour vérifier si le VEB lui‑même était présent, les chercheurs ont mesuré l’ADN et l’ARN du VEB dans le liquide céphalorachidien. Ils ont détecté du matériel génétique du VEB chez la plupart des participants, ce qui reflète la large diffusion du virus dans la population générale. Pourtant, certains transcrits du VEB associés à la réactivation virale étaient plus élevés chez les personnes atteintes de SEP ou ayant eu un premier épisode démyélinisant que chez les témoins. Notamment, les patients porteurs de cellules T CD8 spécifiques du VEB fortement étendues dans leur liquide céphalorachidien avaient également tendance à présenter des signatures du VEB dans ce liquide. Ce schéma suggère un scénario dans lequel le VEB devient actif dans ou près du système nerveux central, attirant et étendant des cellules T spécialisées dans la lutte contre le virus.
Ce que cela signifie pour la compréhension de la SEP
Globalement, l’étude montre que, dans la SEP précoce non traitée, le liquide entourant le cerveau contient une petite mais proéminente population de cellules T CD8 fortement étendues, armées pour endommager les tissus et, dans plusieurs cas, spécifiquement orientées vers la reconnaissance du VEB. Parallèlement, des traces génétiques du VEB sont plus abondantes dans le liquide céphalorachidien de ces patients. Si ce travail ne prouve pas que le VEB cause directement la SEP ni que ces cellules T attaquent la myéline, il apporte un soutien solide à l’idée que le VEB joue un rôle important dans l’environnement de la maladie. Ce lien pourrait éventuellement permettre aux médecins de suivre les cellules immunitaires pertinentes dans le liquide spinal et inspirer des thérapies visant soit le VEB lui‑même, soit la modulation des cellules T spécifiques au virus qui s’accumulent dans le cerveau des personnes atteintes de SEP.
Citation: Hayashi, F., Mittl, K., Dandekar, R. et al. Antigen specificity of clonally enriched CD8+ T cells in multiple sclerosis. Nat Immunol 27, 490–502 (2026). https://doi.org/10.1038/s41590-025-02412-3
Mots-clés: sclérose en plaques, virus Epstein–Barr, cellules T CD8, liquide céphalorachidien, neuroinflammation auto-immune