Clear Sky Science · fr
Un axe GDF-15–GFRAL contrôle les réponses des lymphocytes T auto-immunes lors de la neuroinflammation
Pourquoi la grossesse peut calmer un système immunitaire déréglé
Les médecins observent depuis longtemps une énigme médicale : de nombreuses femmes atteintes de sclérose en plaques, une maladie où le système immunitaire attaque le cerveau et la moelle épinière, se sentent souvent mieux pendant la grossesse. Le nombre de poussées chute fortement, pour revenir après l’accouchement. Cette étude révèle un élément clé de ce puzzle, montrant un signal qui part du corps vers une petite région du cerveau puis revient vers le système immunitaire, réduisant les attaques nuisibles sans pour autant couper complètement les défenses. 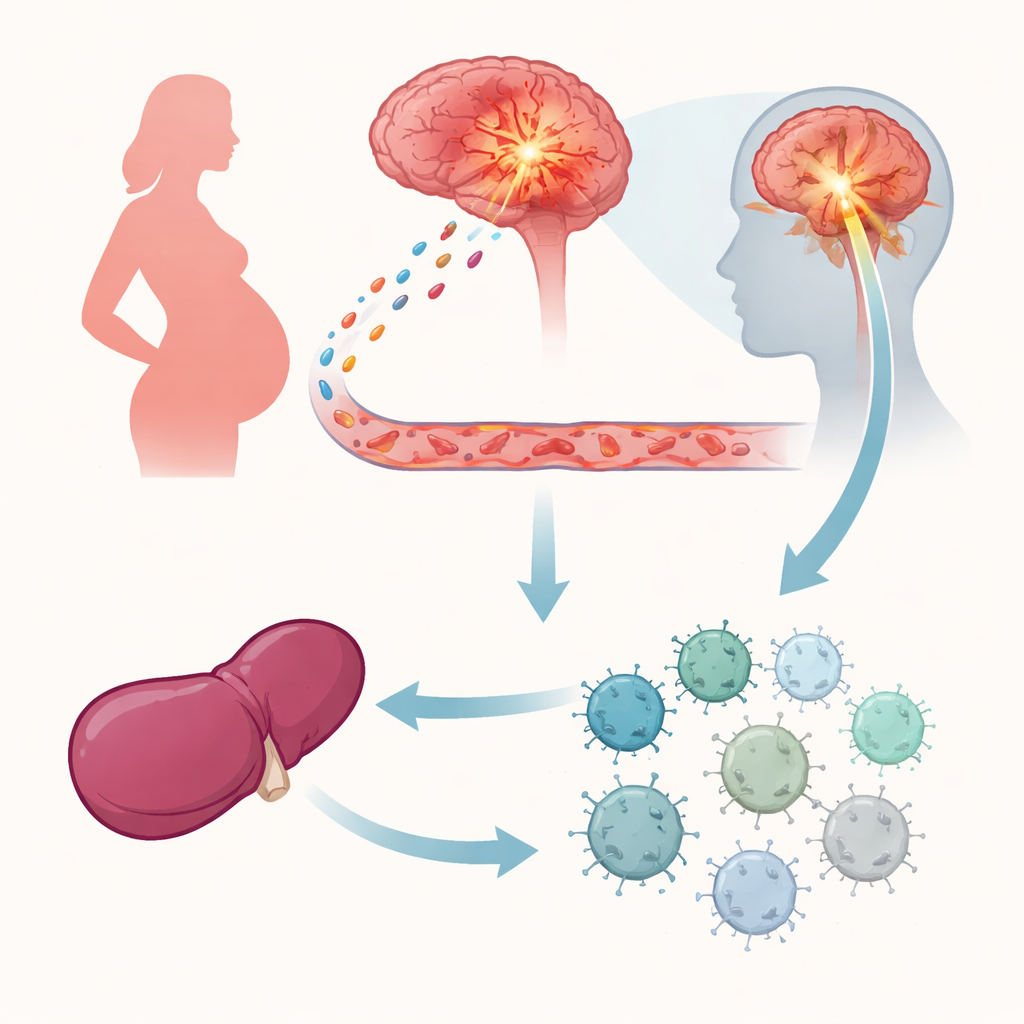
Un messager qui augmente lors de la grossesse et des maladies cérébrales
Les chercheurs se sont concentrés sur une protéine appelée GDF-15, présente dans le sang. Ils ont mesuré les taux de GDF-15 chez des femmes enceintes et chez des souris et constaté que cette molécule augmente régulièrement au cours de la grossesse. Les femmes atteintes de sclérose en plaques qui sont restées sans rechute pendant la grossesse avaient des taux de GDF-15 plus élevés que celles qui ont présenté des poussées. Chez des souris portant des descendants génétiquement différents, les taux de GDF-15 augmentaient particulièrement, et des niveaux plus faibles étaient associés à des portées plus petites, suggérant que cette protéine aide le corps maternel à tolérer le fœtus en partie étranger.
Lorsque le cerveau est enflammé, le signal monte
L’équipe a ensuite étudié ce qui se passe lors d’une neuroinflammation expérimentale, un modèle murin de sclérose en plaques. Chez ces animaux, des cellules du cerveau et de la moelle épinière ont commencé à produire de grandes quantités de GDF-15 précisément au niveau des foyers inflammatoires. Des cellules immunitaires infiltrées dans le système nerveux central ont également contribué à cette poussée. Les souris dépourvues de GDF-15 sont devenues plus malades, ont mal récupéré et ont présenté des cellules immunitaires cérébrales plus agressives, suggérant que la molécule agit normalement comme un frein aidant à résoudre l’inflammation plutôt qu’à l’empêcher de démarrer.
Le « central téléphonique » du tronc cérébral envoie des signaux apaisants à la rate
GDF-15 ne peut déclencher de signal que s’il se fixe à un senseur spécifique appelé GFRAL, présent presque exclusivement sur des neurones d’une petite zone du tronc cérébral située en dehors de la barrière hémato‑encéphalique classique. Les scientifiques ont utilisé la thérapie génique et des injections protéiques pour augmenter les niveaux de GDF-15 chez la souris et ont constaté que cela protégeait puissamment contre la neuroinflammation, même après l’apparition de la maladie, sans dépendre des hormones du stress ni d’une simple perte de poids. Lorsque GFRAL manquait, ou quand une forme mutante de GDF-15 incapable de se lier à ce récepteur était utilisée, la protection disparaissait. L’activation directe des neurones positifs pour GFRAL, via un outil chimiogénétique permettant d’activer les cellules par un médicament conçu, suffisait à elle seule à empêcher les cellules immunitaires d’envahir la moelle épinière. 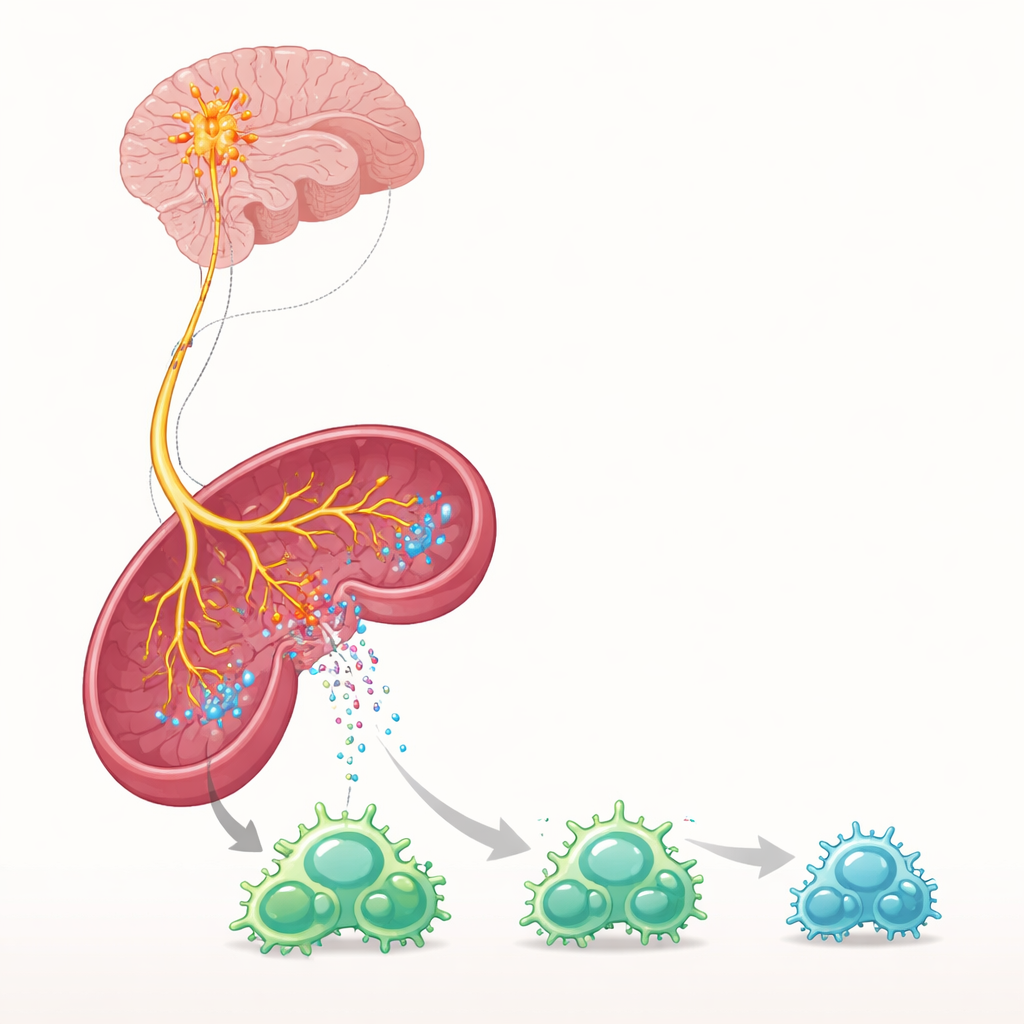
Comment les signaux nerveux reprogramment les lymphocytes T
Pour comprendre comment un petit groupe de neurones pouvait contrôler une vaste réponse immunitaire, l’équipe a retracé leurs effets jusqu’à la rate, un pôle majeur des cellules immunitaires. Augmenter le GDF-15 ou stimuler les neurones exprimant GFRAL a accru l’activité des fibres nerveuses sympathiques dans la rate et élevé les niveaux de noradrénaline, un messager chimique mieux connu pour son rôle dans la réponse « combat-fuite ». Lorsque les lymphocytes T spléniques ont été exposés à la noradrénaline ou à des médicaments similaires, ils se sont divisés moins, ont présenté des marqueurs d’activation plus faibles et des niveaux réduits de protéines de surface importantes qui leur permettent normalement d’adhérer aux parois des vaisseaux sanguins et de pénétrer dans le cerveau. In vivo, cela s’est traduit par moins de lymphocytes T activés dans les organes lymphoïdes et beaucoup moins de cellules immunitaires atteignant le cerveau et la moelle épinière.
Un nouveau circuit cerveau–immunité avec un potentiel thérapeutique
Dans l’ensemble, les résultats révèlent un circuit finement réglé : la grossesse ou le stress tissulaire élève le GDF-15, ce signal atteint les neurones exprimant GFRAL dans le tronc cérébral, ces neurones activent les nerfs sympathiques vers la rate, et la noradrénaline freine ensuite les lymphocytes T potentiellement nuisibles en limitant leur activation, leur prolifération et leur capacité à entrer dans le cerveau. Plutôt que de supprimer l’immunité de façon générale, cette voie refroidit sélectivement les attaques auto-immunes. Comme des versions pharmacologiques du GDF-15 et des outils ciblant son récepteur ont déjà été testés pour d’autres affections, cet axe cerveau–immunité nouvellement cartographié offre une voie prometteuse vers de futures thérapies pour la sclérose en plaques et possiblement d’autres maladies auto-immunes.
Citation: Sonner, J.K., Kahn, A., Binkle-Ladisch, L. et al. A GDF-15–GFRAL axis controls autoimmune T cell responses during neuroinflammation. Nat Immunol 27, 503–515 (2026). https://doi.org/10.1038/s41590-025-02406-1
Mots-clés: sclérose en plaques, neuroinflammation, tolérance immunitaire, circuit neuro-immunitaire, GDF-15