Clear Sky Science · fr
La répartition spatiale du signal TGFβ dans les fibroblastes sous‑tend la résistance au traitement dans la polyarthrite rhumatoïde
Pourquoi la douleur articulaire tenace compte
Beaucoup de personnes atteintes de polyarthrite rhumatoïde prennent des médicaments modernes qui apaisent le système immunitaire, et pourtant leurs articulations restent douloureuses et raides. Cette étude se demande pourquoi certains patients ne s’améliorent pas malgré l’apparente disparition de l’inflammation articulaire. En examinant de près où et comment certains cellules de soutien de l’articulation activent des programmes cicatriciels, les chercheurs mettent au jour une forme de lésion cachée qui pourrait expliquer la douleur persistante et indiquer de nouvelles stratégies thérapeutiques.
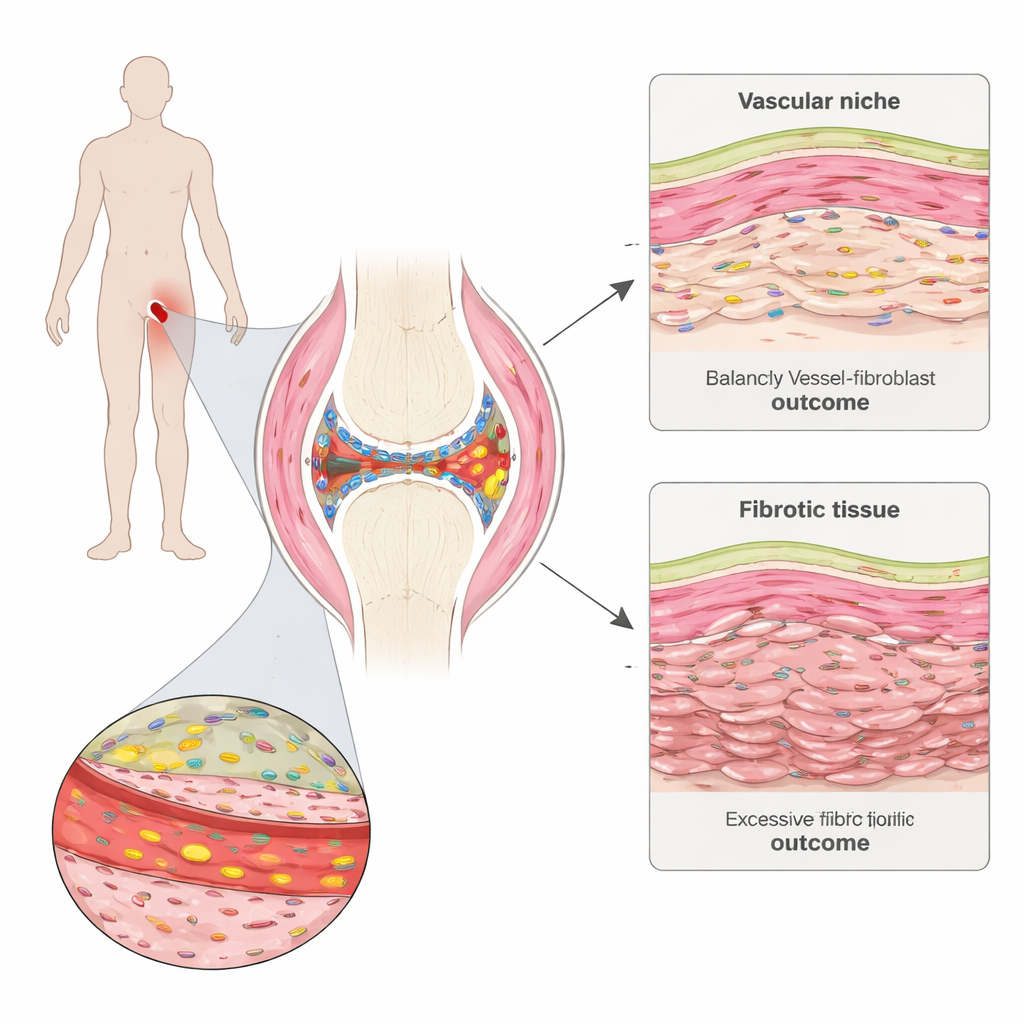
Un examen approfondi de l’articulation douloureuse
La polyarthrite rhumatoïde attaque la synoviale, une fine couche qui tapisse et lubrifie les articulations. L’équipe a prélevé de minuscules biopsies synoviales chez des personnes présentant une maladie précoce avant le début du traitement, puis de nouveau six mois plus tard. Grâce à une cartographie spatiale avancée de l’expression génique, ils ont pu voir quels gènes étaient actifs dans des milliers de cellules individuelles tout en préservant leur position dans le tissu. Ils ont identifié des « quartiers » distincts dans la synoviale, incluant des amas de cellules immunitaires, des zones riches en graisse, la mince muqueuse interne et des régions denses en vaisseaux sanguins et en cellules structurelles appelées fibroblastes.
Cellules formatrices de cicatrices et résistance au traitement
En comparant les patients qui ont ensuite atteint la rémission avec ceux qui ne l’ont pas fait, les chercheurs ont trouvé un schéma frappant : avant le traitement, les patients ne rémissionnant pas présentaient déjà des signaux plus marqués de cicatrisation tissulaire, ou fibrose. Un programme fibroblastique particulier, marqué par une forte production d’une protéine matricielle extracellulaire appelée COMP, était augmenté chez ces patients. Ces fibroblastes riches en COMP partageaient des caractéristiques avec les cellules formatrices de cicatrices observées dans la fibrose pulmonaire et cutanée et étaient les mieux corrélés à une mauvaise réponse au traitement. Avec le temps, les régions dominées par ces cellules avaient tendance à devenir densément remplies de tissu conjonctif mais relativement pauvres en cellules, ce qui suggère qu’elles déposent une matrice rigide susceptible de persister même après la réduction de l’inflammation.
Les vaisseaux sanguins comme conducteurs cachés
Les fibroblastes fibrogéniques n’étaient pas répartis au hasard. Ils s’agrégeaient autour des vaisseaux sanguins, formant des zones périvasculaires en couches. La couche la plus interne, accolée à la paroi du vaisseau, exprimait des gènes différents de la couche externe. L’équipe a montré que les cellules qui tapissent les vaisseaux envoient des signaux Notch aux fibroblastes voisins, qui à leur tour modulèrent la manière dont ces fibroblastes répondent à une famille d’indices pro‑cicatrisation connue sous le nom de TGF‑bêta. Près du vaisseau, la signalisation Notch pousse les fibroblastes à produire du TGF‑bêta mais réduit simultanément le nombre de récepteurs au TGF‑bêta à leur surface, limitant ainsi leur sensibilité. Plus loin, où l’influence de Notch s’estompe, les fibroblastes présentent davantage de récepteurs et deviennent très réactifs, se transformant en cellules riches en COMP qui déclenchent la fibrose.
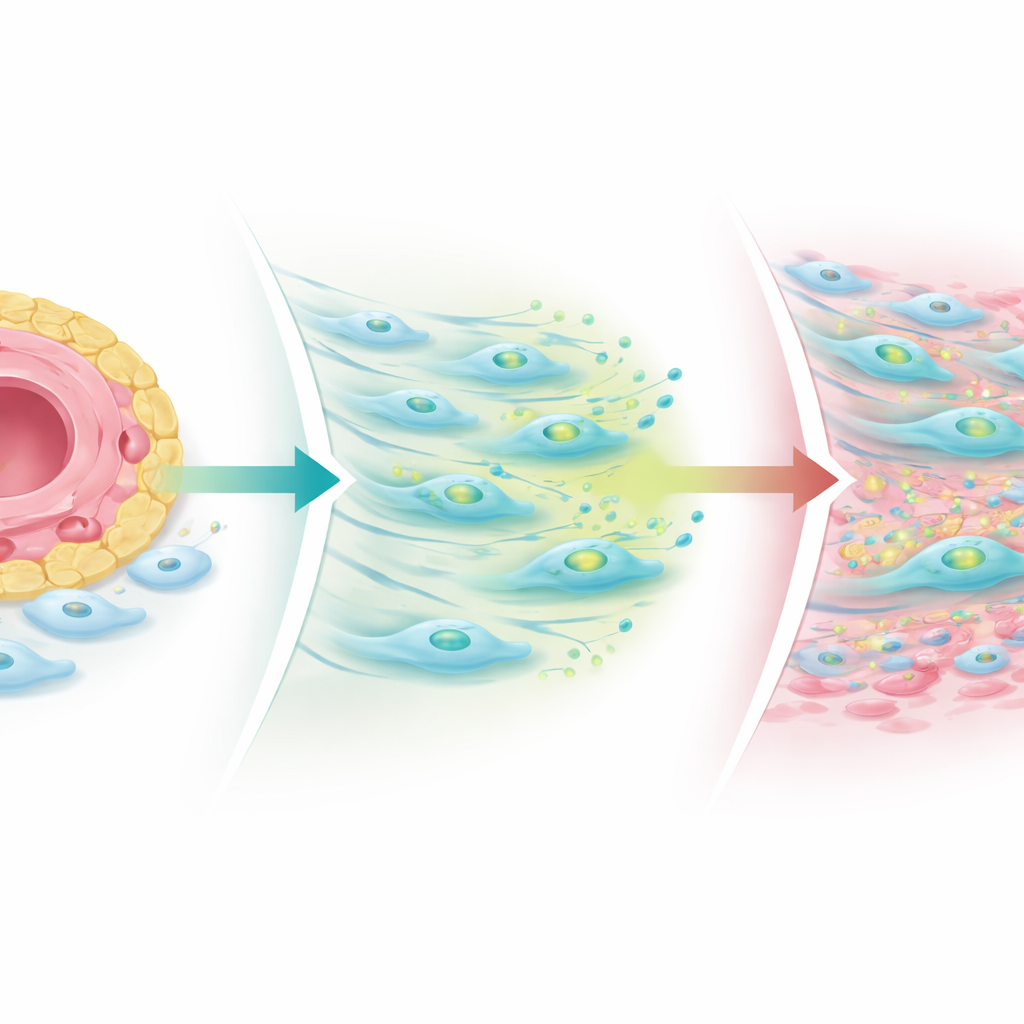
Que se passe‑t‑il lorsque l’équilibre est rompu
Les chercheurs ont construit des modèles articulaires simplifiés en boîtes de culture et des organoïdes tridimensionnels dérivés de tissus de patients pour explorer ce mécanisme. Lorsqu’ils ont renforcé les signaux Notch provenant des cellules endothéliales, les fibroblastes ont augmenté la production de TGF‑bêta tout en réduisant le nombre de récepteurs, limitant ainsi la formation de cicatrices. Lorsqu’ils ont bloqué Notch ou perturbé son schéma stable, les fibroblastes ont retrouvé des récepteurs du TGF‑bêta — en particulier un co‑récepteur appelé récepteur III du TGF‑bêta — et les cellules fibrogéniques COMP‑positives se sont étendues loin des vaisseaux. Dans les biopsies de patients prélevées après traitement, les amas de cellules immunitaires avaient diminué chez presque tous les sujets, mais les niches fibrogéniques, en particulier les régions riches en COMP, avaient souvent augmenté, surtout chez ceux dont la douleur articulaire persistait. Cela suggère que les traitements anti‑inflammatoires standards peuvent éteindre le « feu » immunitaire tout en laissant en place ou même en révélant un processus cicatriciel qui maintient rigidité et douleur articulaires.
Nouvelles façons d’apaiser les articulations tenaces
Enfin, l’équipe a testé si perturber ce circuit fibrogénique pouvait avoir un intérêt thérapeutique. Dans des organoïdes dérivés de patients, des médicaments inhibant Notch ou bloquant la signalisation TGF‑bêta ont réduit la production de COMP, d’autres protéines liées à la cicatrisation et de collagènes clés, et ont reprogrammé l’activité génique dans les zones périvasculaires. Pour un lecteur non spécialiste, le message est que toute la lésion dans la polyarthrite rhumatoïde ne provient pas de l’inflammation visible : une partie est « câblée » dans les cellules de soutien de l’articulation et les vaisseaux sanguins. En ciblant la conversation Notch–TGF‑bêta qui contrôle la façon dont les fibroblastes déposent le tissu cicatriciel, les traitements futurs pourraient prévenir ou inverser une forme fibrotique tenace de la maladie qui résiste aux médicaments actuels axés sur le système immunitaire.
Citation: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Mots-clés: polyarthrite rhumatoïde, fibrose, fibroblastes, signalisation TGF‑bêta, voie Notch