Clear Sky Science · fr
Identification d’un anticorps neutralisant largement puissant ciblant un épitope indépendant du glycan N332gp120 sur le site glycan V3
À la recherche de nouvelles façons de désarmer le VIH
Depuis plus de quarante ans, le VIH résiste obstinément à nos meilleures tentatives pour créer un vaccin ou un remède simple et durable. Une stratégie prometteuse consiste à exploiter des anticorps rares provenant de personnes dont le système immunitaire contrôle naturellement le virus, puis à transformer ces molécules en médicaments ou en modèles pour des vaccins. Cette étude décrit un tel anticorps, nommé 007, qui reconnaît un point faible de l’enveloppe virale d’une manière inhabituelle, ouvrant de nouvelles possibilités pour la prévention, le traitement et peut‑être des stratégies de guérison fonctionnelle.
Un anticorps puissant issu d’un donneur atypique
Les chercheurs ont commencé par analyser le sang de plus de deux mille personnes vivant avec le VIH pour identifier des « neutralisateurs d’élite » — des individus dont les anticorps peuvent désactiver une large gamme de souches virales. Un donneur de Tanzanie, désigné EN01, s’est distingué par une activité de blocage du virus exceptionnellement large et puissante. À partir des lymphocytes B de cette personne, l’équipe a isolé des dizaines d’anticorps et identifié une famille, nommée 007, qui neutralisait puissamment des virus issus de plusieurs sous‑types du VIH. Contrairement à certains anticorps antérieurs qui reconnaissaient parfois les propres tissus de l’hôte, 007 n’a montré aucune auto‑réactivité détectable dans des tests de sécurité standard, ce qui en fait un solide candidat pour un développement ultérieur.
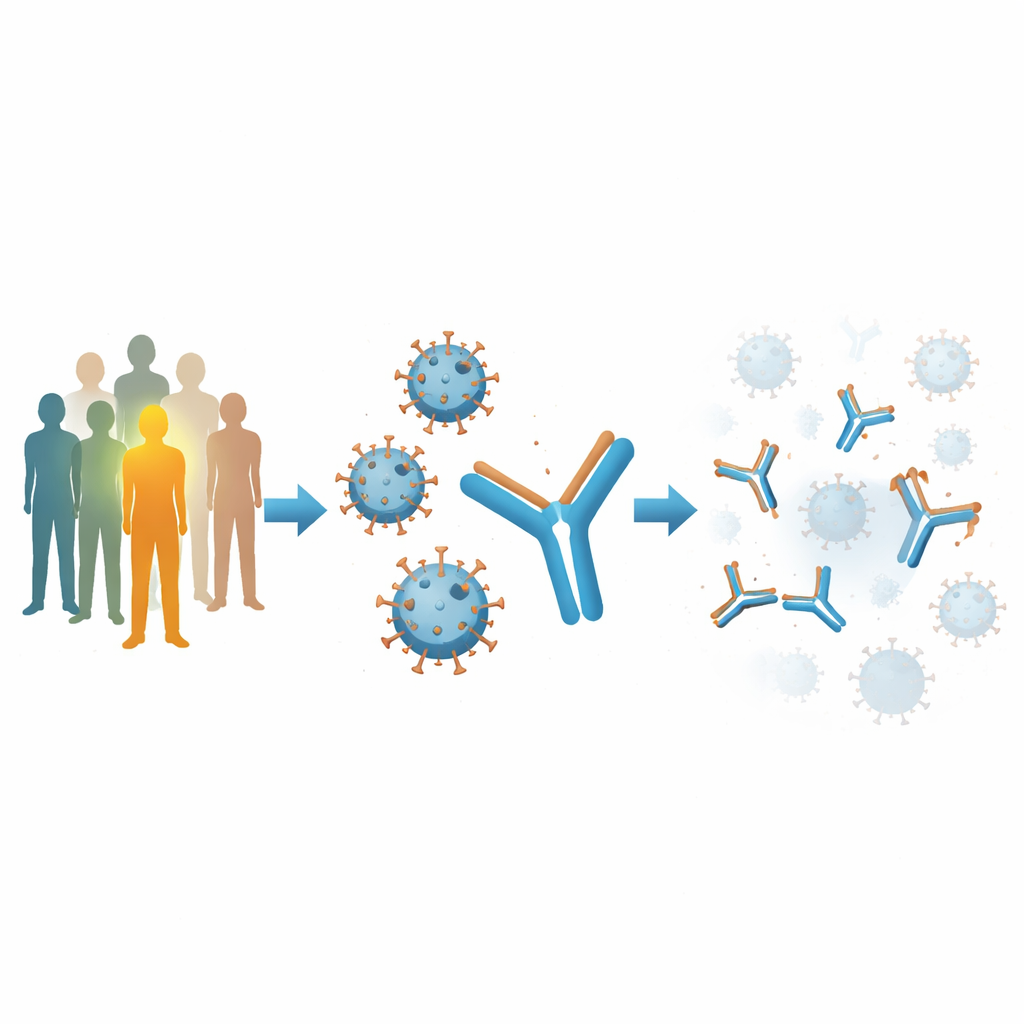
Atteindre un point faible caché sur la coque virale
Le VIH se protège par une dense forêt de sucres couvrant sa protéine d’enveloppe externe, ce qui aide le virus à échapper à la plupart des anticorps. Nombre des anticorps neutralisants largement étudiés ciblent une région près de la base d’une boucle de cette protéine, connue sous le nom de région V3, et dépendent fortement d’un site glycosylé particulier appelé N332. L’anticorps 007, toutefois, brise cette règle. Grâce à la cryo‑microscopie électronique à haute résolution, les auteurs ont montré que 007 insère une longue boucle de sa surface de liaison dans une gorge conservée de la région V3, établissant des contacts précis avec une courte séquence d’acides aminés tout en s’appuyant sur des sucres à deux positions voisines. De manière cruciale, il ne dépend pas du glycan habituel N332, ce qui signifie que les virus qui utilisent l’astuce d’échappement courante consistant à muter ou supprimer ce sucre restent vulnérables à 007.
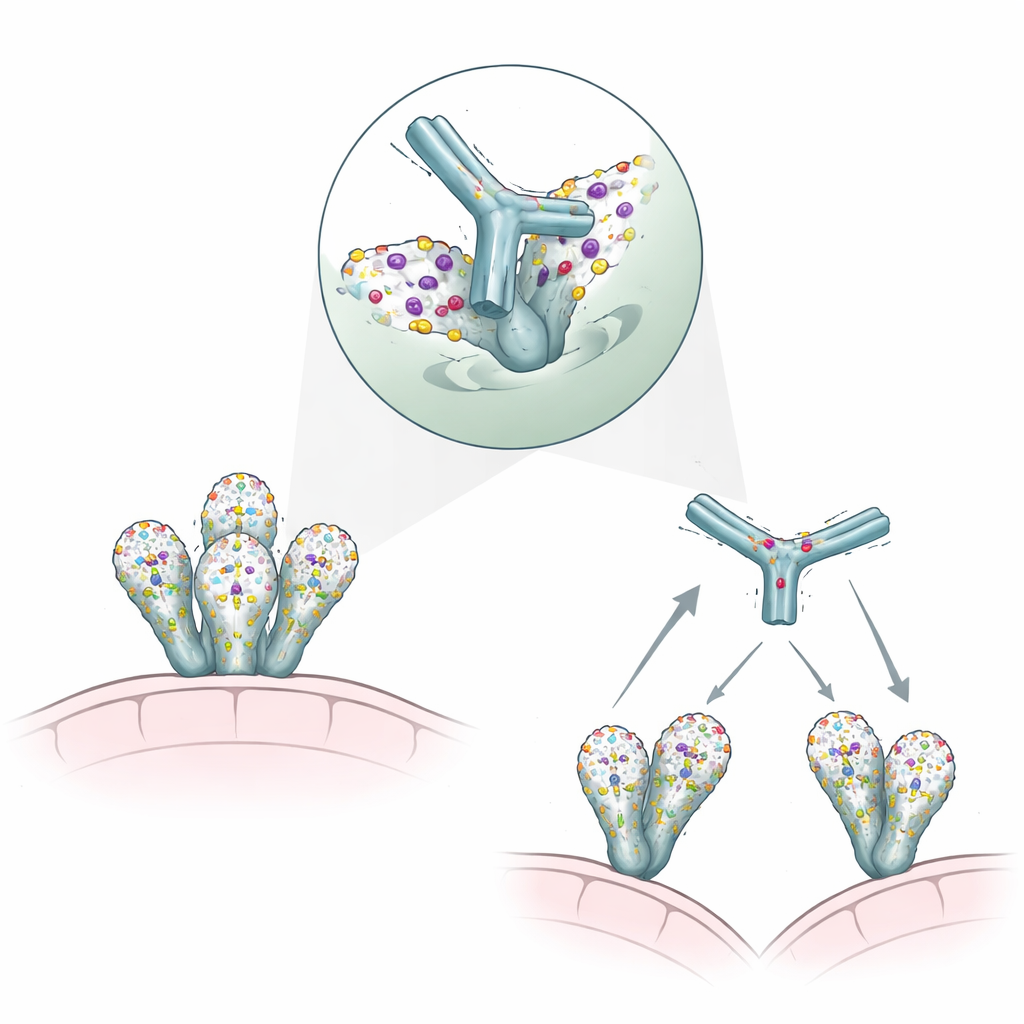
Comment 007 gagne en adhérence grâce à une liaison à deux mains
Lorsque l’équipe a testé un seul « bras » de 007, appelé fragment Fab, il se liait faiblement aux formes solubles du pic d’enveloppe du VIH. Pourtant, l’anticorps entier, avec ses deux bras, était remarquablement puissant pour neutraliser le virus vivant. Des mesures détaillées de liaison et de neutralisation ont révélé que 007 bénéficie fortement de l’utilisation simultanée de ses deux bras, un phénomène connu sous le nom d’avidité. Des études structurelles avec l’anticorps intact et des protéines d’enveloppe trimériques ont montré que trois copies de 007 peuvent relier deux pics viraux en une assembly symétrique de type dimère, suggérant que l’anticorps peut faire le pont entre des pics sur la même particule virale ou sur des particules voisines. Cet engagement à deux mains semble compenser l’affinité modeste d’un seul bras et aide à expliquer la capacité frappante de 007 à inactiver des souches virales difficiles et cliniquement pertinentes.
Se démarquer des autres anticorps anti‑VIH
Pour comprendre comment 007 se situe par rapport à des anticorps bien connus, les auteurs l’ont testé contre de larges panels de souches virales diverses, y compris des variantes difficiles à neutraliser provenant de nombreuses régions du monde. Sur ces panels, 007 a montré une grande étendue et une forte puissance, surpassant souvent les anticorps classiques ciblant V3 et dépassant nettement un anticorps récemment décrit qui reconnaît une région similaire. Remarquablement, 007 est resté efficace contre de nombreux virus qui avaient déjà échappé à un anticorps V3 de référence en modifiant le site glycan N332. Inversement, les virus résistants à 007 étaient souvent neutralisés par ces anticorps classiques. Lorsque l’équipe a modélisé puis testé expérimentalement des combinaisons, 007 s’est particulièrement bien associé à l’anticorps 10‑1074, offrant une couverture nettement améliorée et des concentrations nécessaires pour la neutralisation plus faibles.
Évaluer 007 chez des organismes vivants
Les chercheurs ont ensuite interrogé la capacité de 007 à contrôler l’infection in vivo. Chez des souris humanisées infectées chroniquement par le VIH‑1 ADA, le traitement par 007 a entraîné une chute rapide des niveaux de virus dans le sang, suivie d’un rebond ultérieur à mesure que le virus mutait. L’analyse génétique a révélé que l’échappement à 007 impliquait des changements dans les régions entourant son nouveau site de liaison, plutôt que le glycan habituel N332. Fait important, les virus ayant échappé à 007 restaient sensibles à 10‑1074, et réciproquement. Lorsque les deux anticorps ont été administrés ensemble, ou lorsqu’un anticorps a été ajouté après l’émergence d’une résistance à l’autre, la suppression virale a duré plus longtemps et a exigé que le virus accumule plusieurs mutations à travers son enveloppe, probablement au prix d’un coût pour sa fitness.
Pourquoi ce travail compte pour la prévention future du VIH
En découvrant un anticorps qui cible la région V3 du VIH sans dépendre du glycan standard N332, cette étude élargit le paysage connu des sites vulnérables du virus. L’anticorps 007 combine une activité neutralisante large et puissante avec un schéma d’échappement distinct et une liaison puissante à deux bras, ce qui en fait un ajout prometteur aux cocktails d’anticorps pour la prévention, la thérapie ou des stratégies de guérison fonctionnelle. Pour les concepteurs de vaccins, 007 met en lumière une cible sur la coque virale jusque‑là sous‑exploitées qui pourrait être mimée pour entraîner le système immunitaire à produire des anticorps similaires. Ensemble, ces résultats suggèrent que s’écarter d’un unique point chaud glycannique et cibler conjointement des régions voisines pourrait être la clé pour enfin piéger la capacité d’échappement du VIH.
Citation: Gieselmann, L., DeLaitsch, A.T., Rohde, M. et al. Identification of a potent V3 glycan site broadly neutralizing antibody targeting an N332gp120 glycan-independent epitope. Nat Immunol 27, 572–585 (2026). https://doi.org/10.1038/s41590-025-02385-3
Mots-clés: anticorps neutralisants largement actifs contre le VIH, épitope glycan V3, anticorps 007, conception de vaccin contre le VIH, thérapie par combinaison d’anticorps