Clear Sky Science · fr
Ingénierie de la xylosyltransférase pour manipuler les protéoglycanes dans les cellules de mammifères
Pourquoi les « manteaux » cellulaires comptent
Chaque cellule de notre corps porte un « manteau » moléculaire qui l’aide à communiquer avec ses voisines et à percevoir son environnement. Une part importante de ce manteau est constituée de protéoglycanes — des protéines décorées de longues chaînes glucidiques qui font office de minuscules antennes pour les facteurs de croissance, les signaux immunitaires et les indices structuraux. Lorsque cette ornementation sucrée dysfonctionne, le développement peut être perturbé et des tissus tels que l’os et le muscle peuvent être gravement affectés. Pourtant, il a été difficile pour les chercheurs de cartographier précisément quelles protéines portent ces chaînes et comment les composants individuels du manteau influencent le comportement cellulaire. Cette étude présente une stratégie chimique précise pour marquer et reconstruire ces chaînes sucrées sur des cellules de mammifères vivantes, ouvrant la voie à la lecture et à la réécriture de l’information codée à leur surface. 
Reconfigurer la première étape de l’attachement du sucre
La construction des protéoglycanes commence lorsqu’une famille d’enzymes particulière, les xylosyltransférases XT1 et XT2, installe le premier sucre sur une protéine, marquant l’emplacement où une longue chaîne va se développer. Parce que les deux enzymes peuvent effectuer cette même première étape, il a été difficile de savoir sur quelles protéines chacune agit à l’intérieur des cellules. Les auteurs ont utilisé une conception « bump‑and‑hole » — courante en biologie chimique moderne — pour résoudre ce problème. Ils ont légèrement remodelé le site actif de XT1, créant un espace supplémentaire (le « trou »), et introduit un bloc de sucre correspondant, légèrement plus volumineux, le 6AzGlc (le « bossage »). La XT1 modifiée peut désormais utiliser ce sucre altéré, alors que l’enzyme naturelle ne le peut pas, permettant aux chercheurs de marquer uniquement les protéines touchées par l’enzyme repensée.
Faire entrer en douce un sucre sur mesure dans les cellules
Pour rendre cette approche opérationnelle dans des cellules vivantes, l’équipe a dû délivrer le sucre « bossé » sous une forme que le métabolisme cellulaire reconnaisse. Plutôt que de compter sur les voies normales d’absorption des sucres — qui ne traitent pas bien les analogues de la xylose — ils ont conçu une version masquée du 6AzGlc portant un groupe phosphate caché. Une fois dans le cytosol, des enzymes cellulaires dévoilent ce groupe et convertissent la molécule en UDP‑6AzGlc, la forme activée requise par les xylosyltransférases modifiées. Une chromatographie soigneuse a confirmé que les cellules traitées avec le composé masqué correctement configuré produisaient des quantités substantielles du sucre designer activé, tandis qu’un témoin image miroir en produisait presque aucune. 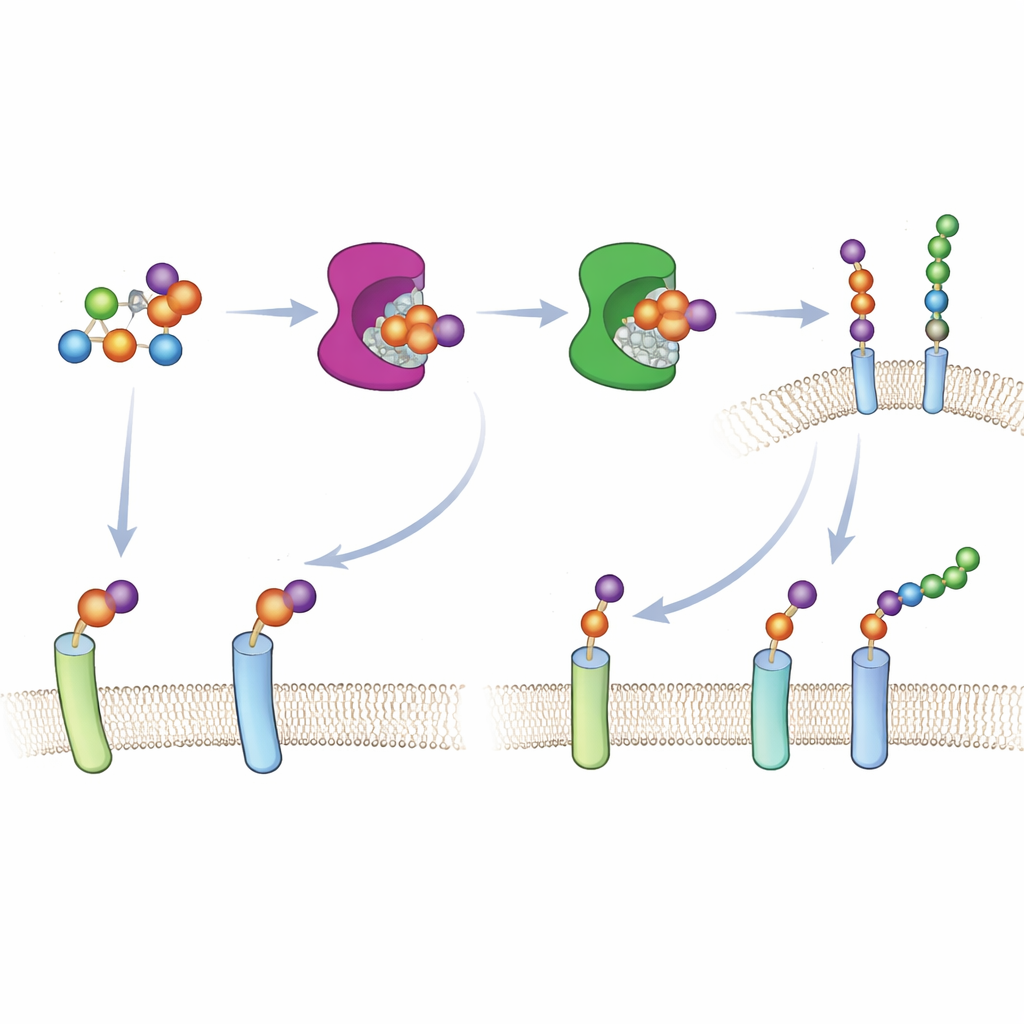
Marquer et identifier les acteurs cachés
Avec l’enzyme modifiée et le sucre activé en place, les chercheurs ont montré que seules les cellules exprimant la XT1 ou la XT2 modifiées incorporaient l’étiquette 6AzGlc dans leurs protéoglycanes de surface. Le groupe azide du 6AzGlc sert de petite poignée chimique qui peut être « clickée » avec des colorants fluorescents ou de la biotine, permettant la visualisation et l’enrichissement des protéines marquées. La spectrométrie de masse d’échantillons enrichis a révélé une riche collection de protéoglycanes connus — dont la décorine, plusieurs glypicanes, la syndécane‑4, CD44 et la versicane — confirmant que le système marque de véritables protéines porteuses de sucres. Il est important de noter que les enzymes modifiées ont conservé les mêmes préférences de séquence que leurs homologues naturels, ce qui signifie que l’étiquette chimique est installée aux sites d’attachement authentiques plutôt qu’à de nouvelles positions artificielles.
Construire des protéoglycanes sur mesure
Un bonus inattendu de l’étiquette 6AzGlc est que, contrairement au sucre de départ naturel, elle ne peut pas être étendue en une chaîne complète par les enzymes en aval. Cela cappe effectivement la chaîne et simplifie la structure moléculaire qui doit être analysée par spectrométrie de masse. Les auteurs ont transformé cette caractéristique en outil : après que XT1 ait installé le 6AzGlc à un site d’attachement naturel, ils utilisent la chimie click pour fixer des fragments d’héparine synthétiques, créant des « protéoglycanes sur mesure » avec des chaînes glucidiques précisément définies. Dans des cellules de cancer du sein dépourvues de leur propre syndécane‑1, le rétablissement de telles versions conçues a restauré l’étalement normal sur une surface recouverte de protéine, prouvant que le protéoglycane reconstruit chimiquement peut remplacer fonctionnellement l’original.
Ce que cela signifie pour la biologie et la médecine
Ce travail fournit un jeu d’outils puissant pour marquer sélectivement et manipuler les chaînes sucrées qui contrôlent la communication cellulaire. En séparant les rôles de XT1 et XT2 et en n’étiquetant que leurs cibles directes, les chercheurs peuvent désormais cartographier quels protéoglycanes opèrent dans des tissus spécifiques et dans des états pathologiques. La capacité d’arrêter la croissance naturelle des chaînes et de la remplacer par des sucres conçus permet aussi de disséquer dans quelle mesure la fonction d’un protéoglycane est portée par son épine dorsale protéique versus son manteau sucré. À long terme, une telle ingénierie de précision pourrait aider à décoder des signalements complexes à la surface cellulaire et inspirer des thérapies visant à réparer ou reprogrammer des manteaux cellulaires défectueux dans les troubles du développement, le cancer et d’autres maladies.
Citation: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Mots-clés: protéoglycanes, glycosaminoglycanes, xylosyltransférase, biologie chimique, signalisation à la surface cellulaire