Clear Sky Science · fr
Un seul site allostérique réunit activation, modulation et inhibition dans TRPM5
Comment un minuscule gardien module le goût et le métabolisme
Les aliments que nous apprécions et la manière dont nos organismes gèrent le sucre dépendent de protéines « gardiennes » microscopiques au sein de nos cellules. L’une d’elles, un canal nommé TRPM5, nous aide à percevoir les saveurs sucrées, amères et umami et participe à la libération d’insuline par le pancréas. Cette étude montre qu’un petit creux unique sur TRPM5 peut agir comme un bouton de commande maître : il peut mettre le canal en marche, régler sa sensibilité et même l’éteindre — des découvertes susceptibles d’éclairer la conception future de traitements pour le diabète, l’obésité et les troubles intestinaux.
Un canal au carrefour du goût et de la glycémie
TRPM5 se trouve dans la membrane des cellules gustatives de la langue, des cellules productrices d’hormones dans l’intestin et des cellules sécrétrices d’insuline dans le pancréas. Quand le calcium intracellulaire augmente, TRPM5 s’ouvre et laisse passer des ions chargés positivement, modifiant brièvement le potentiel de la cellule. Dans les bourgeons gustatifs, ce signal électrique informe le cerveau qu’il y a quelque chose de sucré, d’amer ou d’umami sur la langue. Dans le pancréas, il contribue à ajuster les poussées d’insuline après un repas. Les personnes et les animaux dont la fonction de TRPM5 est altérée présentent des anomalies de sécrétion d’insuline et de contrôle glycémique, ce qui suggère que cibler TRPM5 pourrait un jour aider à traiter les maladies métaboliques. Jusqu’à récemment, les chercheurs manquaient toutefois d’outils précis pour activer ou inhiber ce canal.
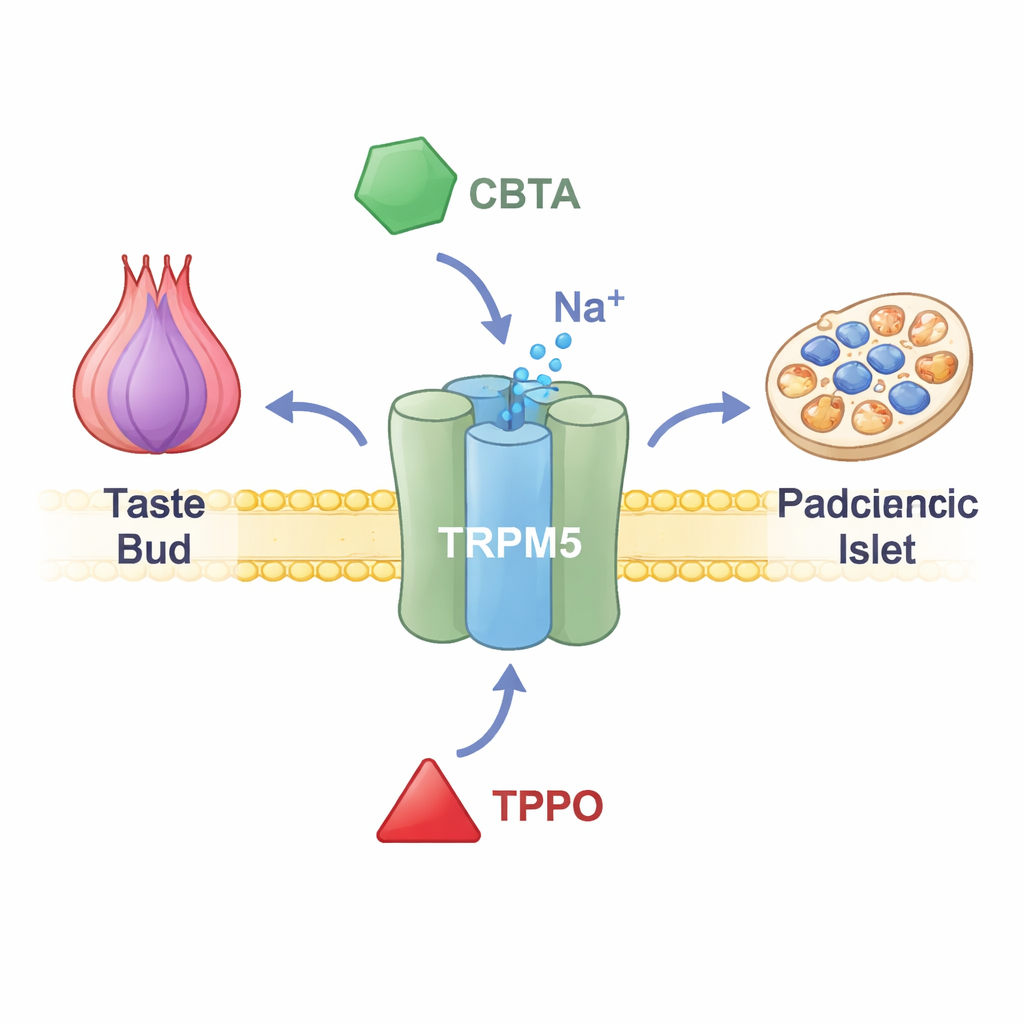
Un interrupteur chimique qui suractive le canal
Les chercheurs se sont intéressés à un composé synthétique appelé CBTA, connu pour stimuler TRPM5 mais jusqu’alors mal compris. À l’aide d’enregistrements électriques de cellules génétiquement modifiées pour exprimer TRPM5, ils ont montré que CBTA peut ouvrir le canal même lorsque le calcium est presque absent, prouvant qu’il s’agit d’un vrai activateur et non d’un simple amplificateur de l’effet du calcium. Lorsque de faibles quantités de calcium sont présentes — des niveaux qui laissent normalement TRPM5 au repos — CBTA et le calcium agissent ensemble, générant des courants bien plus importants que l’un ou l’autre seul. Autrement dit, CBTA rend TRPM5 extraordinairement sensible : des concentrations de calcium proches du niveau basal deviennent soudain suffisantes pour déclencher l’ouverture complète du canal.
Un site de contrôle caché révélé par cryo‑EM
Pour comprendre ce mécanisme au niveau atomique, l’équipe a utilisé la cryo‑microscopie électronique pour capturer des clichés tridimensionnels de TRPM5 dans différentes conditions. Ils ont découvert que CBTA se loge dans une cavité jusque‑là inaperçue, située dans la partie supérieure d’une région sensible à la tension du canal, juste au‑dessus du site où le calcium se lie habituellement. Cette cavité, formée par un regroupement d’acides aminés, sert de site d’accrochage précis. Lorsque les chercheurs ont muté des éléments clés qui bordent cette poche, CBTA n’a plus pu activer TRPM5, même si le calcium conservait son effet, confirmant que cette petite niche est essentielle à l’action du composé. Fait marquant, la liaison de CBTA réarrange subtilement des segments voisins de la protéine d’une manière qui facilite l’occupation du site calcique classique, ce qui explique la forte synergie observée dans les mesures électriques.
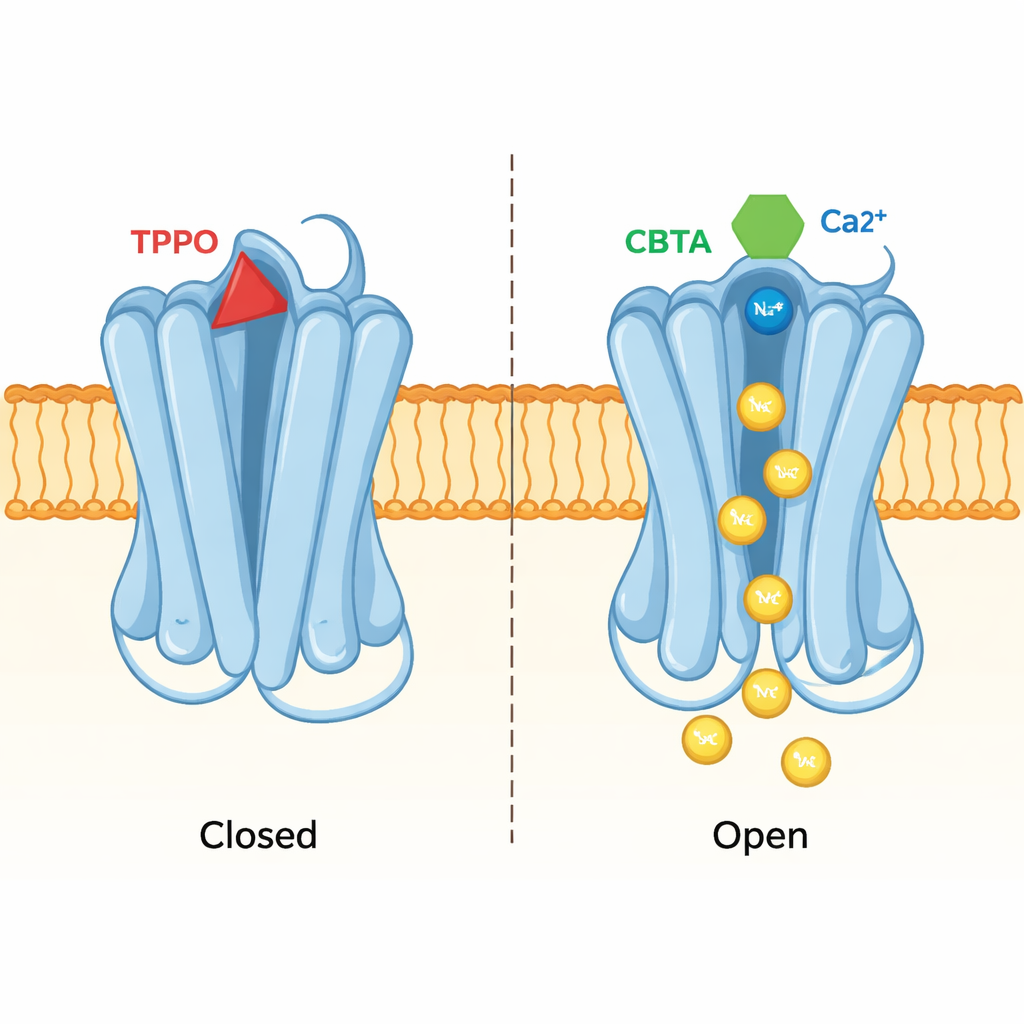
Une même poche, deux effets opposés
La même approche structurale a permis de montrer comment un inhibiteur, le TPPO, utilise exactement cette même poche pour produire l’effet inverse. Lorsque TPPO se lie, les deux sites calciques de TRPM5 peuvent rester occupés, mais le pore central du canal reste pincé et aucun ion ne le traverse. La comparaison des structures liées à TPPO et à CBTA révèle que leurs formes différentes poussent des segments protéiques voisins dans des directions opposées. CBTA favorise des mouvements qui se propagent jusqu’au pore et l’ouvrent ; TPPO, au contraire, perturbe la communication entre la poche et le pore, maintenant la fermeture du passage. En substance, une même poche peut agir soit comme un accélérateur, soit comme un frein, selon la molécule qui l’occupe.
Reconfigurer le câblage interne du canal
L’étude montre également que ce site de contrôle peut remplacer des fonctions normalement assurées par une région de liaison au calcium située du côté intracellular. Dans des canaux mutants où le site calcique interne habituel est désactivé, le calcium seul ne peut pas ouvrir TRPM5. Pourtant, CBTA active toujours ces mutants et restructure un élément clé qui relie les parties interne et externe du canal. Dans d’autres mutants qui interrompent la connexion entre la liaison du calcium et l’ouverture du pore, l’ajout de CBTA restaure le comportement normal. Ces résultats révèlent que le site nouvellement identifié peut contourner ou réparer la communication entre différents domaines du canal, agissant comme un hub flexible pour la signalisation à longue portée au sein de la protéine.
Pourquoi cela compte pour les médicaments de demain
Pour un public non spécialiste, l’essentiel est que les chercheurs ont identifié une unique poche sensible aux médicaments sur TRPM5 capable d’intégrer activation, réglage fin et inhibition. Un petit activateur comme le CBTA peut à la fois mimer le calcium et accroître fortement la sensibilité du canal, tandis qu’un autre composé, le TPPO, peut verrouiller ce même canal fermé — le tout en se fixant au même endroit. Cette vision unifiée du contrôle de TRPM5 ouvre la voie à la conception de molécules ciblées qui renforcent ou atténuent son activité dans des tissus spécifiques, avec des applications potentielles allant de l’amélioration des thérapies basées sur le goût et des médicaments pour la motricité intestinale à de nouvelles stratégies de gestion de la glycémie et des maladies métaboliques.
Citation: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Mots-clés: canal TRPM5, perception du goût, sécrétion d’insuline, ouverture des canaux ioniques, modulation allostérique