Clear Sky Science · fr
Analyses d’association génomique de l’hypothyroïdie auto-immune révèlent des contributions spécifiques au système immunitaire et à la thyroïde et une relation inverse avec le risque de cancer
Pourquoi cela compte pour la santé quotidienne
Beaucoup de personnes se sentent fatiguées, ont froid ou une certaine brume mentale sans se douter que leur glande thyroïde peut en être la cause. L’hypothyroïdie auto-immune, où les défenses de l’organisme attaquent lentement la thyroïde, touche plus d’une personne sur vingt. Cette étude utilise des données génétiques provenant de centaines de milliers de volontaires pour poser deux grandes questions : quels changements héréditaires dans notre ADN rendent cette affection plus probable, et comment ces mêmes changements sont-ils liés au risque de développer un cancer ? Les réponses révèlent un compromis surprenant entre un système immunitaire qui peut parfois nuire à la thyroïde mais offrir en même temps une protection supplémentaire contre les tumeurs.
Regarder à l’échelle du génome
Les chercheurs ont combiné dossiers de santé et informations génétiques de deux grands projets populationnels, FinnGen en Finlande et l’UK Biobank au Royaume-Uni. Ils se sont concentrés sur les personnes nécessitant un traitement hormonal thyroïdien à long terme et ont soigneusement exclu celles dont les troubles thyroïdiens étaient dus à une chirurgie, un cancer ou d’autres causes non auto-immunes. Cela a permis d’identifier plus de 81 000 cas d’hypothyroïdie auto-immune et plus de 700 000 témoins, faisant de cette étude la plus vaste à ce jour. En scannant des millions de marqueurs d’ADN sur l’ensemble du génome, ils ont découvert 418 signaux génétiques indépendants en dehors du principal cluster de gènes immunitaires, répartis sur au moins 280 régions du génome. Beaucoup de ces signaux impliquaient des variations rares ou à faible fréquence qui modifient la structure des protéines, donnant des indices directs sur la biologie sous-jacente.
Séparer les effets immunitaires généraux des effets spécifiques à la thyroïde
L’hypothyroïdie auto-immune se situe à l’intersection de l’auto-immunité générale et de la biologie spécifique de la thyroïde. Pour démêler ces composantes, l’équipe a comparé ses résultats avec des études génétiques d’autres maladies auto-immunes et avec les taux sanguins d’hormone stimulant la thyroïde, le marqueur clinique clé pour détecter une thyroïde peu active. En utilisant une méthode bayésienne de classification, ils ont regroupé les signaux génétiques en ceux partagés avec des maladies auto-immunes larges et ceux plus spécifiques à la régulation hormonale thyroïdienne. Ils estiment qu’environ 38 % des signaux agissent via des voies immunitaires générales influençant de nombreuses pathologies auto-immunes, tandis qu’environ 20 % agissent principalement via la fonction thyroïdienne elle‑même. Les variants axés sur la thyroïde avaient tendance à influencer les taux hormonaux et des gènes actifs dans le tissu thyroïdien, alors que les variants immunitaires généraux étaient plus actifs dans les cellules T, les globules blancs qui orchestrent les réponses immunitaires.
Approfondir un commutateur immunitaire clé
Une découverte particulièrement marquante concernait une variation d’ADN rare dans le gène ZAP70, qui code pour une protéine de signalisation essentielle au sein des cellules T. De sévères défauts de cette protéine sont connus pour provoquer une immunodéficience profonde, mais le variant identifié ici entraîne seulement une perte partielle de fonction. Des expériences en laboratoire sur des cellules T génétiquement modifiées ont montré que ce ZAP70 altéré affaiblit, sans toutefois bloquer complètement, la cascade de signaux qui suit normalement la reconnaissance d’une cible. Les cellules porteuses du variant étaient moins aptes à activer des marqueurs d’activation et les étapes de signalisation en aval. Cette réponse amoindrie semble perturber l’équilibre délicat qui élimine normalement les cellules T auto‑réactives, prédisposant ainsi les porteurs à des maladies auto-immunes tout en augmentant modestement leur risque de certaines déficiences immunitaires.
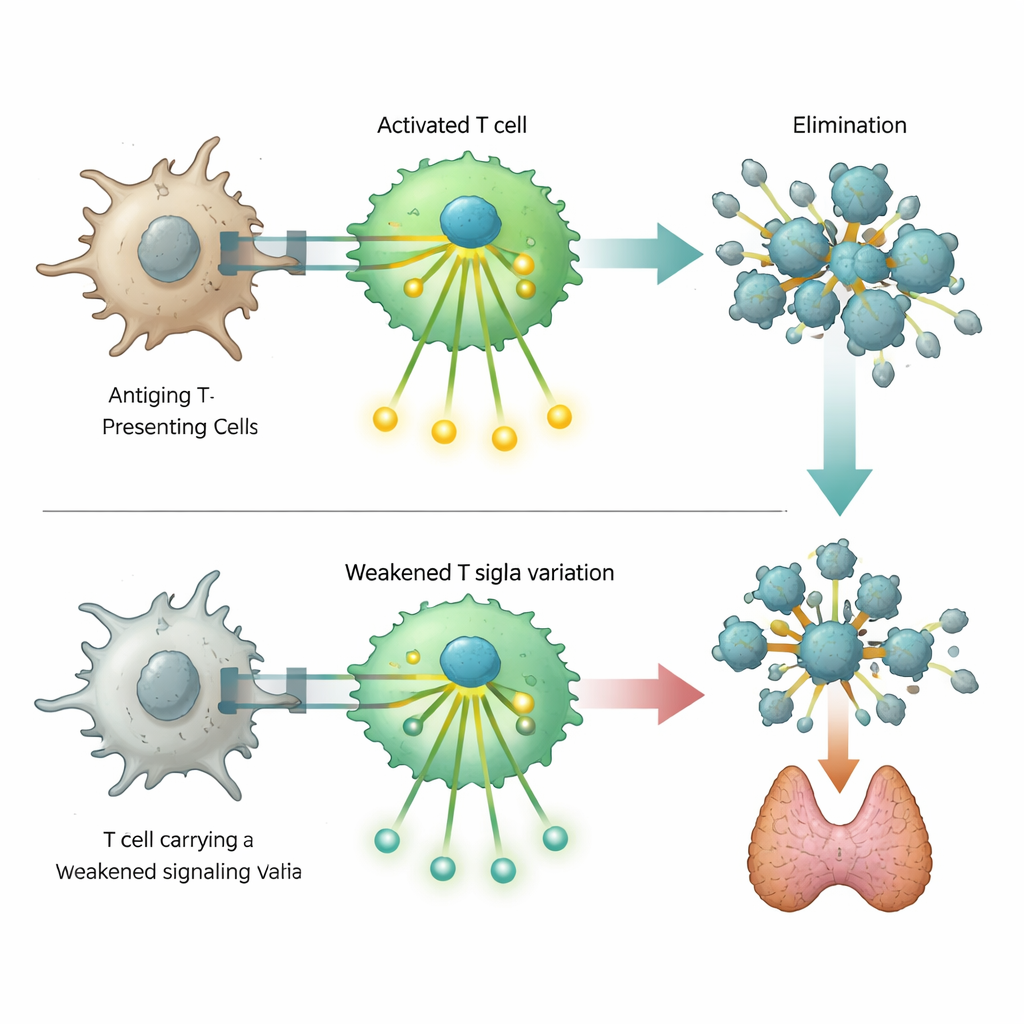
Un lien inattendu avec la protection contre le cancer
Comme les mêmes voies immunitaires qui provoquent l’auto-immunité peuvent aussi attaquer les tumeurs, les auteurs ont ensuite examiné comment la génétique de l’hypothyroïdie auto-immune se rapporte au risque de cancer. Ils ont calculé un score de risque polygénique résumant la propension héréditaire de chaque individu à développer une hypothyroïdie et ont testé son association avec de nombreuses maladies dans les données finlandaises. Comme attendu, un score plus élevé corrélait avec un risque accru de diverses affections auto-immunes. Plus surprenant fut un schéma constant de risque réduit pour plusieurs cancers, en particulier le carcinome basocellulaire et d’autres cancers de la peau, mais aussi le cancer du sein et de la prostate et un regroupement global « tous cancers ». Lorsque l’équipe a examiné directement des analyses génomiques de cancer, environ 10 % des sites liés à l’hypothyroïdie influençaient également le cancer de la peau, le même variant génétique augmentant généralement l’auto-immunité thyroïdienne tout en diminuant le risque de cancer cutané. Ces variants partagés se concentraient dans des gènes liés au système immunitaire, y compris des cibles médicamenteuses bien connues utilisées en immunothérapie par inhibition de points de contrôle.
Ce que cela signifie pour les patients et la médecine
Vu de manière vulgarisée, ce travail montre que certaines personnes naissent avec un système immunitaire légèrement « plus chaud », les rendant plus sujettes à des lésions lentes et souvent silencieuses de la thyroïde mais, en même temps, mieux équipées pour repérer et éliminer les cancers naissants. L’étude distingue quelles variations génétiques agissent via une suractivité immunitaire générale et lesquelles affectent spécifiquement la production d’hormones thyroïdiennes, expliquant pourquoi des affections comme la maladie de Hashimoto et la maladie de Basedow peuvent partager certains gènes de risque tout en poussant la fonction thyroïdienne dans des directions opposées. Elle aide aussi à comprendre pourquoi les patients qui développent des problèmes thyroïdiens lors de traitements anticancéreux stimulant le système immunitaire répondent souvent mieux à ces traitements. Globalement, les résultats suggèrent que la variation naturelle courante dans les gènes de points de contrôle et de signalisation immunitaires façonne à la fois la maladie thyroïdienne auto-immune et le risque de cancer au cours de la vie, offrant de nouvelles pistes pour la prévention et une utilisation plus personnalisée des immunothérapies.
Citation: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Mots-clés: hypothyroïdie auto-immune, maladie thyroïdienne, risque génétique, système immunitaire, protection contre le cancer