Clear Sky Science · fr
Des expansions de répétitions GGC dans de nouveaux cadres de lecture ouverts sont traduites en protéines polyglycine toxiques dans la myopathie oculopharyngodistale
Messages cachés dans notre ADN
La plupart d’entre nous ont appris à l’école qu’une petite portion seulement de notre ADN code pour des protéines, tandis que le reste était autrefois considéré comme de la « poubelle ». Cette étude renverse cette idée. Elle montre que de courtes séquences répétées, négligées, peuvent secrètement donner naissance à de nouvelles protéines qui endommagent les muscles et le cerveau, contribuant à expliquer un groupe de maladies neurologiques rares mais dévastatrices — et indiquant une voie possible de traitement.
ADN répétitif et maladies musculaires mystérieuses
Notre génome est rempli de courtes séquences répétées, comme des syllabes de trois lettres copiées encore et encore. Lorsque certaines de ces répétitions s’allongent excessivement, elles peuvent causer plus de 60 maladies humaines connues. Dans la myopathie oculopharyngodistale (OPDM) et un trouble connexe avec atteintes cérébrales nommé OPML, les patients présentent des paupières tombantes, des difficultés à avaler, une faiblesse des mains et des pieds, et parfois des atteintes nerveuses et cérébrales plus larges. Au microscope, les médecins observent des amas protéiques caractéristiques à l’intérieur des cellules musculaires et nerveuses, mais jusqu’à présent il n’était pas clair comment des répétitions situées dans des régions supposées « non codantes » de l’ADN pouvaient produire des protéines toxiques.
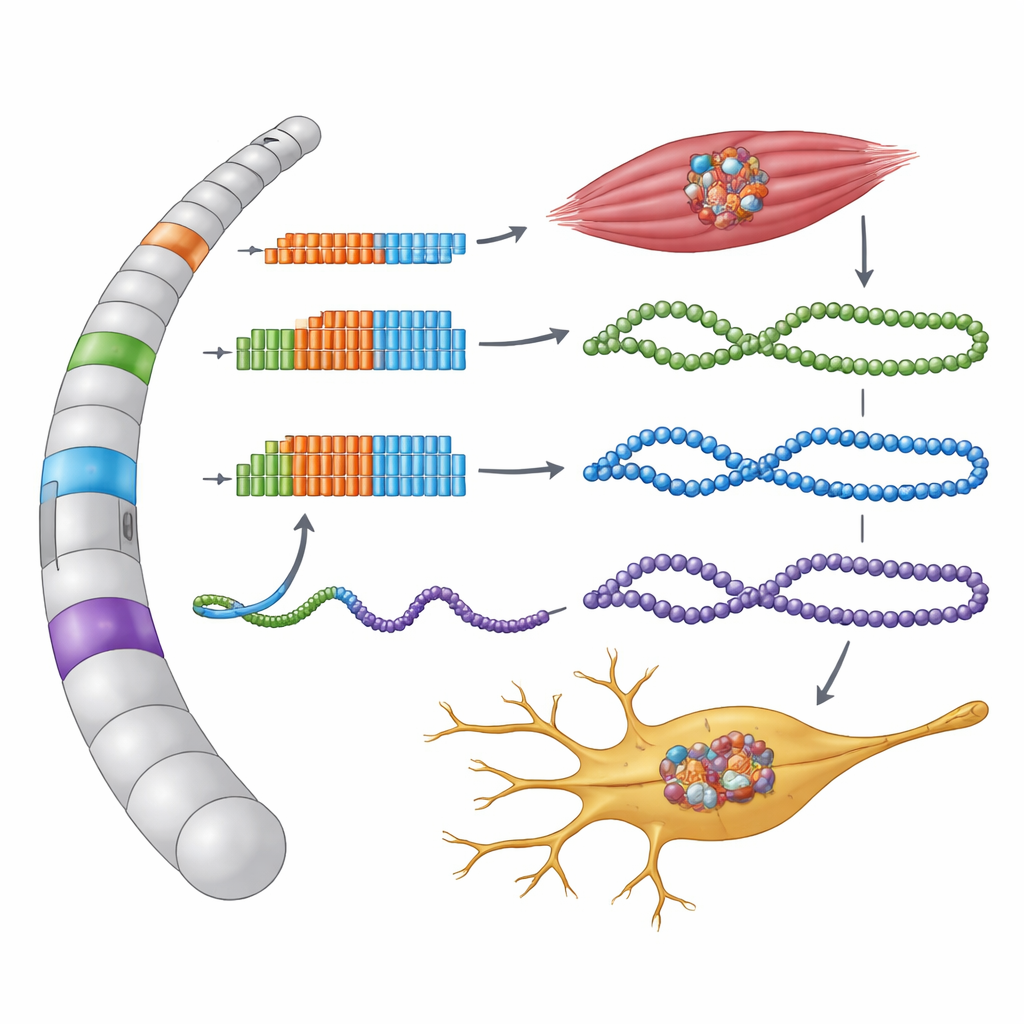
Des régions non codantes qui fabriquent secrètement des protéines
Les chercheurs se sont concentrés sur des régions d’ADN où la séquence de trois lettres GGC est répétée de nombreuses fois dans plusieurs gènes associés à l’OPDM et l’OPML. Ces répétitions se trouvent dans des zones annotées comme non codantes — des queues non traduites de gènes ou de longs ARN censés ne pas produire de protéines. En recréant ces séquences humaines dans des cellules et en suivant leur lecture, l’équipe a découvert que chaque segment de GGC se situe en réalité à l’intérieur d’une petite unité codante précédemment non reconnue, appelée petit cadre de lecture ouvert. Lorsque les cellules lisent ces instructions cachées, chaque répétition GGC est traduite en l’acide aminé glycine, formant de longues queues « polyglycine » sur de nouvelles microprotéines.
Nouvelles protéines toxiques qui s’agglomèrent et tuent les cellules
À l’aide d’anticorps personnalisés, les scientifiques ont montré que ces microprotéines portant des polyglycines sont présentes dans des échantillons musculaires de patients et se concentrent exactement là où l’on observe les étranges amas protéiques p62-positifs. Ils ont ensuite forcé des cellules musculaires humaines, des drosophiles et des souris à produire les mêmes types de protéines polyglycine. Dans les trois systèmes, les protéines se sont condensées en inclusions rondes et denses dans le cytoplasme et le noyau, ressemblant à ce que l’on voit dans les tissus des patients. Les cellules produisant ces protéines étaient plus susceptibles de mourir, et chez la souris les muscles affectés présentaient des fibres atrophiées, des noyaux internalisés et des signes d’inflammation. Lorsque ces protéines s’accumulaient dans le cerveau et le cœur, les animaux développaient des troubles du mouvement, une neurodégénérescence, une cardiomyopathie et une durée de vie réduite, reflétant de nombreux symptômes rapportés chez les patients.

Une caractéristique toxique centrale, de nombreuses variantes locales
Bien que ces microprotéines partagent la même caractéristique centrale — une longue chaîne de résidus de glycine — elles ne sont pas identiques. Chacune provient d’un petit cadre de lecture différent dans un gène distinct et possède donc des segments d’acides aminés uniques encadrant la portion polyglycine. L’équipe a constaté que ces segments environnants influencent fortement le comportement des protéines : où dans la cellule elles s’accumulent, leur propension à former des agrégats, les partenaires cellulaires avec lesquels elles interagissent et leur toxicité pour les cellules musculaires et nerveuses. Certaines variantes étaient particulièrement délétères, déclenchant rapidement la formation d’inclusions et la mort cellulaire, tandis que d’autres étaient plus modérées. Cela suggère un mécanisme toxique central commun, modulé par le contexte séquentiel local.
Un premier pas vers une stratégie thérapeutique partagée
De manière encourageante, les chercheurs ont également identifié une petite molécule, la porphyrine cationique TMPyP4, capable de diminuer à la fois l’accumulation et la toxicité de ces protéines polyglycine dans des cellules et dans un modèle de drosophile. TMPyP4 semble agir principalement en perturbant la traduction des régions riches en GC, réduisant la production des protéines nocives sans arrêter de manière générale la synthèse protéique. Loin d’être un médicament prêt à l’emploi, elle fournit néanmoins une preuve de principe qu’une approche thérapeutique unique pourrait un jour aider des patients atteints de plusieurs affections apparentées entraînées par des expansions de répétitions similaires.
Ce que cela change dans notre compréhension des maladies
Pour le non-spécialiste, le message central est frappant : des pans d’ADN longtemps catalogués comme non codants peuvent cacher de petites recettes protéiques qui deviennent dangereuses lorsque certaines répétitions s’étendent. Dans l’OPDM, l’OPML, la maladie d’inclusion intranucléaire neuronale et des troubles apparentés, ces répétitions GGC étendues sont traduites en protéines polyglycine adhésives qui s’agglutinent à l’intérieur des cellules et compromettent progressivement les muscles, les nerfs et le cerveau. En révélant ce mécanisme commun et un premier composé candidat capable de l’atténuer, l’étude élargit notre conception de ce qui constitue un gène et ouvre de nouvelles voies pour traiter une famille croissante de maladies neurologiques liées aux expansions de répétitions.
Citation: Boivin, M., Yu, J., Eura, N. et al. GGC repeat expansions within new open reading frames are translated into toxic polyglycine proteins in oculopharyngodistal myopathy. Nat Genet 58, 517–529 (2026). https://doi.org/10.1038/s41588-026-02507-z
Mots-clés: myopathie oculopharyngodistale, expansion de répétitions microsatellites, protéines polyglycine, traduction de l’ADN non codant, maladie neurodégénérative musculaire