Clear Sky Science · fr
Expression réduite de la cycline D3 dans les cellules érythroïdes protège contre le paludisme
Comment une différence sanguine subtile peut lutter contre un parasite mortel
Le paludisme a façonné l’évolution humaine pendant des millénaires en favorisant des modifications génétiques qui aident les individus à survivre à l’infection. Cette étude met au jour l’une de ces modifications dans une population sarde : un petit changement d’ADN qui modifie légèrement la production des globules rouges. Ce changement réduit le nombre de globules rouges et augmente leur taille, élève leur chimie interne de stress et, ce faisant, compromet discrètement le parasite du paludisme qui dépend de ces cellules pour se développer.
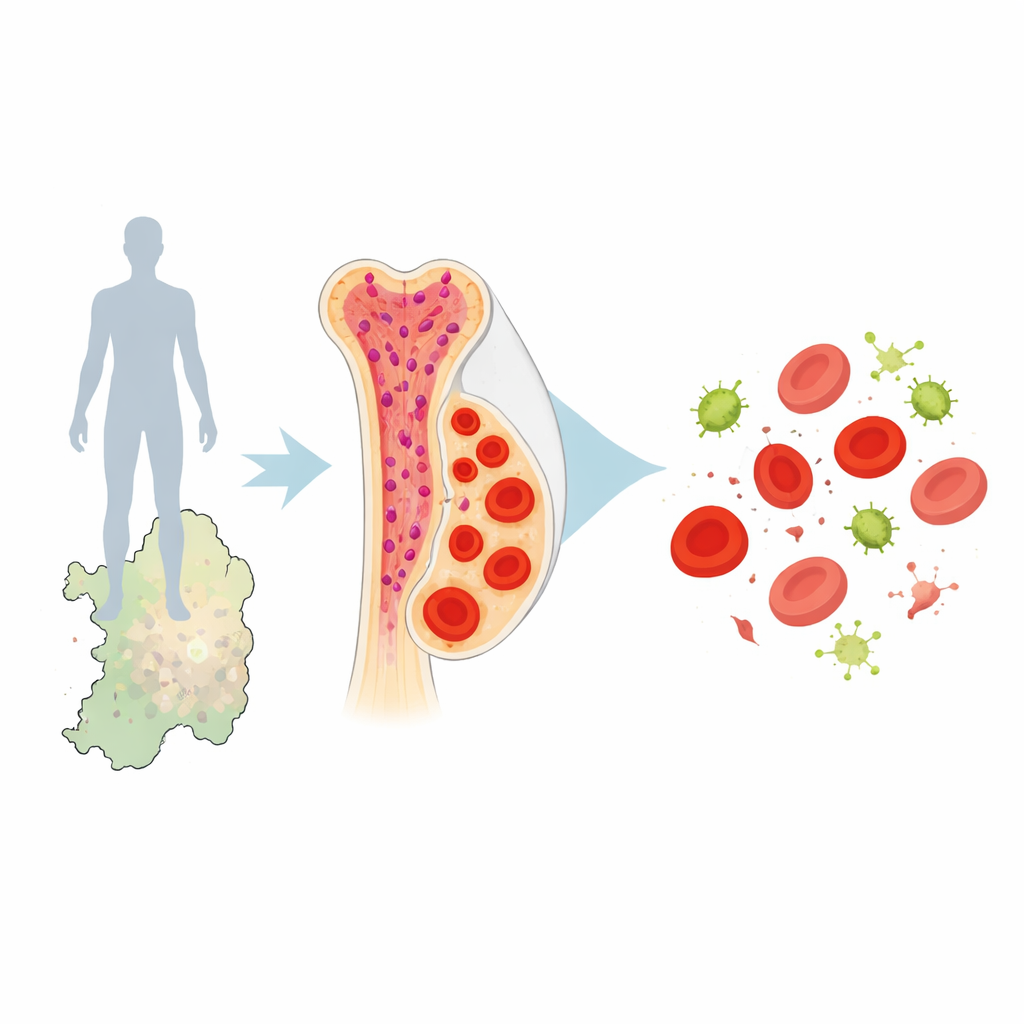
Un minuscule changement d’ADN aux grandes conséquences
Les chercheurs se sont concentrés sur une région de notre ADN qui contrôle une protéine appelée cycline D3, impliquée dans la division des cellules sanguines immatures. Dans des travaux antérieurs, un variant génétique nommé rs112233623-T, proche du gène CCND3, avait été associé à des globules rouges en moins grand nombre mais de plus grande taille, ainsi qu’à des niveaux plus élevés de certaines formes d’hémoglobine. Ce variant est environ dix fois plus fréquent chez les Sardes que chez de nombreux autres Européens, rappelant l’histoire de l’île en tant que foyer ancien du paludisme. L’équipe s’est posé une série de questions liées : comment ce variant modifie-t-il le développement des cellules sanguines, pourquoi est-il si fréquent en Sardaigne, et freine-t-il réellement les parasites du paludisme ?
Ralentir l’usine du cycle cellulaire pour les globules rouges
Pour comprendre l’effet du variant dans les cellules, les scientifiques ont cultivé des précurseurs des globules rouges issus de volontaires portant soit deux copies de rs112233623-T, soit deux copies de la version habituelle. Dans les cellules porteuses du variant, les niveaux de cycline D3 étaient nettement plus faibles et les cellules progressaient plus lentement à travers la phase du cycle où l’ADN est copié et les cellules se divisent. En conséquence, chaque précurseur a subi moins de cycles de division avant de mûrir, produisant un profil sanguin avec moins de globules rouges mais plus grands — très similaire à ce qui avait été observé chez des souris dépourvues de cycline D3. Dans des analyses génétiques portant sur des milliers de volontaires sardes, le variant rs112233623-T est apparu comme le principal moteur de ce schéma de cellules sanguines.
Reprogrammer un interrupteur génétique dans les précurseurs sanguins
Le changement d’ADN crucial se situe dans une région de contrôle « marche–arrêt », ou enhancers, qui augmente l’activité de CCND3 dans les cellules rouges en développement. L’équipe a montré que l’introduction de la version rs112233623-T affaiblissait nettement cet enhancer dans des tests rapporteurs en laboratoire. En disséquant la séquence environnante, ils ont trouvé que la séquence normale forme une plate-forme d’ancrage pour une protéine appelée SMAD3, qui active CCND3. La version T perturbe cette plate-forme et favorise à la place la fixation de GATA1, une protéine qui joue ici plutôt le rôle d’un frein. Dans de vrais précurseurs sanguins, SMAD3 se liait fortement à la séquence normale mais peu à la variante, et des médicaments bloquant les signaux de type SMAD entraînaient une baisse des niveaux de cycline D3. Ensemble, ces expériences révèlent une logique simple : moins de signaux « go » de SMAD3 et plus de signaux « stop » de GATA1 signifient moins de CCND3, une division cellulaire plus lente et une production de globules rouges modifiée.
Une signature évolutive d’un paludisme passé
Pourquoi ce variant apparemment désavantageux est-il devenu courant en Sardaigne ? Les analyses de génétique des populations fournissent un indice. Comparés à d’autres Européens, les Sardes présentent une fréquence anormalement élevée de rs112233623-T, de longues régions d’ADN autour de ce site avec peu de variation, et des schémas mieux expliqués par une sélection positive récente que par le hasard. À l’aide de modèles décrivant l’augmentation de fréquence des variants au fil des générations, les auteurs estiment que rs112233623-T a été fortement favorisé dans le passé récent de la Sardaigne. Étant donné que l’île a connu une transmission intense du paludisme jusqu’au milieu du XXe siècle, les auteurs en déduisent que la protection contre le paludisme est l’avantage le plus probable.
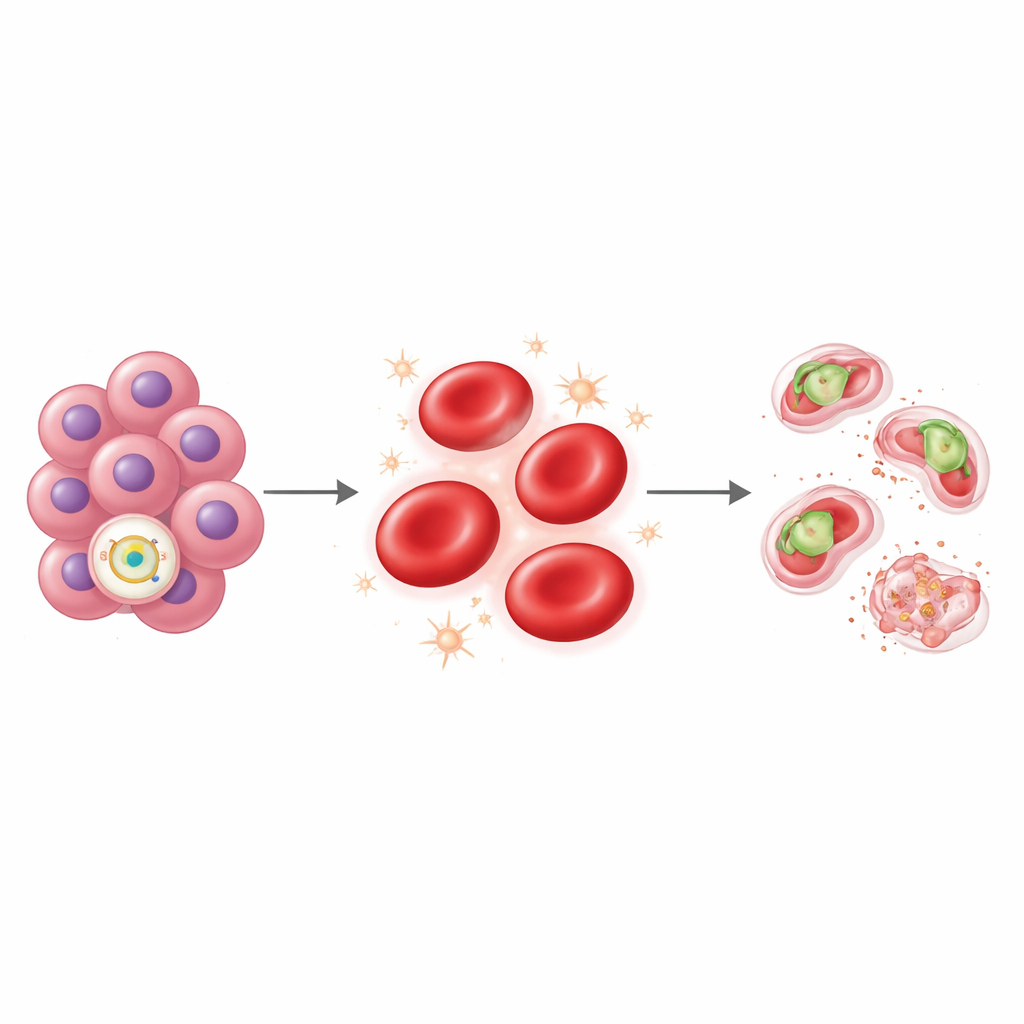
Épuiser le parasite par le stress à l’intérieur de la cellule
Pour tester cette hypothèse directement, l’équipe a infecté des globules rouges de volontaires sardes soigneusement génotypés avec Plasmodium falciparum, le parasite responsable de la forme la plus mortelle du paludisme. Les globules rouges de personnes porteuses du variant rs112233623-T ont permis une croissance parasitaire bien moindre sur plusieurs cycles que les cellules de sujets dépourvus du variant. Les parasites dans ces cellules étaient souvent bloqués et mouraient au lieu d’achever leurs stades de développement habituels. En mesurant la chimie à l’intérieur des globules rouges, les chercheurs ont détecté des niveaux plus élevés d’espèces réactives de l’oxygène — des molécules provoquant un stress oxydatif — chez les porteurs du variant. Plus le stress oxydatif était élevé, moins les parasites croissaient, formant une relation inverse étroite. Fait notable, ce même handicap lié au stress rappelait ce qui est observé chez les personnes présentant un trait protecteur bien connu : une déficience en enzyme G6PD, historiquement associée à une résistance contre le paludisme sévère.
Ce que cela signifie pour la lutte future contre le paludisme
En termes simples, l’étude montre que réduire l’expression de cycline D3 dans les précurseurs des globules rouges rend les cellules résultantes plus hostiles pour les parasites du paludisme, principalement en augmentant une chimie interne d’« oxydation » que le parasite ne peut pas entièrement supporter. Ce ralentissement hérité et modéré de la production des globules rouges semble avoir été favorisé par la sélection naturelle en Sardaigne parce qu’il réduisait le risque d’infections graves et surchargées en parasites. Ces travaux suggèrent que des médicaments imitant temporairement cet effet génétique — en inhibant CCND3 dans la moelle osseuse — pourraient compléter les traitements antipaludiques existants, faisant pencher la balance encore davantage contre le parasite tout en restant dans des limites tolérables pour l’organisme humain.
Citation: Marini, M.G., Mingoia, M., Steri, M. et al. Reduced cyclin D3 expression in erythroid cells protects against malaria. Nature 651, 698–706 (2026). https://doi.org/10.1038/s41586-026-10110-9
Mots-clés: résistance au paludisme, globules rouges, évolution humaine, variant génétique, stress oxydatif