Clear Sky Science · fr
Des GlycoARN complexés avec l’héparane sulfate régulent la signalisation VEGF-A
Comment les cellules ajustent finement les signaux de formation des vaisseaux
Les vaisseaux sanguins ne surgissent pas partout où des signaux de croissance apparaissent — ils doivent être précisément régulés pour nourrir les tissus sans alimenter les tumeurs ni provoquer de cécité. Cet article révèle un « frein » inattendu sur un signal majeur de néovascularisation appelé VEGF-A. Les auteurs montrent que de petits fragments d’ARN, décorant l’extérieur des cellules en association avec des sucres et des protéines, peuvent atténuer le message de VEGF-A, modifiant ainsi notre compréhension du langage que les cellules utilisent à leur surface.
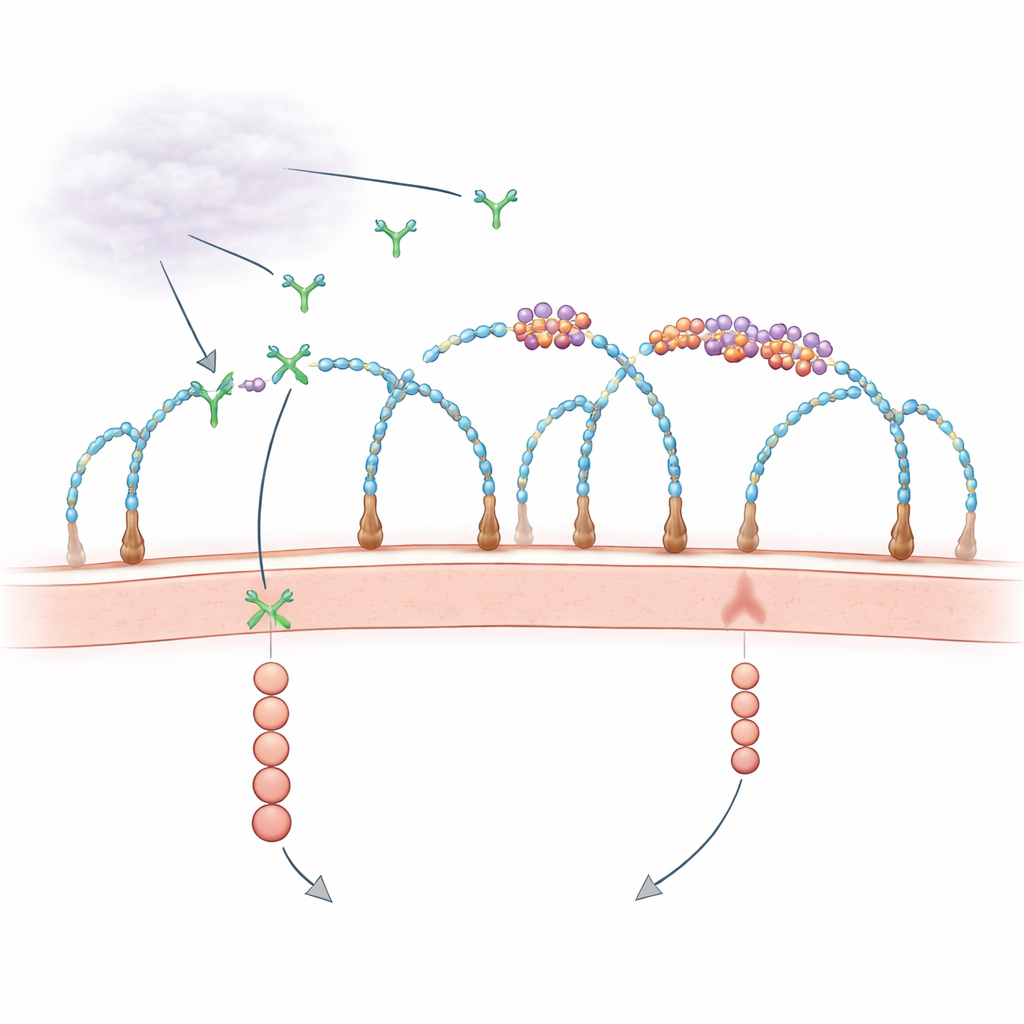
Un rôle surprenant de l’ARN à la surface cellulaire
Depuis des décennies, les biologistes savent que la couche externe de la cellule, riche en protéines décorées de sucres appelées protéoglycanes à héparane sulfate, aide à capturer les facteurs de croissance et à les présenter à leurs récepteurs. Parallèlement, des observations isolées laissaient entendre que des fragments d’ARN extracellulaires pouvaient influencer la croissance des vaisseaux, mais les acteurs et les mécanismes restaient flous. Des travaux récents ont montré que certains petits ARN sont chimiquement liés à des sucres complexes pour former des « glycoARN », et que certaines protéines liant l’ARN apparaissent également à la surface cellulaire, se regroupant avec ces ARN. La nouvelle étude pose une question précise : ces minuscules îlots ARN–protéine à la membrane contrôlent-ils réellement la réception des signaux de croissance comme VEGF-A ?
Assembler des îlots ARN–protéine groupés avec des chaînes sucrées
En utilisant des écrans CRISPR en aval à l’échelle du génome et de la microscopie à haute résolution, les chercheurs ont découvert que des chaînes de sucres spécifiques — l’héparane sulfate avec des décorations de sulfate particulières — sont des échafaudages essentiels pour l’assemblage de ces amas ARN–protéine, qu’ils appellent ribonucléoprotéines à la surface cellulaire (csRNPs). Lorsque des enzymes clés qui construisent ou sulfater l’héparane sulfate ont été éliminées, les amas de glycoARN et de leurs protéines partenaires ont disparu de la surface, bien que les ARN et protéines soient toujours présents à l’intérieur des cellules. Des enzymes qui clivent les chaînes d’héparane sulfate à la surface ou qui bloquent chimiquement la sulfation ont eu le même effet. Ces résultats montrent que des chaînes d’héparane sulfate intactes et correctement sulfates organisent les csRNPs en îlots nanoscopiques à la membrane.
Les amas d’ARN font office de freins sur un puissant signal pro-vasculaire
L’équipe s’est ensuite tournée vers des cellules endothéliales humaines, qui tapissent les vaisseaux et répondent au VEGF-A. Ils ont constaté que ces cellules exposent aussi des amas csRNP ancrés à l’héparane sulfate. Le traitement des cellules vivantes par des RNases, enzymes qui dégradent l’ARN, a éliminé la composante ARN sans perturber les chaînes sucrées sous-jacentes. Dans ces conditions, la forme la plus courante de VEGF-A qui se lie à l’héparane (VEGF-A165) a déclenché une activation beaucoup plus forte de la voie de signalisation ERK en aval, tandis qu’une forme plus courte dépourvue de la queue liant l’héparane (VEGF-A121) est restée inchangée. Davantage de molécules de VEGF-A165 se sont liées à la surface cellulaire après la suppression de l’ARN, alors que les niveaux de récepteur restaient identiques. Dans des dispositifs microfluidiques 3D, les cellules endothéliales exposées aux RNases ont pénétré plus loin dans des gels de collagène et formé des structures tubulaires de manière plus robuste, indiquant que la destruction de l’ARN de surface libère un comportement pro-angiogénique.
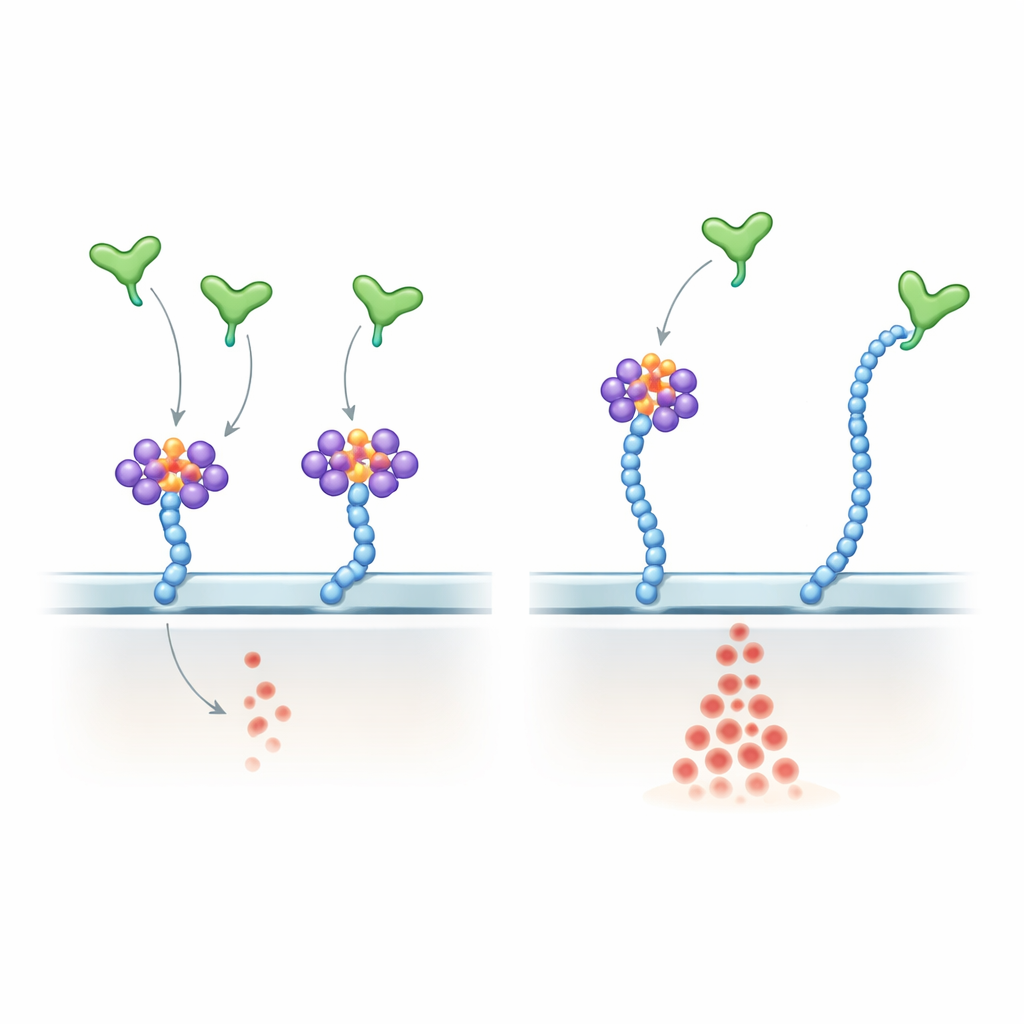
Disséquer comment VEGF-A perçoit l’ARN versus les sucres
Pour sonder le mécanisme, les auteurs ont montré que le VEGF-A165 se lie directement à certains petits ARN, y compris de nombreux glycoARN connus, via sa région C-terminale chargée positivement — la même région qui se lie à l’héparane sulfate. Ils ont conçu une version subtilement modifiée de VEGF-A165 dans laquelle des résidus d’arginine clés de cette queue ont été remplacés par des lysines. Ce mutant a conservé sa charge globale positive et continuait à interagir avec les chaînes d’héparane sulfate, mais il se liait mal aux glycoARN et est devenu largement insensible au traitement par RNase. Dans les cellules endothéliales, le mutant a produit une activation ERK plus forte et plus résistante aux RNases que le VEGF-A165 normal, reproduisant de près l’effet de la suppression de l’ARN à la surface. Chez la souris vivante, l’injection de ce mutant dans l’œil a provoqué une croissance vasculaire rétinienne plus exubérante que la protéine normale. Chez l’embryon de zebrafish, la surexpression de la version mutante de Vegfa a perturbé le patronage normal des vaisseaux et augmenté le nombre de cellules endothéliales.
Du mécanisme de base aux implications plus larges
Enfin, les auteurs ont montré que fusionner la queue liant l’héparane du VEGF-A à une protéine de signal non apparentée, Wnt3a, pouvait rediriger l’activité de Wnt : attacher la queue normale réduisait les changements développementaux induits par Wnt, tandis qu’attacher la queue insensible à l’ARN les renforçait. Ensemble, ces expériences soutiennent un modèle dans lequel les amas csRNP, ancrés par un héparane sulfate spécifiquement sulfates, se lient au VEGF-A et à des facteurs apparentés pour tempérer leur activité. Quand la composante ARN est retirée ou quand les facteurs de croissance perdent leur capacité à détecter l’ARN, l’équilibre bascule vers une signalisation plus forte et un développement vasculaire altéré chez plusieurs espèces.
Pourquoi cela compte pour la santé et les thérapies futures
Pour un non-spécialiste, le message clé est que les cellules utilisent non seulement des protéines et des sucres, mais aussi de petits ARN affichés à leur surface pour ajuster précisément des signaux de croissance puissants comme le VEGF-A. Ces amas d’ARN–protéine liés aux sucres agissent comme des freins modulables sur la formation des vaisseaux, aidant à garantir que de nouveaux vaisseaux poussent où et quand il le faut. Perturber cet équilibre — en dégradant l’ARN de surface ou en modifiant les propriétés de liaison à l’ARN des facteurs de croissance — peut soit exagérer soit détourner la croissance vasculaire. Comprendre cette couche de contrôle nouvellement révélée pourrait ouvrir la voie à des thérapies qui moduleraient plus précisément l’angiogenèse dans le cancer, les maladies oculaires, la cicatrisation et la médecine régénérative en ciblant les ARN de surface, leurs échafaudages sucrés ou les régions détectrices d’ARN des facteurs de croissance.
Citation: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Mots-clés: angiogenèse, facteur de croissance endothélial vasculaire, héparane sulfate, ARN à la surface cellulaire, glycoARN