Clear Sky Science · fr
Convergence et divergence développementales dans des modèles de cellules souches humaines de l’autisme
Pourquoi cette recherche compte pour les familles et la société
Le trouble du spectre autistique est notoirement complexe : des centaines de gènes différents ont été associés à un risque accru, pourtant de nombreuses personnes autistes partagent des difficultés similaires de communication, d’interaction sociale et de comportement. Cette étude pose une question apparemment simple mais aux grandes implications : lorsque des altérations génétiques très différentes augmentent la probabilité d’autisme, perturbent-elles finalement le cerveau en développement de la même manière ? En utilisant de petits modèles de cortex humain cultivés en laboratoire à partir des propres cellules des patients, les chercheurs retracent comment des anomalies précoces de l’activité génique peuvent converger vers des voies communes qui modifient la naissance, la maturation et les connexions des cellules cérébrales.
Cultiver un tissu cérébral humain miniature en laboratoire
Pour aborder cette question, l’équipe a collecté des cellules de peau ou du sang auprès de 55 personnes : certaines portaient des mutations rares bien caractérisées fortement associées à l’autisme, d’autres avaient un autisme sans mutation majeure identifiée, et d’autres encore étaient des témoins non affectés. Ces cellules ont été reprogrammées en cellules souches pluripotentes induites, capables de devenir presque n’importe quel type cellulaire. Les scientifiques les ont ensuite orientées pour former des « organoïdes corticaux » tridimensionnels – de petites sphères de tissu qui reproduisent le développement précoce du cortex cérébral humain. Sur 100 jours, ces organoïdes ont évolué d’une population majoritairement composée de progéniteurs de type souche vers des réseaux riches en jeunes neurones. À quatre moments de cette chronologie (jours 25, 50, 75 et 100), l’équipe a mesuré quels gènes étaient activés ou réprimés à travers des centaines d’organoïdes, créant un film détaillé des changements moléculaires au cours du développement cérébral précoce.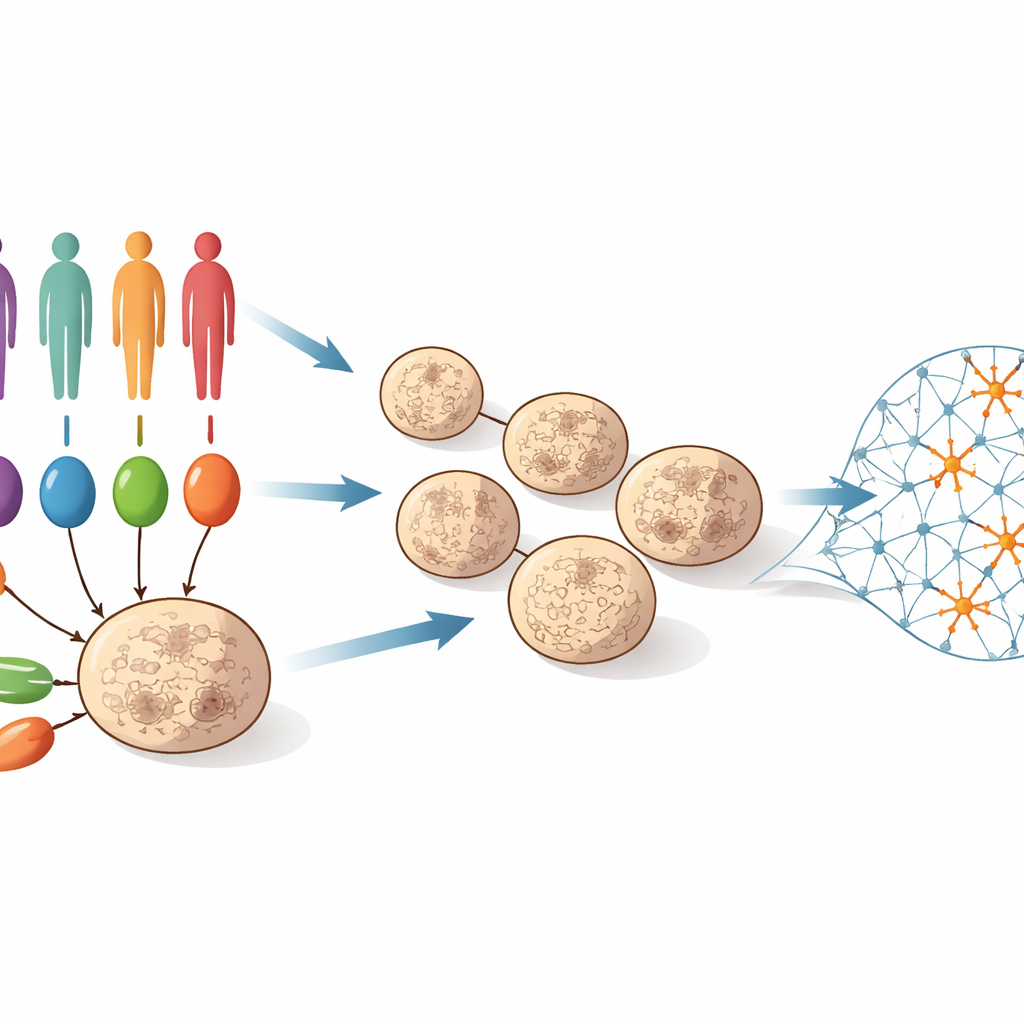
Multiples chemins génétiques, mêmes détours précoces
Bien que les mutations liées à l’autisme soient très différentes – incluant de larges segments d’ADN manquants ou dupliqués et des altérations géniques spécifiques – les organoïdes portant la même mutation présentaient des profils d’activité génique fortement reproductibles. Tôt dans le développement, notamment autour du jour 25, chaque mutation produisait sa propre signature marquée : des centaines à plus d’un millier de gènes étaient déréglés par rapport aux témoins. Pourtant, même à ce stade précoce, plusieurs mutations modifiaient des ensembles de gènes qui se recoupent et qui sont impliqués dans la façon dont l’ADN est empaqueté et lu à l’intérieur des cellules. Ces changements partagés touchaient des gènes déjà connus comme à haut risque pour l’autisme ainsi que d’autres gènes impliqués dans des troubles du neurodéveloppement, ce qui suggère que des mutations différentes commencent très tôt à perturber des machines cellulaires similaires lors de la formation du cerveau.
Convergence à mesure que le modèle cérébral mûrit
À mesure que les organoïdes se développaient vers des neurones plus matures (aux jours 75 et 100), le tableau a évolué. Les différences spécifiques à chaque mutation devenaient moins marquées, tandis que les similarités se renforçaient. Dans presque toutes les formes génétiques d’autisme étudiées, les chercheurs ont observé une activité réduite des gènes importants pour la signalisation électrique aux synapses – les points de communication entre neurones – et une activité accrue des gènes liés à la croissance cellulaire et à la production de protéines. Des variations subtiles dans les proportions et les stades de maturation des différents types cellulaires sont apparues, indiquant des changements dans le calendrier de naissance et de maturation des neurones plutôt qu’une perte massive de populations cellulaires particulières. Au dernier point temporel, des milliers de gènes présentaient un motif commun de dérégulation à travers les différentes mutations rares, même si les mutations elles‑mêmes affectaient des gènes originaux différents.
Un hub de contrôle central reliant de nombreux gènes associés à l’autisme
Approfondissant leur analyse, l’équipe a utilisé des approches en réseau pour regrouper les gènes qui tendent à s’activer et se réprimer ensemble en « modules ». Un module en particulier, nommé M5, s’est démarqué. Ses gènes sont les plus actifs tôt dans le développement et sont fortement enrichis en gènes de risque pour l’autisme, en particulier ceux qui contrôlent la manière dont d’autres gènes sont activés ou réprimés et la façon dont l’ADN est empaqueté. Dans les organoïdes issus de plusieurs groupes de mutations liées à l’autisme, ce module était systématiquement atténué. Les chercheurs ont montré que de nombreuses protéines du module M5 interagissent physiquement, formant un hub régulateur. En utilisant des outils basés sur CRISPR pour réduire sélectivement l’expression de 26 de ces régulateurs M5 dans des progéniteurs neuronaux humains, ils ont confirmé que ce hub contrôle directement de larges ensembles de gènes en aval, incluant de nombreux autres gènes de risque pour l’autisme et le neurodéveloppement, et que sa perturbation peut altérer des voies impliquées dans la formation des neurones et la fonction synaptique.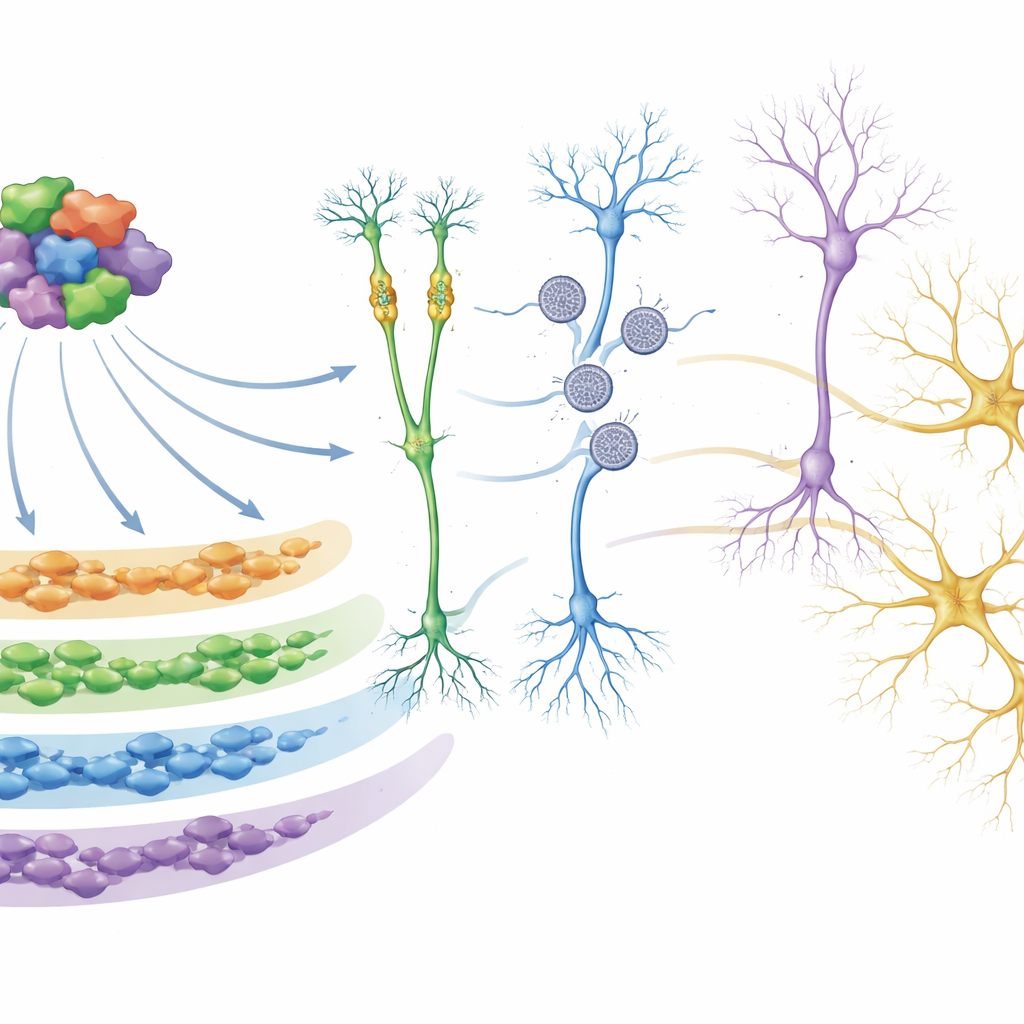
Ce que cela signifie pour la compréhension de l’autisme
Ce travail suggère un tableau unificateur : des mutations rares et puissantes liées à l’autisme commencent par perturber des portions différentes du génome, mais leurs effets se propagent ensuite à travers un réseau de contrôle précoce partagé qui régit la génération et le câblage des neurones corticaux. Avec le temps, ces perturbations convergent vers des résultats communs – retard ou altération de la maturation neuronale et programmes synaptiques perturbés – même si les causes génétiques initiales diffèrent. Pour les familles, cela signifie que des diagnostics très différents au niveau de l’ADN peuvent néanmoins influencer des voies biologiques qui se chevauchent dans le cerveau en développement. Pour les chercheurs et cliniciens, le réseau régulateur identifié offre un ensemble ciblé de cibles moléculaires pour de futures thérapies visant à restaurer des schémas de développement cérébral plus typiques à travers un large éventail de conditions génétiques liées à l’autisme.
Citation: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
Mots-clés: trouble du spectre autistique, organoïdes cérébraux, modèles de cellules souches, régulation des gènes, neurodéveloppement