Clear Sky Science · fr
Le séquençage à l’échelle populationnelle élucide les déterminants de l’ADN persistant du VEB
Pourquoi un virus commun reste important
La plupart des adultes portent le virus Epstein–Barr (VEB), souvent sans même le savoir. Pour certains, cependant, ce passager discret est lié à des maladies allant de la mononucléose à des cancers et des pathologies auto-immunes. Cette étude pose une question simple mais de grande portée : peut-on exploiter les vastes dépôts de données génétiques déjà collectés auprès du public pour déterminer qui présente davantage d’ADN du VEB dans le sang, et si leur patrimoine génétique contribue à expliquer qui contrôle le virus et qui ne le contrôle pas ?
Lire une empreinte virale cachée dans notre ADN
Les biobanques modernes, comme l’UK Biobank et le programme américain All of Us, ont séquencé l’ADN complet de centaines de milliers de volontaires. Ces projets se sont concentrés sur les gènes humains, mais les données brutes contiennent aussi des fragments d’ADN viraux. Les chercheurs ont remarqué que le génome de référence humain utilisé pour l’alignement inclut un « chromosome » supplémentaire pour le VEB. En réexaminant les lectures mappées sur ce segment du VEB, ils ont pu estimer combien de copies du génome du VEB étaient présentes dans le sang de chaque personne au moment du prélèvement. Après avoir soigneusement masqué quelques régions répétitives trompeuses, ils ont défini comme présentant une « ADNémie du VEB » les personnes avec des niveaux clairement détectables—une quantité mesurable d’ADN du VEB en circulation dans le sang.
Une petite minorité porte une charge virale élevée
En analysant près d’un demi-million de personnes dans l’UK Biobank et un quart de million dans All of Us, l’équipe a constaté que la plupart des adultes n’avaient pas d’ADN du VEB détectable dans le sang, bien que plus de 90 % présentent des preuves d’infection passée aux tests sérologiques. Environ 10 % des participants, toutefois, se situaient dans une queue de la distribution avec des taux d’ADN du VEB clairement élevés. Ces individus avaient tendance à être plus âgés, plus souvent des hommes, et étaient légèrement plus susceptibles de prendre des traitements immunosuppresseurs. Des schémas similaires sont apparus dans les deux cohortes, et dans un jeu indépendant d’échantillons de salive le virus était beaucoup plus fréquent, soulignant que le VEB réside dans différents réservoirs de l’organisme et que les mesures sanguines n’en capturent qu’un seul.
Liaisons entre persistance virale et maladie
Avec ce nouveau biomarqueur, les auteurs ont examiné comment la persistance de l’ADN du VEB dans le sang se rapporte à la santé. Ils ont parcouru des milliers de codes de diagnostic et de mesures de laboratoire pour identifier ceux qui étaient plus fréquents chez les personnes présentant une ADNémie du VEB. Des associations fortes sont apparues avec des affections déjà suspectées d’être liées au VEB, notamment le lymphome de Hodgkin, la polyarthrite rhumatoïde, le lupus, la maladie pulmonaire obstructive chronique et certains cancers du poumon. Des signaux ont également été observés pour des problèmes cardiovasculaires, une insuffisance rénale, la dépression et la fatigue, ainsi que des liens suggestifs avec des troubles neurologiques rares tels que l’ophtalmoplégie aiguë/NMO. Beaucoup de ces schémas ont été reproduits dans la cohorte indépendante All of Us. L’étude ne peut pas prouver que le VEB cause ces problèmes, mais elle montre qu’un taux élevé d’ADN du VEB dans le sang est un marqueur de risques sanitaires plus larges et de dysfonctionnement immunitaire.
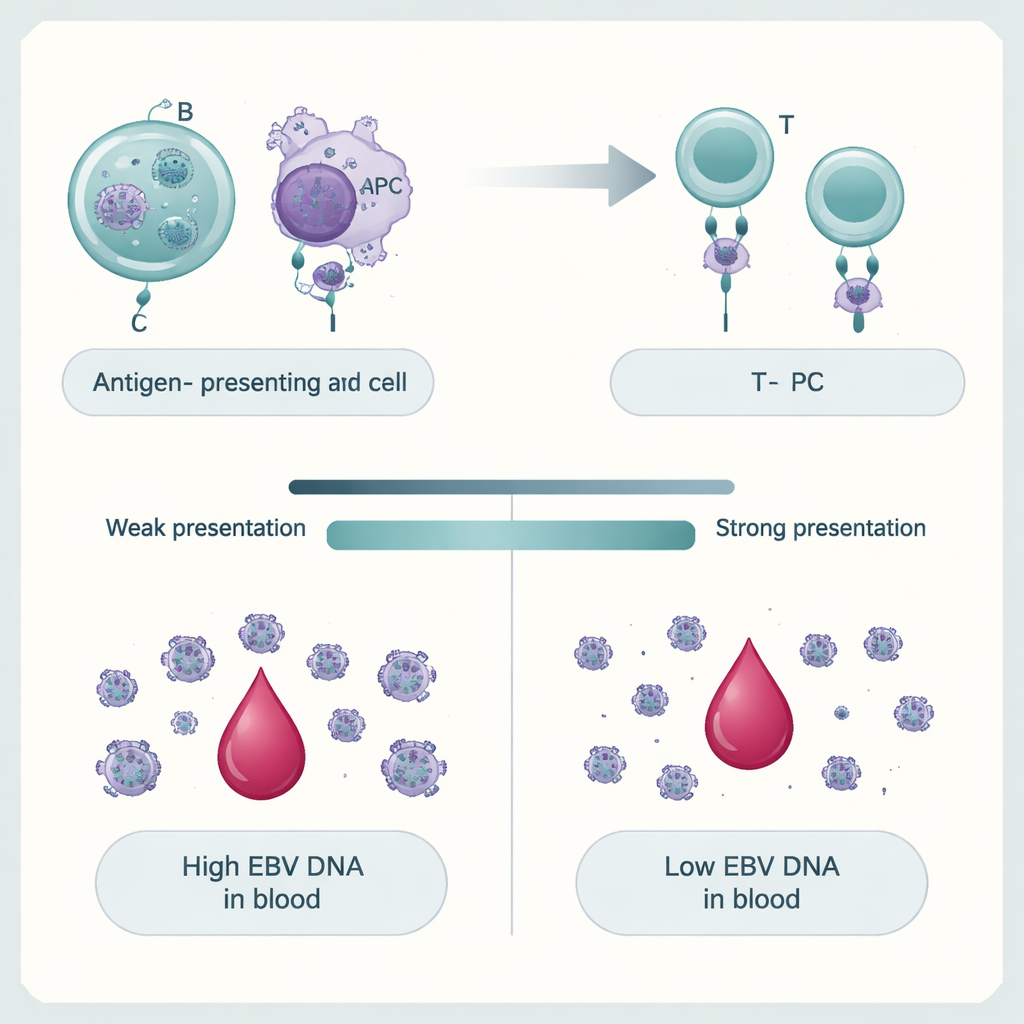
Comment nos gènes influencent le contrôle du virus
L’équipe a ensuite cherché pourquoi seules certaines personnes présentent des niveaux élevés d’ADN du VEB. En analysant des millions de variants génétiques à travers le génome, ils ont montré que l’ADNémie du VEB est un trait polygénique : de nombreuses petites différences d’ADN contribuent ensemble à augmenter ou diminuer les niveaux viraux. Les signaux les plus forts se concentraient dans et autour des gènes du complexe majeur d’histocompatibilité (CMH), qui aident les cellules immunitaires à présenter des fragments viraux aux lymphocytes T. Les variants modifiant ces protéines, en particulier les molécules du CMH de classe II, étaient fortement liés à la persistance de l’ADN du VEB. Les gènes actifs dans les cellules B—le principal site de résidence à long terme du VEB—et dans d’autres cellules présentatrices d’antigènes étaient particulièrement enrichis. En utilisant des modèles informatiques de la façon dont différentes variantes humaines du CMH lient des peptides du protéome du VEB, les auteurs ont trouvé que les versions prévues pour présenter plus fortement des fragments du VEB avaient tendance à protéger contre des niveaux élevés d’ADN du VEB, tandis que les présentatrices plus faibles étaient associées à la persistance.
Ce que cela signifie pour la compréhension de l’infection
Pour un public non spécialiste, le message essentiel est que notre équilibre à long terme avec le VEB n’est pas aléatoire. En exploitant des données de séquençage à l’échelle de la population déjà existantes, l’étude montre que le patrimoine génétique d’une personne—en particulier dans des gènes immunitaires qui exposent des fragments viraux aux lymphocytes T—contribue à déterminer la quantité de VEB qui persiste dans son sang. Des niveaux élevés identifient un sous-groupe de personnes à risque accru pour une gamme d’affections immunitaires, respiratoires et possiblement neurologiques. Ce travail fournit un modèle pour transformer d’anciens jeux de données de séquençage en nouvelles connaissances sur de nombreux virus qui cohabitent avec nous, et suggère que des stratégies ciblées visant à renforcer ou à reproduire une présentation antigénique efficace pourraient un jour aider à mieux contrôler des infections durables comme le VEB.
Citation: Nyeo, S.S., Cumming, E.M., Burren, O.S. et al. Population-scale sequencing resolves determinants of persistent EBV DNA. Nature 650, 664–672 (2026). https://doi.org/10.1038/s41586-025-10020-2
Mots-clés: Virus Epstein–Barr, persistance virale, génétique humaine, maladie auto-immune, séquençage de biobanques