Clear Sky Science · fr
Des vaccins ARNm individualisés suscitent une immunité T durable en adjuvant du cancer du sein TNBC
Un nouvel espoir après le traitement du cancer du sein
Pour de nombreuses femmes atteintes d’une forme agressive de cancer du sein appelée cancer du sein triple négatif, la peur ne s’efface pas lorsque la chimiothérapie et la chirurgie sont terminées. Ce cancer présente un risque élevé de récidive et de métastases, souvent au cours des quelques années qui suivent. L’étude décrite ici évalue un vaccin hautement personnalisé, construit à partir des mutations propres à la tumeur de chaque patiente, pour déterminer s’il peut entraîner le système immunitaire à assurer une surveillance pendant des années et réduire le risque de rechute après la fin du traitement standard.
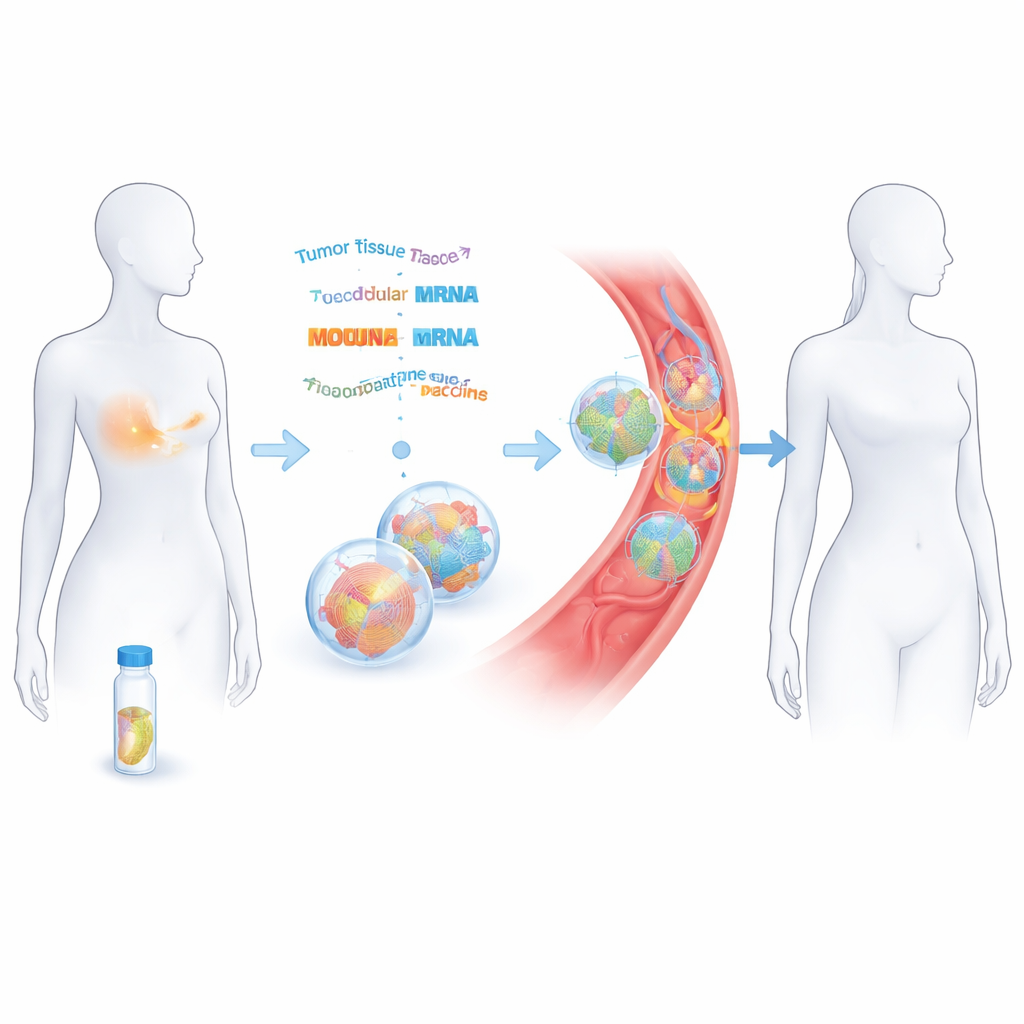
Transformer une tumeur retirée en vaccin sur mesure
Les chercheurs ont travaillé avec 14 femmes atteintes d’un cancer du sein triple négatif au stade précoce, ayant déjà bénéficié d’une chirurgie et d’une chimiothérapie à visée curative. À partir du tissu tumoral prélevé, ils ont séquencé l’ADN et l’ARN pour dresser l’inventaire des mutations propres au cancer. À l’aide d’outils informatiques, ils ont prédit lesquelles de ces altérations pourraient être perçues comme étrangères par les cellules immunitaires. Jusqu’à 20 de ces « néoantigènes » ont ensuite été réunis et encodés dans deux brins d’acide ribonucléique messager (ARNm), sur le même principe que les vaccins contre la COVID‑19 mais adaptés à chaque patiente. Ces brins d’ARNm ont été encapsulés dans de minuscules bulles lipidiques et administrés par voie intraveineuse en huit doses sur environ deux mois.
Comment le vaccin mobilise les défenseurs immunitaires
Une fois dans l’organisme, l’ARNm indique aux sentinelles immunitaires appelées cellules dendritiques de produire brièvement les protéines néoantigènes et d’exposer des fragments de celles‑ci à leur surface. Cela agit comme un portrait‑robot pour les cellules T, la principale force immunitaire chargée d’éliminer les cellules cancéreuses. L’équipe a prélevé du sang avant la vaccination et à plusieurs moments après celle‑ci pour vérifier l’apparition et l’intensité des cellules T spécifiques aux néoantigènes. À l’aide d’essais de laboratoire sensibles, ils ont constaté que chaque patiente développait des réponses de cellules T nouvelles ou renforcées contre au moins une des mutations sélectionnées, et la plupart répondaient à plusieurs. Dans de nombreux cas, des fractions importantes des cellules T circulantes — des niveaux habituellement observés seulement avec des thérapies cellulaires puissantes — étaient désormais orientées pour reconnaître des cibles spécifiques à la tumeur.
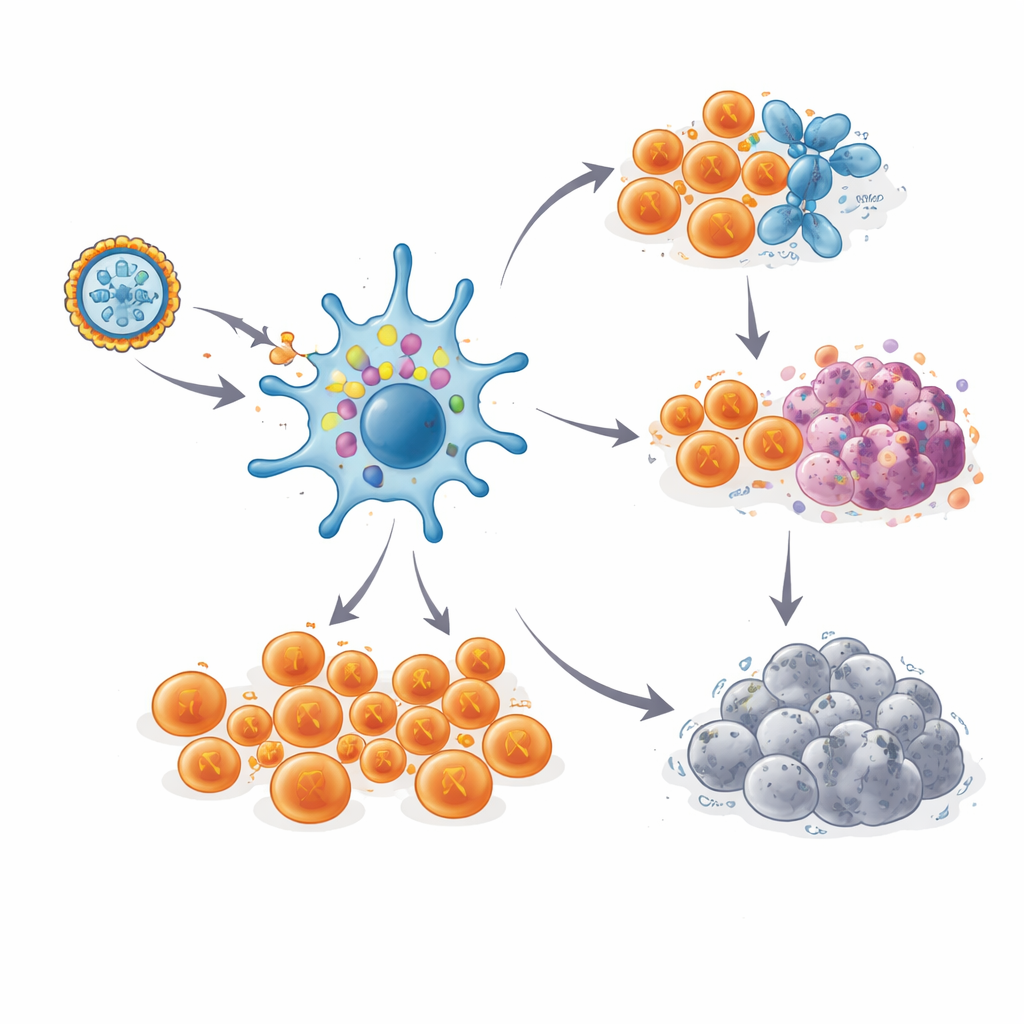
Mémoire immunitaire durable
Fait important, ces réponses des cellules T ne se sont pas estompées rapidement. Chez la plupart des patientes, les réponses robustes ont culminé pendant la période de vaccination, ont légèrement diminué, puis sont restées à des niveaux élevés pendant un à trois ans et demi, même sans rappels. En suivant les « codes-barres » uniques des récepteurs de clones cellulaires T individuels, les scientifiques ont pu suivre des cellules réactives aux néoantigènes spécifiques pendant jusqu’à six ans chez une patiente qui est restée sans cancer. Des analyses détaillées à l’échelle d’une seule cellule ont montré deux destinées principales pour ces cellules. Beaucoup sont devenues des cellules T tueuses hautement armées, prêtes à détruire toute cellule portant le néoantigène approprié. D’autres ont évolué vers un pool mémoire plus rare, de type souches, avec des marqueurs d’auto‑renouvellement, suggérant un réservoir capable de régénérer de nouvelles vagues de combattantes si des cellules cancéreuses réapparaissaient.
Ce qu’il est advenu des patientes
Après un suivi médian d’un peu plus de cinq ans depuis la première dose de vaccin, onze des quatorze femmes n’avaient pas présenté de récidive de leur cancer ; l’une d’elles est décédée pour des causes non liées alors qu’elle était toujours en rémission. Trois femmes ont rechuté, et leurs cas fournissent des indices sur les raisons pour lesquelles un vaccin personnalisé peut parfois échouer. Une patiente n’a montré qu’une faible réponse en cellules T et a ensuite bénéficié d’un autre médicament d’immunothérapie, un anticorps anti‑PD‑1, avant de succomber finalement à une maladie étendue. Une deuxième patiente avait un risque héréditaire et des tumeurs dans les deux seins ; une seule tumeur a été utilisée pour concevoir le vaccin, et des preuves ultérieures ont montré que la récidive provenait de la tumeur génétiquement distincte, non vaccinée. La troisième patiente avait des cellules T induites par le vaccin qui infiltraient la tumeur récidivante, mais les cellules cancéreuses avaient en grande partie perdu des molécules essentielles pour présenter les néoantigènes à leur surface, se cachant ainsi de l’attaque immunitaire.
Pourquoi ce travail importe pour l’avenir
Cette étude de phase précoce était de petite taille et sans groupe témoin, elle ne peut donc pas prouver que le vaccin seul a empêché les rechutes. Néanmoins, elle montre qu’il est faisable, en milieu hospitalier courant, de fabriquer un vaccin ARNm complexe et personnalisé à partir de la tumeur d’une patiente, qu’il est généralement bien toléré et qu’il peut déclencher des armées de cellules T puissantes et durables contre plusieurs cibles spécifiques au cancer. Les résultats soulignent également les voies d’échappement que les tumeurs peuvent emprunter, comme la perte de leur machinerie de présentation d’antigènes ou l’apparition à partir de lésions non ciblées, ce qui oriente vers des associations avec d’autres immunothérapies et un séquençage tumoral plus étendu. Pour les patientes confrontées au cancer du sein triple négatif, ce travail suggère qu’un vaccin sur mesure, administré après le traitement standard, pourrait un jour aider à prévenir la réapparition de la maladie en transformant leur propre système immunitaire en une ligne de défense durable et hautement spécifique.
Citation: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Mots-clés: cancer du sein triple négatif, vaccins anticancéreux à ARNm, immunothérapie par néoantigènes, immunité des cellules T, récurrence tumorale