Clear Sky Science · fr
La protection métabolique dépendante des polyamines régule l’épissage alternatif
Comment de Minuscules Molécules Aident les Cellules à Lire Leurs Gènes
À l’intérieur de chaque cellule, un même script d’ADN peut être lu de multiples façons, permettant à un nombre limité de gènes de produire une grande variété de protéines. Cette flexibilité repose sur un processus nommé épissage alternatif, qui édite les messages ARN avant leur traduction en protéines. Cet article révèle que de petites molécules chargées positivement, appelées polyamines, orientent discrètement cette étape d’édition, agissant comme une sorte de bouclier protecteur qui aide la cellule à décider quelles versions d’ARN produire. Parce que l’épissage alternatif est crucial dans le cancer, la fonction cérébrale et les cellules souches, la découverte de ce niveau de contrôle caché a des implications étendues pour la santé et la maladie.
Petits Aides Chargés Présents dans Chaque Cellule
Les polyamines sont de minuscules molécules flexibles portant plusieurs charges positives. Les cellules les synthétisent à partir de nutriments de base, et on les connaît depuis longtemps comme des soutiens de la croissance et de la survie, en particulier dans les cellules à division rapide comme les tumeurs. Les auteurs ont cherché à savoir si les polyamines servent aussi de signaux, et pas seulement de carburant. En bloquant partiellement la production de polyamines dans des cellules de cancer de la prostate et chez la souris, ils ont mesuré comment les protéines et l’ARN changeaient au fil du temps. Ils ont constaté que bien avant que les niveaux totaux de polyamines ne chutent de façon spectaculaire, une forte vague de modifications de phosphorylation des protéines — des étiquettes chimiques qui activent ou désactivent des interrupteurs protéiques — survenait, en particulier sur des composants de la machinerie d’édition de l’ARN, le spliceosome.
Reconfigurer l’Éditeur d’ARN de la Cellule
En se concentrant spécifiquement sur l’ARN, l’équipe a utilisé le séquençage profond pour suivre l’épissage alternatif lorsque la synthèse des polyamines était inhibée. Des centaines de segments d’ARN étaient exclus ou inclus différemment, dans des lignées cancéreuses, des types cellulaires normaux et des tissus de souris. Ces changements n’étaient pas simplement un effet secondaire d’un ralentissement de la division cellulaire ni d’un autre processus dépendant des polyamines appelé hypusinylation. Au contraire, lorsque les chercheurs réapprovisionnaient les cellules en polyamines exogènes, de nombreux changements d’épissage revenaient vers la normale. Tant des médicaments que des outils génétiques réduisant les polyamines produisaient des profils d’épissage similaires, et une réduction supplémentaire des polyamines par une combinaison médicamenteuse accentuait encore les modifications, confirmant que l’effet était étroitement lié à la disponibilité des polyamines.
Une Cible Cachée : le Module SF3 de l’Épissage
Pour localiser où, dans la machinerie d’épissage, les polyamines agissent, les auteurs ont comparé la signature d’épissage induite par la baisse des polyamines à une large carte de référence générée en silencant individuellement plus de 300 facteurs d’épissage connus. La correspondance la plus proche pointait vers une partie spécifique du spliceosome appelée le sous-complexe SF3, qui aide à reconnaître des signaux clés dans l’ARN. L’analyse computationnelle de données publiques de liaison protéine–ARN soutenait ce lien : les ARN dont l’épissage était altéré par la perte de polyamines étaient particulièrement susceptibles d’être liés par des protéines SF3. Lorsque l’équipe a partiellement désactivé génétiquement des composants de SF3 ou utilisé un médicament ciblant SF3, les effets d’épissage de l’appauvrissement en polyamines ont été en grande partie effacés, montrant que l’activité intacte de SF3 est requise pour cette nouvelle voie de régulation. 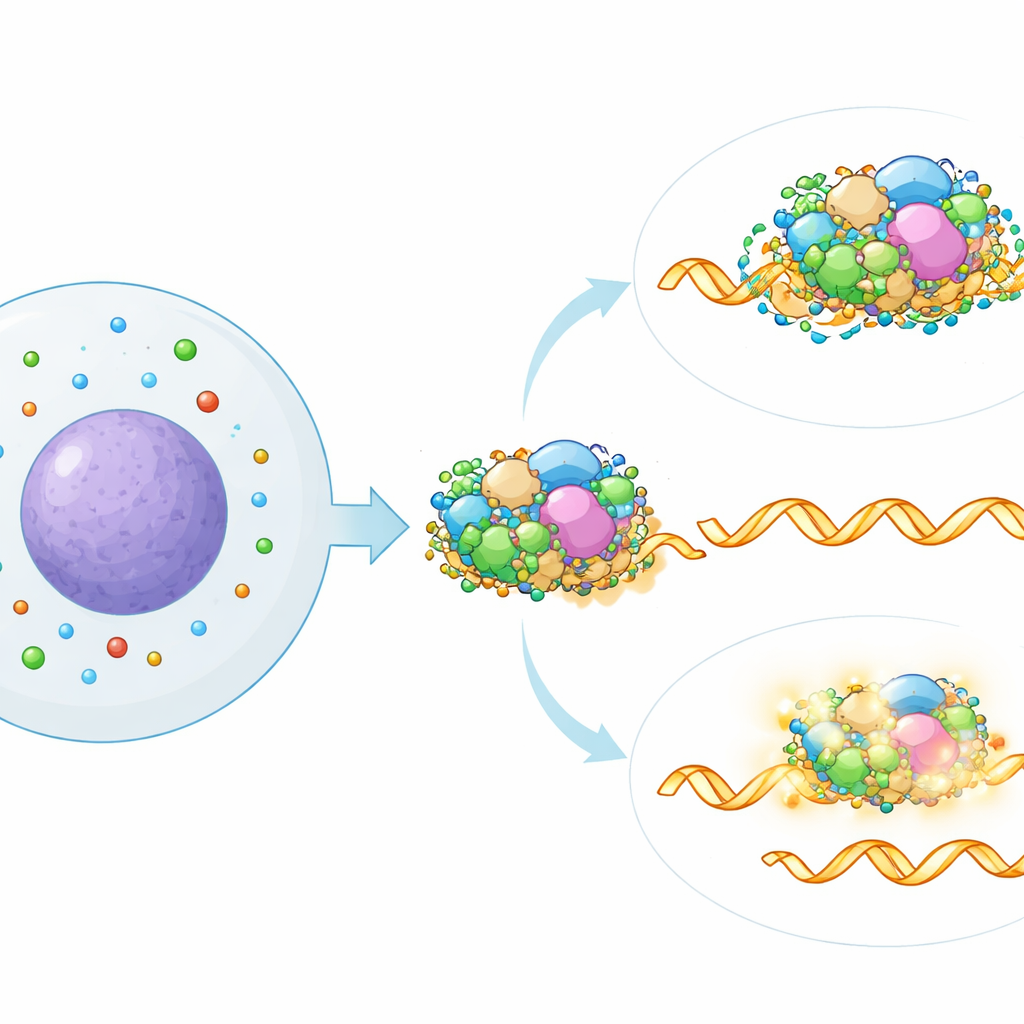
Protection Métabolique : Comment les Polyamines Bloquent les Marquages Protéiques
En approfondissant, les chercheurs ont remarqué que les sites de phosphorylation les plus fortement affectés sur les protéines SF3 se regroupaient dans de courts segments riches en acides aminés chargés négativement. La modélisation moléculaire et des expériences de résonance magnétique nucléaire ont montré que les polyamines se logent dans ces zones acides, formant de multiples contacts électrostatiques et couvrant partiellement des résidus de sérine voisins où les groupes phosphate sont habituellement ajoutés. Cette « étreinte » physique réduit l’accessibilité de ces sites aux kinases protéiques — les enzymes qui attachent les phosphates. Dans des expériences in vitro, l’ajout de polyamines bloquait directement une kinase nommée CK1 de phosphoryler les protéines SF3. In vivo, l’inhibition de CK1 et de sa proche parente CK2 atténuait les changements d’épissage causés par la perte de polyamines, et des souris génétiquement modifiées dont la protéine SF3A3 manquait trois sites clés de phosphorylation devenaient en grande partie insensibles aux variations d’épissage dépendantes des polyamines. 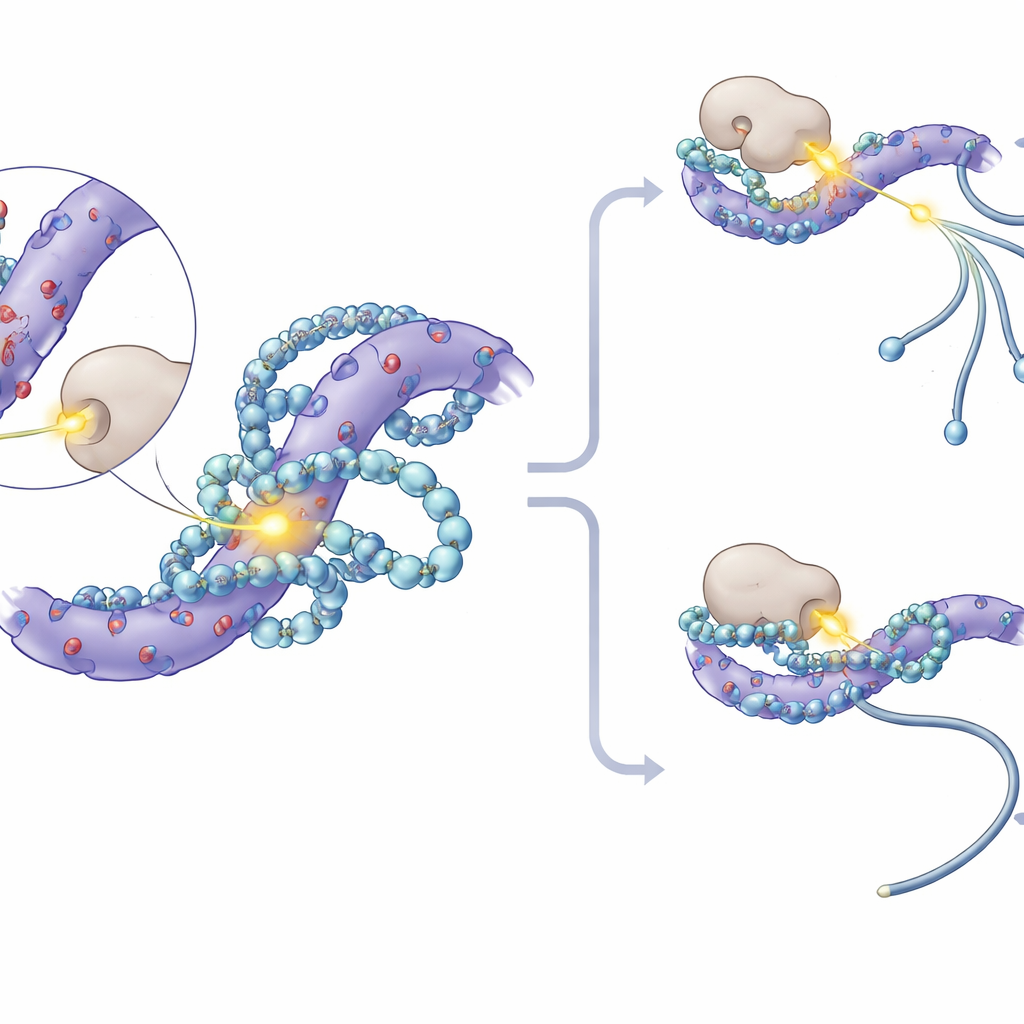
Une Molécule Conçue qui Sépare les Rôles
L’étude présente aussi un médicament de type polyamine, BENSpm, qui porte une charge positive plus forte tout en arrêtant simultanément la production cellulaire de polyamines. BENSpm se liait fortement aux zones acides de SF3 et bloquait l’action des kinases, tout comme les polyamines naturelles, mais il ne sauvait pas la croissance cellulaire lorsque les polyamines réelles faisaient défaut. Cela a permis aux auteurs de dissocier les fonctions classiques des polyamines (soutenir la croissance et le métabolisme) du rôle de protection nouvellement défini. Dans des cellules souches embryonnaires de souris, l’épuisement des polyamines poussait les cellules à perdre leur marqueur de « stemness » Nanog et modifiait leur paysage d’épissage. BENSpm rétablit à la fois le profil d’épissage et l’expression de Nanog malgré la suppression continue de la synthèse normale des polyamines, indiquant que la protection métabolique est une exigence clé pour le maintien de l’identité des cellules souches.
Pourquoi Cette Découverte Compte
En termes simples, ce travail montre que les polyamines agissent comme de minuscules gants protecteurs autour de parties sensibles de protéines d’épissage essentielles. Lorsque les gants sont en place, les kinases ne peuvent pas facilement saisir et taguer ces sites, et l’édition de l’ARN par la cellule demeure sur sa trajectoire. Lorsque les polyamines sont faibles, les gants tombent, la phosphorylation augmente et les schémas d’épissage changent, avec des conséquences pour les cellules cancéreuses et les cellules souches. En définissant ce mécanisme de « protection métabolique » et en fournissant une molécule-outil qui le mime sélectivement, l’étude ouvre la voie à de nouvelles façons d’ajuster la lecture des gènes sans modifier l’ADN lui‑même, ce qui pourrait inspirer des thérapies futures ciblant l’épissage en oncologie et en médecine régénérative.
Citation: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Mots-clés: polyamines, épissage alternatif, traitement de l’ARN, signalisation métabolique, régulation des cellules souches