Clear Sky Science · fr
La variation courante dans les gènes de la méiose façonne la recombinaison humaine et l’aneuploïdie
Pourquoi les erreurs chromosomiques des embryons comptent
De nombreuses grossesses se terminent avant même d’être reconnues, souvent parce qu’un embryon porte un nombre incorrect de chromosomes. Cette étude pose une question apparemment simple mais aux conséquences profondes pour la fertilité et la santé reproductive : comment des différences d’ADN ordinaires entre individus modulent-elles la façon dont les ovules et les spermatozoïdes recombinent et séparent les chromosomes, et comment cela influe-t-il sur la probabilité qu’un embryon ait trop ou pas assez de chromosomes ? En examinant plus d’une centaine de milliers d’embryons issus de fécondation in vitro (FIV), les auteurs montrent comment des variations génétiques courantes dans une poignée de gènes peuvent légèrement incliner les probabilités en faveur ou contre ces erreurs chromosomiques.
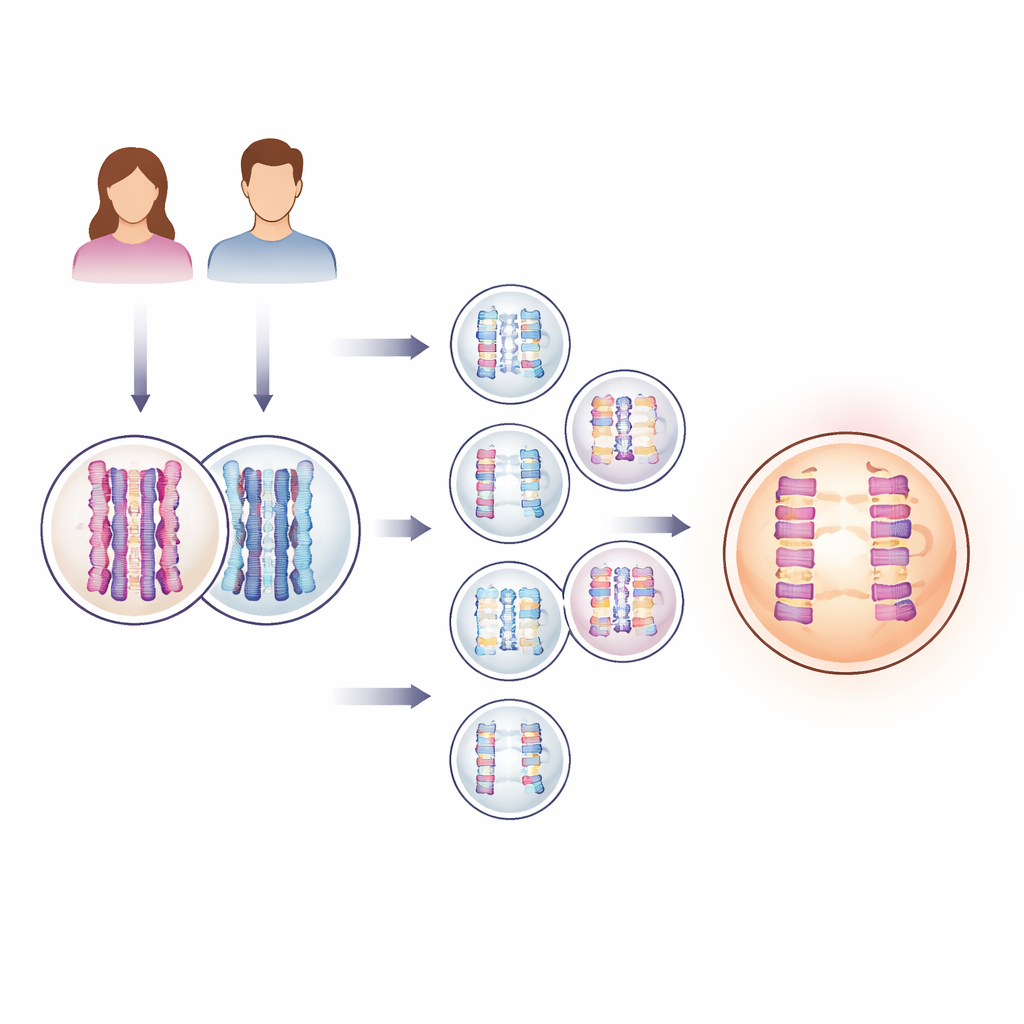
Plonger dans des milliers d’embryons de FIV
Pour étudier un phénomène qui se déroule généralement de façon invisible à l’intérieur du corps humain, les chercheurs ont utilisé des données de tests génétiques recueillies de manière routinière lors de FIV. Les cliniques prélèvent souvent quelques cellules d’un embryon quelques jours après la fécondation pour vérifier la présence de problèmes chromosomiques avant le transfert. Ici, l’équipe a analysé l’ADN de 139 416 embryons de ce type, ainsi que l’ADN de près de 23 000 paires de parents biologiques. Grâce à une méthode statistique qui suit des blocs d’ADN parentaux transmis aux embryons, ils ont pu à la fois compter les « croisements » — les points où les chromosomes parentaux échangent des segments — et détecter quand un embryon avait gagné ou perdu un chromosome entier, une condition appelée aneuploïdie.
À quelle fréquence surviennent les erreurs chromosomiques et qu’est-ce qui les façonne ?
Le relevé a montré qu’un peu moins de 30 % des embryons portaient au moins un chromosome aneuploïde. La plupart de ces erreurs provenaient de la mère plutôt que du père et impliquaient souvent des chromosomes déjà connus pour être plus sujets aux problèmes. Comme l’expérience clinique le prédit, la proportion d’embryons présentant des erreurs chromosomiques maternelles augmentait fortement avec l’âge maternel, tandis que l’âge paternel avait peu d’effet. De façon cruciale, lorsque l’équipe a comparé les embryons au caryotype normal à ceux porteurs d’erreurs, ils ont constaté que les embryons sujets aux erreurs avaient tendance à présenter moins de croisements sur leurs autres chromosomes normaux. Cela étaye l’idée selon laquelle les croisements remplissent une double fonction : ils génèrent de nouvelles combinaisons génétiques, mais jouent aussi le rôle d’attaches physiques qui aident les chromosomes à se séparer proprement lors de la formation des ovules.
Des différences génétiques courantes dans des gènes clés ont de l’importance
Les auteurs ont ensuite cherché dans les génomes maternels des variants d’ADN courants qui corrélaient avec la fréquence d’aneuploïdie chez leurs embryons. Une région remarquée se situait près d’un gène appelé SMC1B, qui code pour une partie d’un complexe protéique en forme d’anneau maintenant les chromatides sœurs ensemble dans les ovules. Les femmes porteuses d’une version particulière de cette séquence d’ADN présentaient une fraction légèrement plus élevée d’embryons avec des erreurs chromosomiques maternelles, et ce risque augmentait avec l’âge. Des analyses complémentaires sur de larges jeux de données d’expression génique ont montré que la version à risque de la séquence est associée à une activité réduite de SMC1B, apparemment via des modifications subtiles de la liaison d’un facteur de transcription à son promoteur. Autrement dit, un ajustement courant et non délétère d’un élément régulateur peut diminuer suffisamment une protéine de cohésion pour accroître de manière mesurable la probabilité d’une mauvaise ségrégation chromosomique.
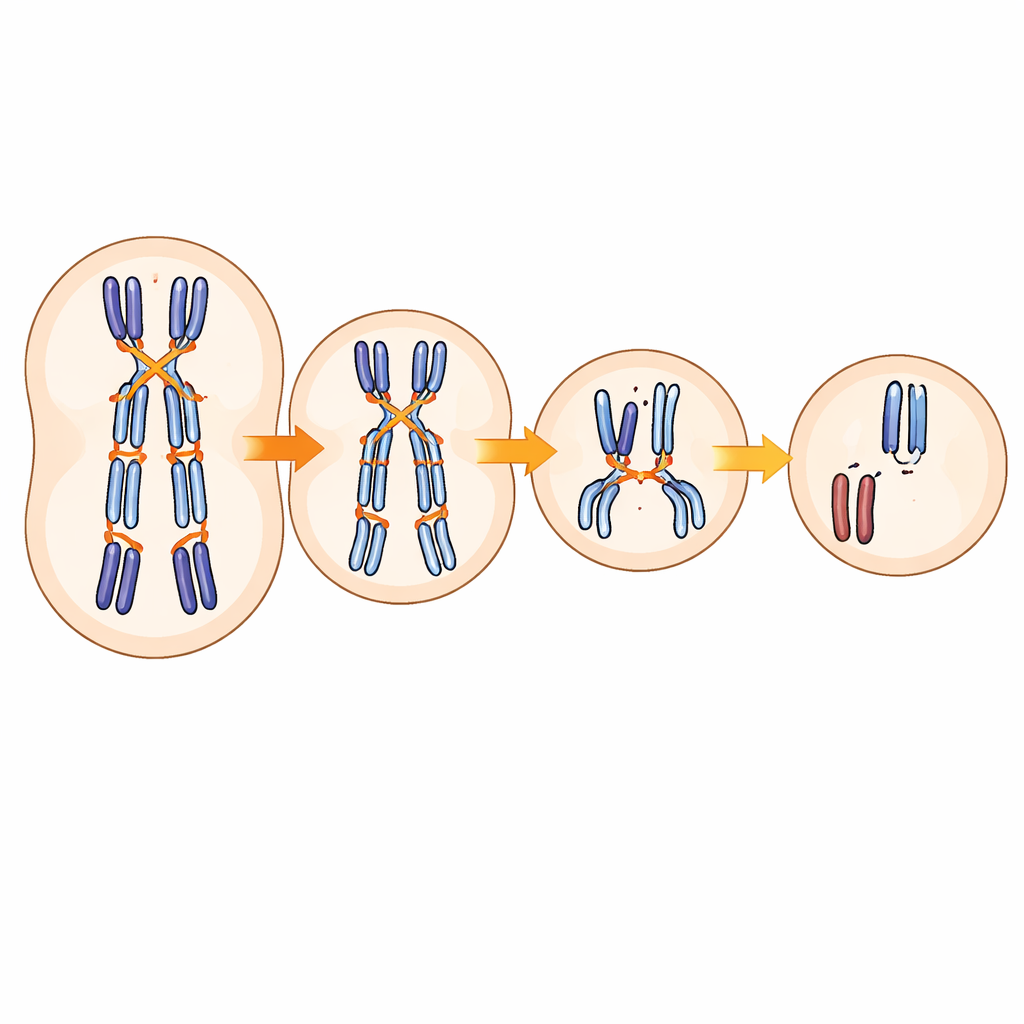
Un fil génétique commun à travers les traits liés à la fertilité
Au-delà de SMC1B, l’étude a mis en lumière d’autres gènes qui aident à aligner et relier les chromosomes pendant la méiose, y compris des composants de l’échafaudage qui rapproche les chromosomes appariés et des enzymes qui marquent les sites de croisements. Les variants de ces gènes ont non seulement influencé les schémas de recombinaison et le risque d’aneuploïdie chez les embryons, mais ont aussi montré des liens avec le moment de la puberté et de la ménopause dans de larges études de population. Pourtant, ensemble, les variants courants n’expliquent qu’une petite partie de la variation globale des erreurs chromosomiques embryonnaires. Cela suggère que l’environnement, des événements aléatoires pendant le développement de l’ovule et des changements génétiques plus rares jouent probablement des rôles importants, même si beaucoup de ces influences convergent vers les mêmes machines moléculaires.
Ce que cela signifie pour la fertilité humaine et l’évolution
Pour un public non spécialiste, le message clé est que les mêmes processus génétiques qui créent une diversité saine dans notre ADN peuvent, lorsqu’ils sont réglés différemment de façon subtile, augmenter le risque de perte précoce de grossesse. Ce travail montre que des différences héréditaires ordinaires dans quelques gènes méiotique peuvent doucement déplacer l’équilibre, surtout avec l’âge des femmes, mais aucun variant unique ne scelle le destin reproductif de quelqu’un. En combinant d’énormes jeux de données d’embryons avec la génétique des populations, l’étude aborde aussi un puzzle évolutif : pourquoi des variants qui accroissent le risque d’embryons non viables restent-ils fréquents chez les humains ? Les auteurs suggèrent que, parce que de nombreux facteurs sociaux et environnementaux estompent le lien entre le nombre d’embryons et la taille réelle des familles, la sélection naturelle peut ne pas éliminer efficacement de tels variants. Ensemble, ces observations approfondissent notre compréhension des raisons pour lesquelles les erreurs chromosomiques sont si fréquentes dans la reproduction humaine et indiquent des voies biologiques qui pourraient, à terme, éclairer le conseil ou des interventions.
Citation: Carioscia, S.A., Biddanda, A., Starostik, M.R. et al. Common variation in meiosis genes shapes human recombination and aneuploidy. Nature 651, 146–153 (2026). https://doi.org/10.1038/s41586-025-09964-2
Mots-clés: aneuploïdie, méiose, fertilité humaine, recombinaison chromosomique, SMC1B