Clear Sky Science · fr
Le stress contrôle l’héritage de l’hétérochromatine via l’ubiquitylation de l’histone H3
Comment les cellules se souviennent du stress
Nos cellules ont besoin de mécanismes pour « se souvenir » de stress passés — comme la chaleur, la privation de nutriments ou l’exposition à des médicaments — afin de réagir plus rapidement la fois suivante. Un système de mémoire puissant repose sur l’hétérochromatine, de l’ADN fortement compacté qui maintient certains gènes éteints pendant de nombreuses divisions cellulaires. Cet article explore comment les cellules ajustent activement cette mémoire en réponse au stress, révélant un centre moléculaire qui relie les signaux environnementaux à des changements durables de l’activité des gènes. Comprendre ce système de contrôle pourrait aider à expliquer comment les champignons développent une résistance aux médicaments et comment le stress reconfigure le paysage épigénétique de nos propres cellules.
Une serrure sur le génome
On peut voir l’hétérochromatine comme une serrure moléculaire appliquée à des segments d’ADN, maintenant silencieux les gènes situés à proximité. Cette serrure se construit à partir de marques chimiques sur les histones, en particulier une marque appelée H3K9me3. Une fois établie, elle peut se recopier à chaque réplication de l’ADN, permettant à des schémas de répression génique d’être hérités sans modifier la séquence d’ADN sous-jacente. Jusqu’ici, la plupart des travaux suggéraient que cette auto‑copie reposait principalement sur une boucle de rétroaction « lire–écrire » : un complexe enzymatique reconnaît les marques H3K9me3 existantes et ajoute la même marque aux histones voisines, étendant progressivement le domaine silencieux. Mais ce modèle n’expliquait pas entièrement comment les conditions environnementales accélèrent, ralentissent ou réorientent la propagation de l’hétérochromatine.
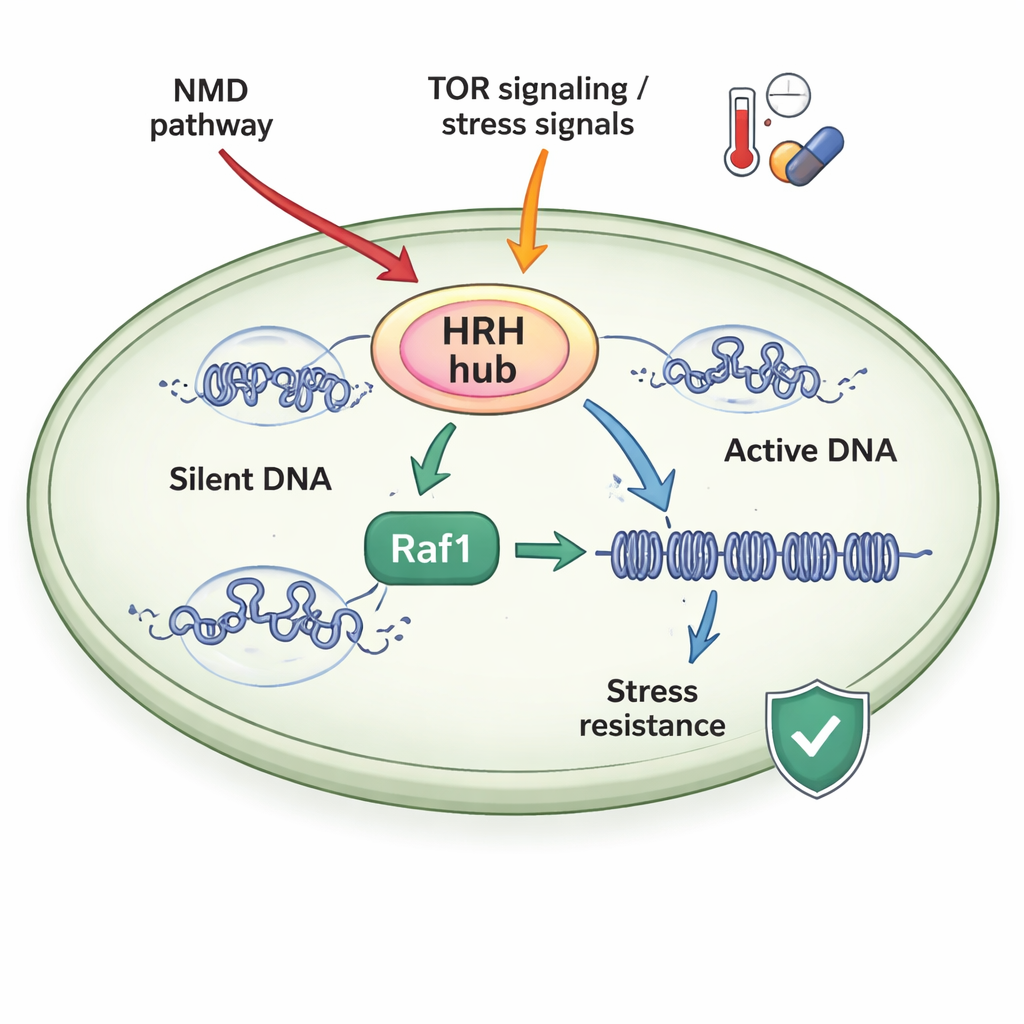
Un centre de contrôle sensible au stress
Les auteurs ont étudié la levure de fission, un organisme modèle simple dont la machinerie de la chromatine ressemble étroitement à celle des organismes supérieurs. Ils se sont intéressés à un complexe appelé ClrC, qui écrit la marque H3K9me3 et attache aussi une petite protéine, l’ubiquitine, à une autre position sur l’histone H3 (H3K14ub). Une sous‑unité clé de ClrC, Raf1, agit comme un « portier » limitant : lorsque Raf1 est rare, une grande partie de l’enzyme principale (Clr4) reste libre au lieu de s’assembler en complexe sur la chromatine, et les domaines silencieux ne parviennent pas à se propager. Quand Raf1 est abondant, davantage de ClrC se forme et se fixe de manière stable à l’ADN, permettant aux marques H3K14ub et H3K9me3 de s’étendre le long des chromosomes et de renforcer l’extinction des gènes.
Affiner la serrure avec l’ubiquitine
En cartographiant les marques de chromatine à l’échelle du génome, l’équipe a montré que H3K14ub est fortement enrichie là où se forme l’hétérochromatine et que cette marque disparaît pratiquement si Raf1 est supprimé. Lorsque les cellules portent une mutation qui bloque l’étape d’ajout d’ubiquitine (tout en laissant H3K9me3 intact au point de départ), les domaines silencieux n’arrivent pas à se propager vers l’extérieur. Autrement dit, H3K14ub n’est pas purement décorative ; elle est nécessaire pour pousser l’avant de l’hétérochromatine en avant. Des expériences biochimiques et d’imagerie expliquent pourquoi : H3K14ub stimule fortement l’activité de l’enzyme Clr4 et aide à maintenir l’ensemble du complexe ancré sur la chromatine, augmentant la densité locale de H3K9me3 au‑dessus du seuil requis pour un héritage stable. Fait remarquable, l’augmentation des niveaux de Raf1 peut compenser plusieurs autres facteurs normalement nécessaires pour maintenir ces domaines silencieux, soulignant que l’ubiquitylation pilotée par Raf1 est un levier de contrôle central.
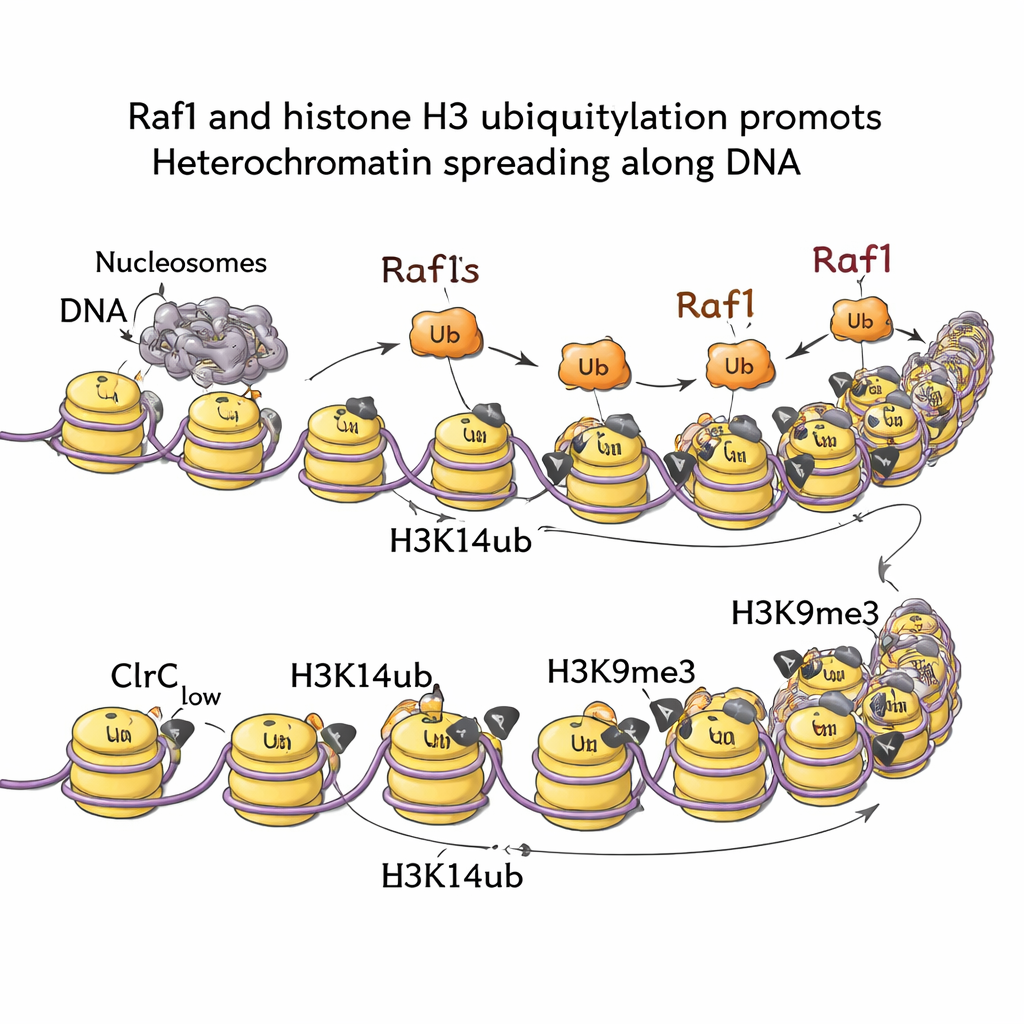
Des signaux issus de la dégradation de l’ARN et des voies de croissance
Les cellules ne laissent pas les niveaux de Raf1 au hasard. L’étude montre que deux grands systèmes sensibles au stress convergent vers ce que les auteurs appellent un hub régulateur de l’héritabilité de l’hétérochromatine (HRH), centré sur Raf1. D’une part, la voie de dégradation des ARNm contenant des codons prématurés — le nonsense‑mediated decay (NMD) —, connue pour détruire les ARNm défectueux, cible l’ARN messager codant Raf1, maintenant les niveaux de Raf1 bas en conditions normales. Inactiver la NMD stabilise l’ARN de Raf1, augmente l’abondance de la protéine Raf1 et restaure la propagation de l’hétérochromatine chez des mutants qui autrement ne peuvent pas maintenir les domaines silencieux. D’autre part, un capteur de croissance et de stress appelé TORC2, agissant via la kinase Gad8, favorise l’expression de Raf1. Les hautes températures inhibent cette voie, abaissant les niveaux de Raf1, affaiblissant l’hétérochromatine et rendant plus difficile pour les cellules le maintien des états silencieux, sauf si Raf1 est augmenté expérimentalement.
Stress, résistance aux médicaments et implications plus larges
Les auteurs relient ensuite ce hub moléculaire à l’adaptation en situation réelle. Exposer la levure à la caféine, un stress qui est aussi connu pour atténuer la NMD dans d’autres systèmes, augmente les niveaux de Raf1 et favorise l’extension de l’hétérochromatine vers de nouveaux sites, y compris des gènes dont l’extinction confère une résistance à la caféine et aux antifongiques. De même, les cellules dont Raf1 est artificiellement élevé deviennent plus résistantes au fluconazole et au clotrimazole, antifongiques courants. À l’inverse, lorsque Raf1 est réduit — par la chaleur ou par la perte du signal TORC2–Gad8 — l’hétérochromatine devient instable et la mémoire épigénétique s’estompe, sauf si Raf1 est rétabli. Parce que des protéines similaires à Raf1, le complexe ClrC et la marque H3K14ub ont des homologues chez les champignons pathogènes et chez les mammifères, ces résultats suggèrent qu’un hub épigénétique sensible au stress similaire pourrait façonner la résistance aux médicaments, le développement et la maladie dans de nombreuses espèces.
Pourquoi c’est important
En termes concrets, ce travail montre que l’extinction génique par la chromatine n’est pas une serrure rigide mais un système intelligent et ajustable. Les cellules utilisent un hub central pour lire les signaux environnementaux — variations de température, statut nutritif, contraintes chimiques — et ajuster l’expression de Raf1 à la hausse ou à la baisse. Cela gouverne à quel point le génome est enveloppé dans un silence durable et à quelle vitesse les cellules peuvent se « reprogrammer » sans muter leur ADN. En révélant le rôle clé de l’ubiquitylation de l’histone H3 et du dosage de Raf1 dans ce processus, l’étude fournit une feuille de route expliquant comment le stress peut remodeler rapidement le paysage épigénétique — et suggère de nouvelles voies pour influencer la résistance aux médicaments chez les champignons ou l’extinction génique aberrante dans les maladies humaines.
Citation: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Mots-clés: hétérochromatine, héritage épigénétique, ubiquitination des histones, adaptation au stress, résistance fongique aux médicaments