Clear Sky Science · fr
Résolution de l’intégrité structurelle et de la pharmacocinétique des origamis d’ADN in vivo
Observer de minuscules machines d’ADN à l’intérieur du corps
L’ADN peut être plié comme du papier pour former de petites structures tridimensionnelles, une technique appelée origami d’ADN. Ces nanostructures peuvent être programmées pour transporter des médicaments, des vaccins ou des molécules de signalisation avec une précision exceptionnelle. Mais une fois injectées dans l’organisme, restent-elles intactes suffisamment longtemps pour agir, ou se décomposent-elles rapidement ? Cet article présente une nouvelle méthode pour observer ces machines d’ADN en action chez des animaux vivants, révélant combien de temps elles survivent, comment elles circulent dans le sang et même quelles parties de chaque structure se désagrègent en premier.
Pourquoi le pliage de l’ADN pourrait transformer la médecine
L’origami d’ADN exploite les mêmes règles d’appariement des bases qui stockent notre information génétique, mais les réutilise pour construire des objets à l’échelle nanométrique. Les chercheurs peuvent disposer des protéines, des médicaments ou des signaux immunostimulants sur ces objets comme des plots sur une plaque Lego, créant des thérapies très contrôlées contre le cancer, les maladies auto-immunes et les infections. Pour que de tels traitements de précision soient sûrs et efficaces, les autorités et les scientifiques doivent connaître l’intégrité de ces structures dans l’organisme et leur vitesse d’élimination — ensemble connues sous le nom de pharmacocinétique. Les méthodes de suivi existantes fixent généralement des colorants fluorescents ou comptent simplement des fragments d’ADN, ce qui peut faire passer des débris désassemblés pour des nanostructures intactes. Jusqu’à présent, il n’existait pas de moyen pratique de déterminer, chez des animaux vivants, si les formes originales d’origami d’ADN étaient encore entières.
Un « test d’intégrité » moléculaire pour l’origami d’ADN
L’équipe a mis au point une méthode qu’elle appelle PLASTIQ, pour proximity ligation assay for structural tracking and integrity quantification. L’idée clé est de laisser l’origami d’ADN rendre compte de son propre état. À des positions spécifiques de chaque structure, les chercheurs placent des paires de courts « staples » d’ADN qui se trouvent côte à côte le long d’une hélice lorsque l’origami est correctement replié. L’un de chaque paire porte un petit marqueur chimique permettant de les joindre enzymatiquement, ou ligaturer, mais uniquement s’ils sont maintenus proches l’un de l’autre par un brin échafaud intact. Si la structure fond, se casse ou est dégradée par des enzymes, ces deux pièces s’éloignent et ne peuvent plus être ligaturées. Après ligature, les paires jointes sont amplifiées par une réaction en chaîne par polymérase standard et quantifiées par qPCR sensible ou séquençage, transformant la présence de segments locaux intacts en signaux mesurables à partir de simples microlitres de sang.
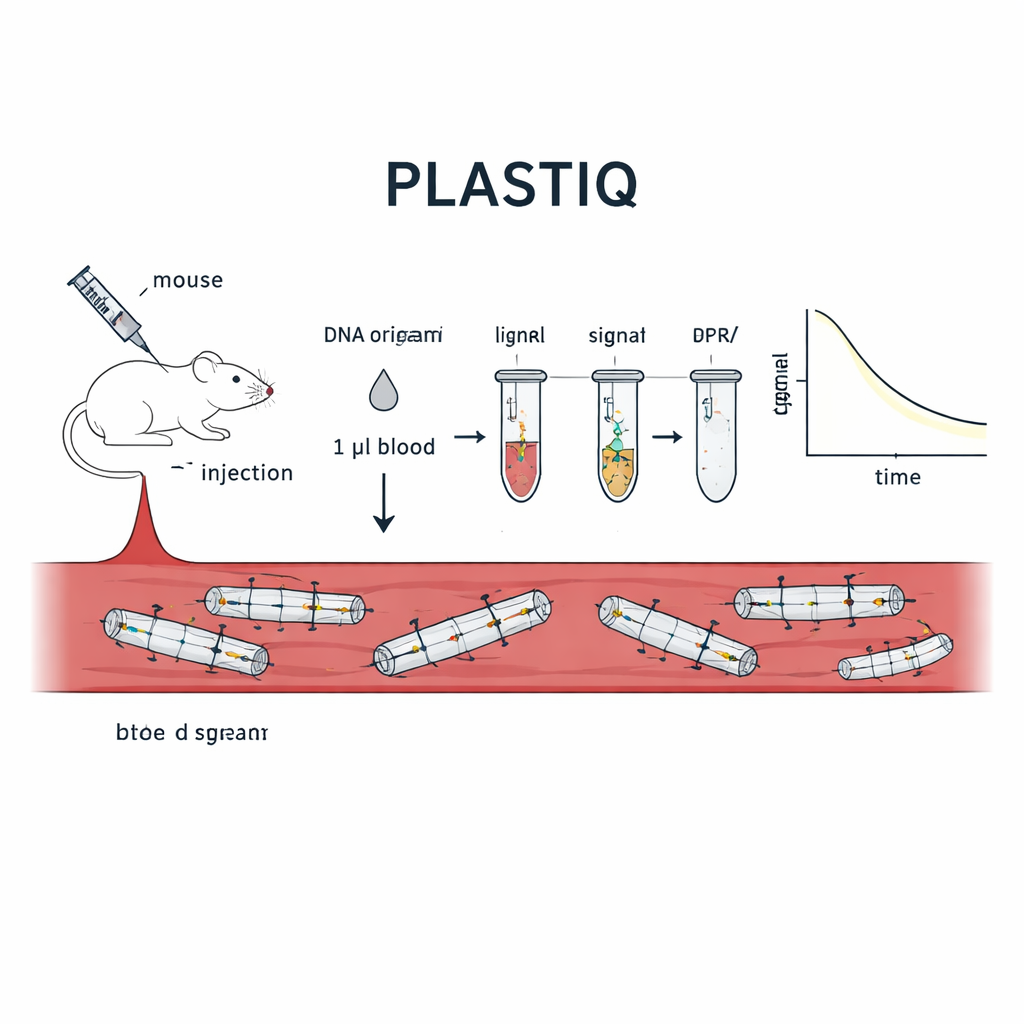
Mettre le test en œuvre chez des souris vivantes
Pour démontrer que PLASTIQ mesure réellement l’intégrité structurelle, les auteurs l’ont d’abord appliqué à des origamis d’ADN en forme de bâtonnets simples dans des éprouvettes. Des signaux n’apparaissaient que lorsque les bâtonnets étaient intacts et disparaissaient après dépliage par la chaleur, tandis que des essais ADN plus traditionnels détectaient toujours de l’ADN indépendamment de la forme. Ils ont ensuite injecté ces bâtonnets à des souris par différentes voies — directement dans la circulation sanguine, dans la cavité abdominale, dans le muscle et sous la peau — et prélevé seulement un microlitre de sang à différents moments. PLASTIQ a révélé comment la concentration de structures intactes augmentait puis diminuait selon la voie d’injection, correspondant aux attentes générales de la pharmacologie des médicaments mais avec un niveau de détail structurel bien supérieur. La méthode était sensible jusqu’à 0,01 femtomolaire, tout en nécessitant un volume sanguin minime, permettant des prélèvements répétés sur le même animal pendant plusieurs heures.
Tester des revêtements protecteurs et des points faibles cachés
De nombreux groupes cherchent à protéger les origamis d’ADN en les enrobant de polymères tels que le PEG, en réticulant les brins par UV ou en ajoutant des liants chimiques, mais il a été difficile d’évaluer l’efficacité réelle de ces astuces in vivo. En utilisant PLASTIQ, les auteurs ont montré que des bâtonnets revêtus de PEG restent intacts légèrement plus longtemps dans le sang que des bâtonnets nus, mais qu’ils sont aussi éliminés plus rapidement une fois en circulation, et que le revêtement n’empêche pas les enzymes PLASTIQ de fonctionner. En combinant PLASTIQ avec des modèles mathématiques simples, ils ont extrait des taux d’absorption et d’élimination pour différentes voies d’injection et revêtements, et ont même pu simuler des schémas d’administration répétée. Ils ont ensuite poussé la méthode plus loin avec un origami en forme de barillet à double couche, plus densément empaqueté à l’intérieur qu’à l’extérieur. Les mesures PLASTIQ ont montré que les staples à la surface extérieure exposée perdaient leur intégrité plus rapidement que ceux faisant face à la cavité interne, confirmant directement que les hélices enfouies sont protégées des enzymes dégradantes dans le sang.
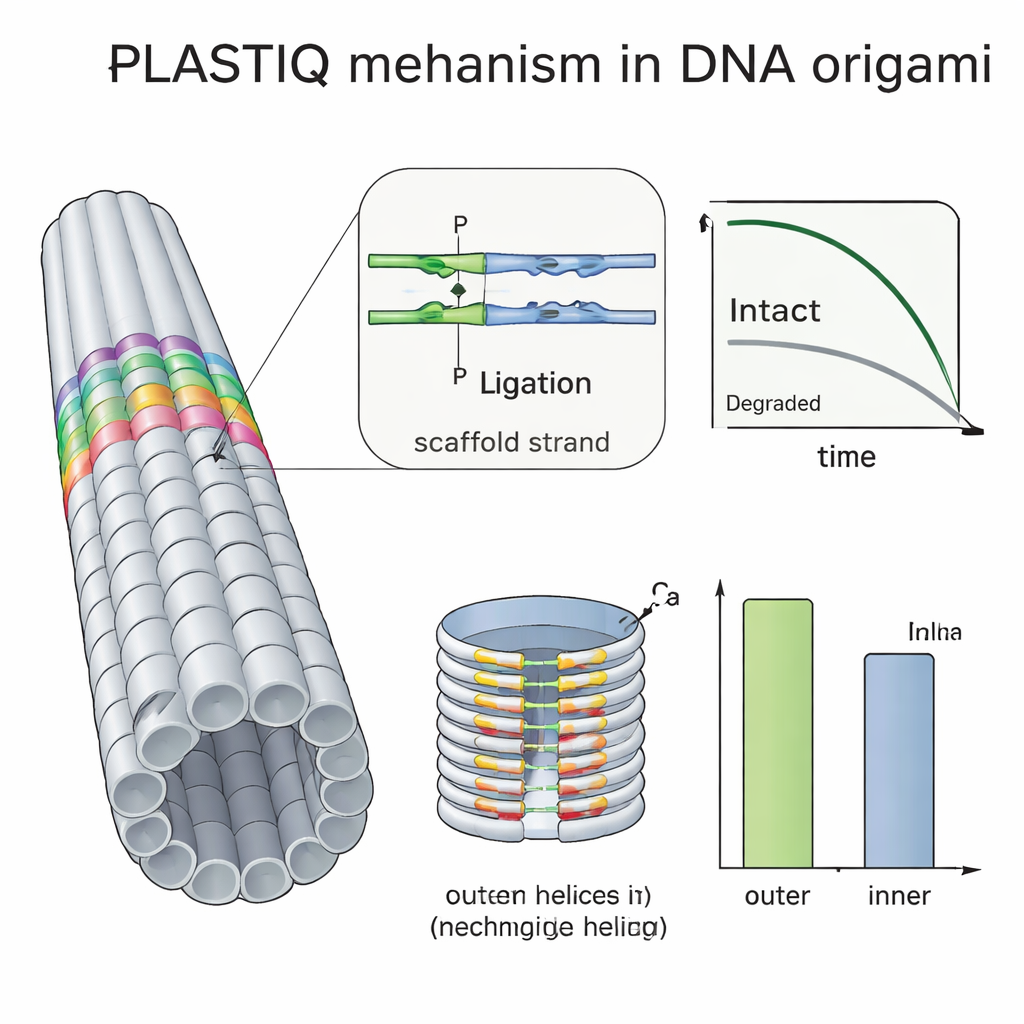
Ce que cela signifie pour les thérapies futures à base d’ADN
Pour un non-spécialiste, PLASTIQ peut être vu comme un bilan structural pour des dispositifs d’ADN à l’échelle nanométrique circulant dans l’organisme. Plutôt que de se contenter de demander « y a-t-il de l’ADN ici ? », il répond « cet ADN est-il encore replié dans l’objet précis que nous avons conçu ? ». En répondant à cette question avec une grande sensibilité à partir de petits échantillons sanguins, PLASTIQ offre aux développeurs de médicaments un moyen d’optimiser la conception, le revêtement et les schémas posologiques des médicaments et vaccins basés sur l’origami d’ADN. Avec le temps, ces informations détaillées et quantitatives sur le comportement de ces nanostructures dans des environnements biologiques réels pourraient aider à transformer l’origami d’ADN d’un concept élégant de laboratoire en des thérapeutiques fiables et conformes aux exigences réglementaires.
Citation: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Mots-clés: Origami d’ADN, nanomédecine, administration de médicaments, pharmacocinétique, nanotechnologie