Clear Sky Science · fr
La disruption de la tryptophanase favorise le mutualisme insecte–bactérie
Comment de minuscules partenaires intestinaux peuvent faire ou défaire un insecte
De nombreux animaux, y compris les humains, dépendent de trillions de microbes vivant dans leur intestin. Ces partenaires invisibles peuvent aider à digérer la nourriture, à fabriquer des vitamines, ou, dans certains cas, nous rendre malades. Cette étude examine une modification génétique simple mais surprenante chez des bactéries qui transforme un microbe ordinaire en un partenaire vital pour une punaise phytophage. En se concentrant sur un seul gène bactérien, le travail montre comment un changement microscopique peut déclencher une amitié stable entre des formes de vie très différentes.
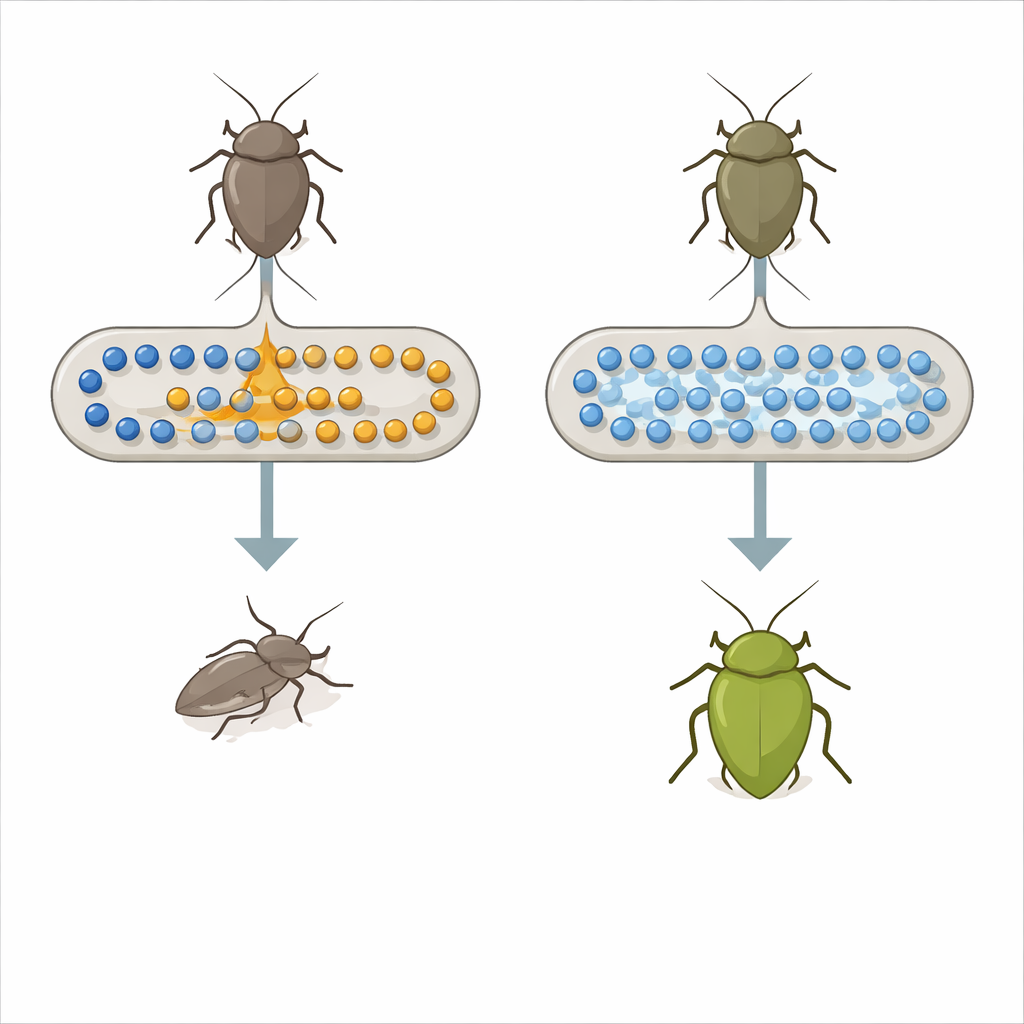
Une punaise, une bactérie et une alliance improbable
La punaise Plautia stali dépend de bactéries spéciales vivant dans une poche de son intestin moyen pour se développer et survivre. À l’état naturel, ces partenaires sont généralement des membres du genre Pantoea, qui fournissent des nutriments que l’insecte ne peut pas obtenir uniquement à partir de la sève des plantes. Des travaux en laboratoire avaient déjà montré qu’une souche commune d’Escherichia coli, une bactérie typique des intestins de mammifères, peut rapidement évoluer pour devenir un partenaire utile pour cette punaise après une seule mutation dans un système de contrôle global appelé répression catabolique du carbone. Cette découverte antérieure soulevait une grande question : un changement réglementaire aussi radical est‑il vraiment la manière dont des symbioses bénéfiques émergent dans la nature, ou existe‑t‑il un commutateur génétique plus ciblé ?
Suivre la piste d’un seul élément de construction
Pour répondre à cela, les chercheurs ont comparé des punaises portant des E. coli ordinaires à celles portant des mutants d’E. coli évolués et utiles. Ils ont mesuré de nombreuses petites molécules dans le sang et l’intestin des insectes. Un acide aminé essentiel, le tryptophane, s’est distingué : ses niveaux étaient plus de dix fois plus élevés chez les insectes hébergeant les mutants utiles que chez ceux hébergeant des E. coli normaux. Parmi des dizaines de gènes bactériens affectés par la mutation réglementaire antérieure, deux étaient liés au traitement du tryptophane. L’un, appelé tnaA, produit une enzyme qui dégrade le tryptophane en un composé nommé indole ainsi qu’en d’autres sous‑produits ; l’autre aide au transport du tryptophane dans la cellule. Lorsque l’équipe a supprimé le gène tnaA chez E. coli, les punaises se sont soudainement beaucoup mieux portées, avec une survie accrue et une couleur corporelle vert riche caractéristique d’insectes sains et bien nourris.
Quand moins de destruction signifie plus d’aide
Le changement clé s’est avéré ne pas être que les bactéries produisaient plus de tryptophane, mais qu’elles ont cessé de le détruire et de produire un excès d’indole. Les insectes portant des E. coli déficients en tnaA avaient des niveaux élevés de tryptophane et presque pas d’indole circulant dans leur corps. En revanche, les insectes portant des E. coli normaux avaient peu de tryptophane et beaucoup plus d’indole. Des expériences d’alimentation ont confirmé ce tableau : l’administration d’indole dans l’eau de boisson nuisait aux insectes, en particulier à ceux avec des bactéries productrices d’indole, tandis qu’un apport supplémentaire de tryptophane n’était nocif que lorsque les bactéries pouvaient le convertir en plus d’indole. Une souche distincte d’E. coli modifiée pour surproduire du tryptophane a donné aux punaises un léger avantage, renforçant l’idée que davantage de ce constituant, et moins de produit de dégradation toxique, améliore la santé de l’insecte.
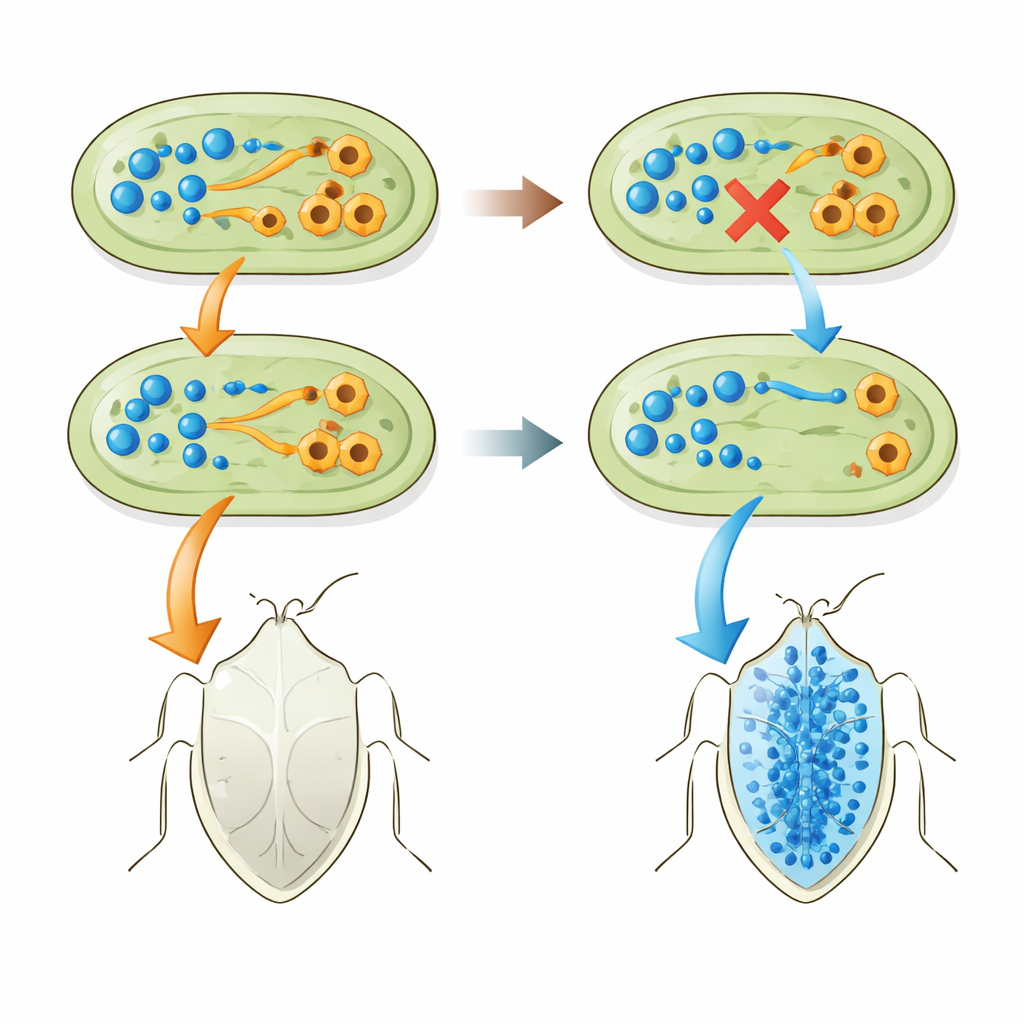
Les partenaires naturels partagent la même perte génétique
L’équipe a ensuite demandé si cette même perte de gène apparaissait dans des symbioses du monde réel. Ils ont séquencé les génomes de nombreuses bactéries Pantoea vivant à l’intérieur de P. stali et de punaises apparentées à travers les îles Ryukyu au Japon, ainsi que des souches de Pantoea isolées du sol qui pouvaient être amenées à aider les punaises. De façon frappante, chaque symbionte réussi ou potentiellement réussi manquait du gène tnaA et ne montrait aucune activité de l’enzyme dégradant le tryptophane. En revanche, plusieurs souches libres de Pantoea ananatis qui possédaient encore tnaA ne pouvaient pas du tout soutenir le développement des punaises. Lorsque les chercheurs ont inactivé tnaA dans l’une de ces souches de P. ananatis, sa capacité à aider les insectes s’est améliorée, bien que pas au niveau des partenaires naturels. Et lorsqu’ils ont forcé un symbionte naturel à porter un opéron tnaA actif, les insectes se sont moins bien portés et présentaient moins de tryptophane et plus d’indole dans leur sang.
Ce que cela signifie pour les partenariats cachés de la vie
Pris ensemble, les résultats pointent vers une règle simple mais puissante : les bactéries qui cessent de dégrader le tryptophane, évitant ainsi d’inonder leur hôte d’indole, sont plus susceptibles de devenir des partenaires fiables pour les punaises phytophages. En laboratoire, cela peut être déclenché par une mutation dans un système régulateur global ; dans la nature, cela se manifeste comme une perte directe du gène clivant le tryptophane lui‑même. Dans les deux cas, l’arrêt de cette enzyme permet d’aligner les intérêts de l’insecte et du microbe. L’étude suggère que le passage d’une association lâche à un mutualisme étroit peut parfois dépendre d’étapes génétiques étonnamment petites, et que des pertes de fonctions similaires dans le métabolisme bactérien peuvent sous‑tendre de nombreuses autres alliances cachées à travers l’arbre de la vie.
Citation: Wang, Y., Moriyama, M., Koga, R. et al. Tryptophanase disruption promotes insect–bacterium mutualism. Nat Microbiol 11, 759–769 (2026). https://doi.org/10.1038/s41564-026-02264-z
Mots-clés: microbiote intestinal des insectes, mutualisme bactérien, métabolisme du tryptophane, évolution de la symbiose, symbiontes Pantoea