Clear Sky Science · fr
La vaccination par ARNm surmonte l’altération des vaccins antipaludiques à parasite entier médiée par l’hémozoin chez la souris
Pourquoi un antécédent palustre affaiblit les vaccins
Le paludisme tue des centaines de milliers de personnes chaque année, et l’un des vaccins les plus prometteurs utilise des parasites entiers atténués pour entraîner le système immunitaire. Pourtant, curieusement, cette approche « référence » fonctionne bien mieux chez des personnes n’ayant jamais eu le paludisme que chez celles ayant grandi dans des régions où la maladie est courante. Cette étude, réalisée chez la souris, pose une question simple mais cruciale : qu’est‑ce dans les infections palustres antérieures qui fait qu’un vaccin très efficace perd soudainement de sa puissance — et un nouveau type de vaccin ARNm peut‑il résoudre le problème ?
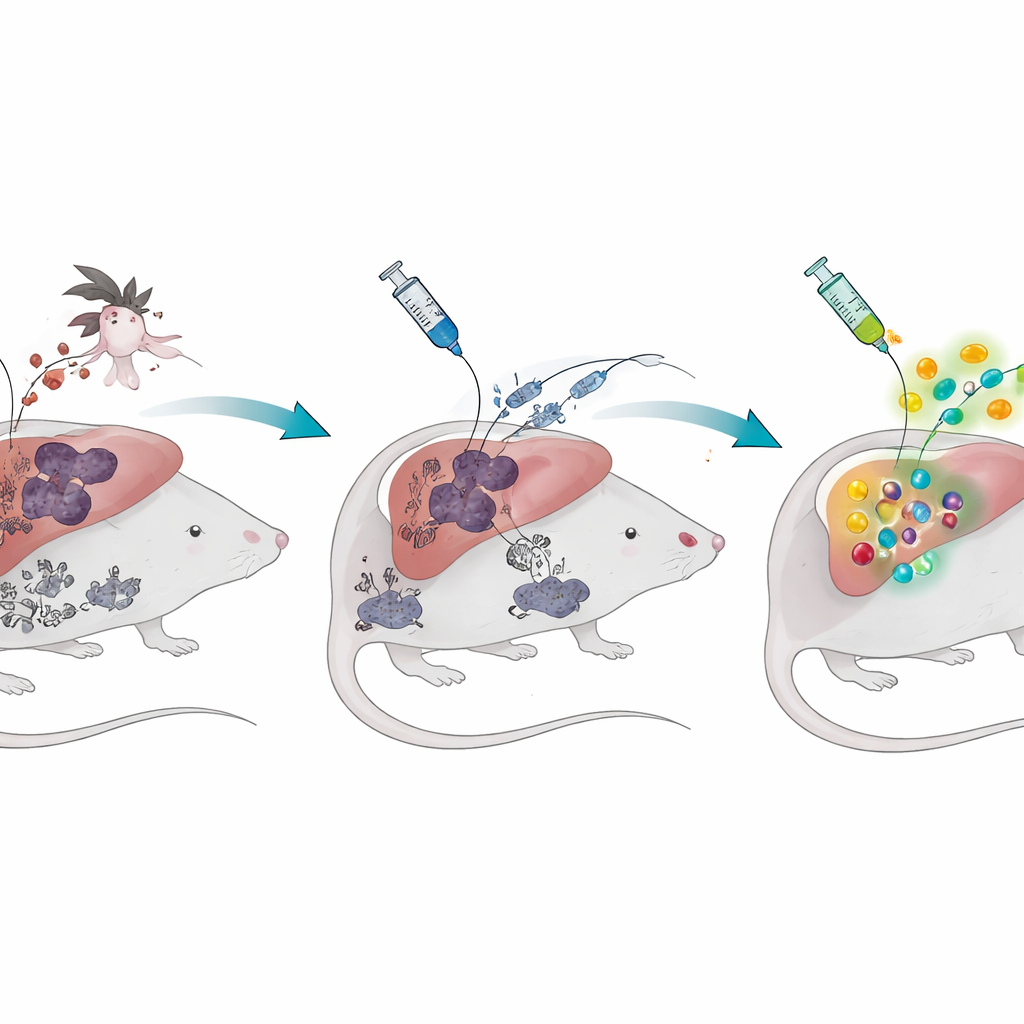
L’histoire de deux stades du paludisme
Le parasite du paludisme a deux stades principaux dans l’organisme humain. D’abord, après la piqûre d’un moustique, il infecte silencieusement le foie. Plus tard, il envahit les globules rouges, provoquant fièvre et maladie. Les vaccins à parasite entier dits de sporozoïtes atténués par irradiation ciblent le stade hépatique silencieux : les parasites pénètrent dans les cellules hépatiques mais ne peuvent pas achever leur cycle de vie, offrant au système immunitaire un aperçu sans danger. Chez les souris non exposées au paludisme, cette stratégie génère de grandes quantités de lymphocytes T cytotoxiques spécialisés qui s’installent dans le foie et peuvent éliminer les parasites avant qu’ils ne causent la maladie. Mais lorsque les chercheurs ont d’abord infecté les souris par un stade sanguin du paludisme puis laissé l’infection s’éteindre, le même vaccin a produit beaucoup moins de cellules T protectrices, et les animaux étaient beaucoup moins protégés lors d’un défi ultérieur avec des parasites vivants.
Un pigment persistant qui ne disparaît pas
L’équipe s’est ensuite demandé ce qui différenciait ces souris « expérimentées » par le paludisme. Un suspect majeur était l’hémozoin, un pigment sombre et cristallin que le parasite fabrique dans les globules rouges pour détoxifier les résidus riches en fer issus de la digestion de l’hémoglobine. Ce pigment ne disparaît pas à la guérison de l’infection ; il peut rester dans le foie, la rate et la moelle osseuse pendant de nombreux mois. Les scientifiques ont constaté que, même plus d’un an après la fin d’une infection sanguine, les souris présentaient toujours de l’hémozoin stocké et une réponse des cellules T affaiblie au vaccin ciblant le stade hépatique. L’administration à des souris saines d’hémozoin synthétique purifié — sans parasites vivants — suffisait à reproduire cette faiblesse vaccinale durable et à réduire la protection contre un défi palustre ultérieur.
Comment l’hémozoin perturbe les sentinelles immunitaires
En creusant davantage, les chercheurs se sont concentrés sur les cellules dendritiques, les sentinelles du système immunitaire qui captent des morceaux de pathogènes et les présentent aux cellules T. Pour que le vaccin à parasite entier au stade hépatique fonctionne, les cellules dendritiques doivent capturer le matériel parasitaire provenant des cellules hépatiques infectées et le montrer aux lymphocytes T cytotoxiques. Dans des expériences sur cultures cellulaires, l’équipe a démontré que l’hémozoin interfère directement avec cette étape de capture : plus les cellules dendritiques avaient été exposées à l’hémozoin, moins elles ingéraient efficacement les antigènes protéiques. Ce défaut est apparu aussi bien chez des cellules de souris que chez des cellules immunitaires humaines dérivées de donneurs de sang, et il ne dépendait pas d’un senseur inflammatoire bien connu, suggérant que l’hémozoin agit lui‑même comme un obstacle physique ou biochimique au traitement normal des antigènes.
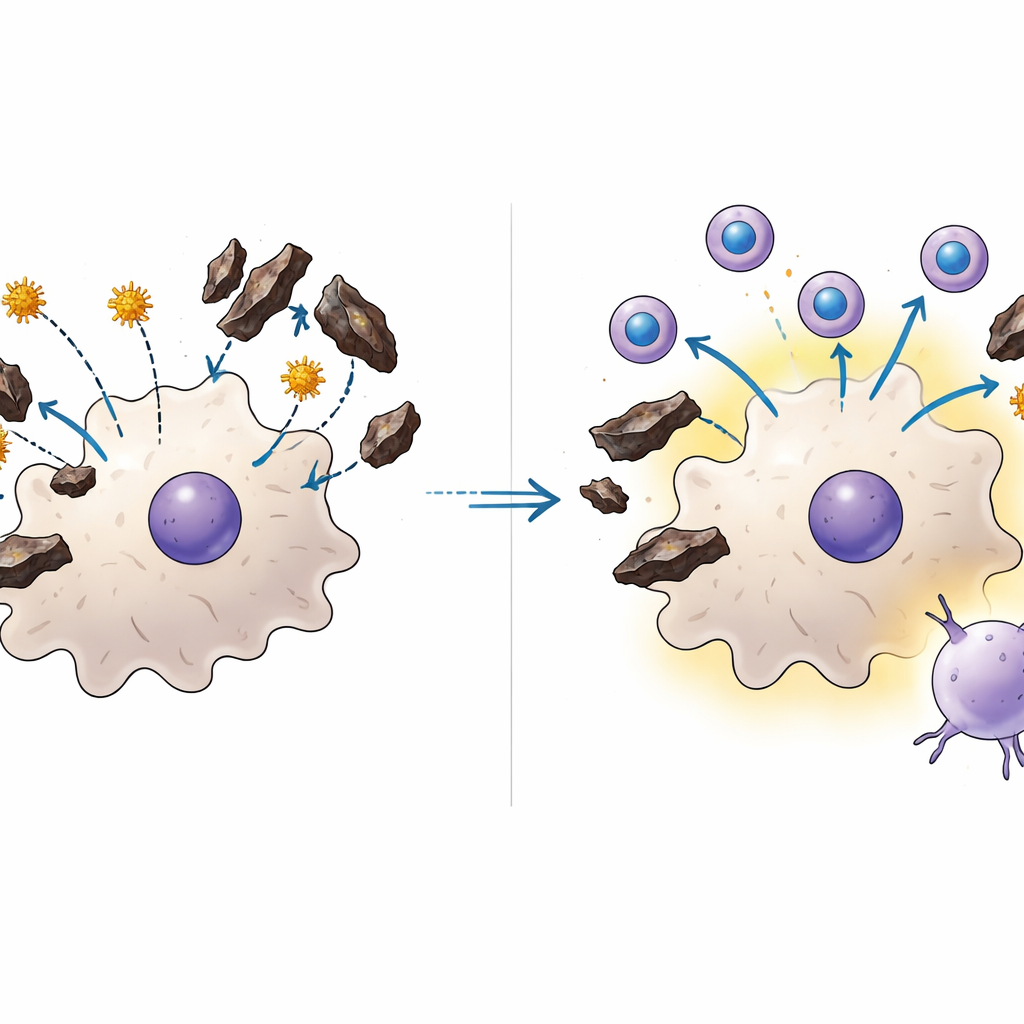
Les vaccins ARNm contournent l’obstacle
Pour savoir si un format vaccinal différent pouvait éviter ce problème, les scientifiques ont conçu un vaccin ARNm encapsulé dans des nanoparticules lipidiques. Au lieu d’apporter des protéines parasitaires depuis l’extérieur, cette approche donne aux cellules de l’hôte les instructions génétiques pour fabriquer de courts fragments de plusieurs protéines parasitaires à l’intérieur de la cellule. Chez des souris avec ou sans antécédent palustre, le vaccin ARNm a généré des réponses de lymphocytes T cytotoxiques d’une intensité comparable et a amélioré le contrôle de l’infection hépatique. Fait remarquable, lorsque le vaccin ARNm a été combiné avec une dose unique du vaccin à parasite entier du stade hépatique, les souris ont constitué des réservoirs de cellules T particulièrement importants qui ont pris une résidence à long terme dans le foie — une population cellulaire connue pour être clé dans la protection rapide. En culture, l’hémozoin n’a pas bloqué la prise en charge ni la fonction des nanoparticules chargées d’ARNm, ce qui explique comment cette stratégie peut réussir là où l’ancien vaccin seul échoue.
Ce que cela signifie pour les futures vaccinations contre le paludisme
Concrètement, l’étude montre que des infections palustres antérieures laissent des débris microscopiques semblables à des minéraux qui bouchent la façon dont certaines cellules immunitaires apprennent normalement à partir des vaccins, affaiblissant un des principaux vaccins antipaludiques à parasite entier. Mais en passant à un vaccin basé sur l’ARNm, ou en le combinant, qui insère discrètement les instructions des fragments parasitaires directement dans les cellules, les chercheurs peuvent contourner ces débris et restaurer une protection forte chez des hôtes déjà exposés au paludisme — du moins chez la souris. Ce travail désigne l’hémozoin comme un obstacle important pour la vaccination dans les populations vivant en zones endémiques, et suggère que des schémas vaccinaux ARNm ou mixtes soigneusement conçus pourraient être une voie prometteuse vers une immunisation antipaludique plus efficace et plus largement utile.
Citation: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Mots-clés: vaccins contre le paludisme, hémozoin, vaccin ARNm, immunité T cellulaire, infection à Plasmodium