Clear Sky Science · fr
Sites initiaux de la reprise du SIV après l’arrêt du traitement antirétroviral chez le macaque rhésus
Pourquoi le virus revient
Les médicaments modernes contre le VIH peuvent faire chuter la charge virale sanguine à des niveaux si faibles que les tests standard ne détectent plus rien. Pourtant, quand le traitement est interrompu, le virus réapparaît presque toujours. Cette étude chez le macaque rhésus, infecté par un proche cousin du VIH appelé SIV, pose une question simple mais cruciale : où, exactement, survient la toute première étincelle de cette reprise virale dans le corps, et quels types de tissus l’alimentent ensuite ?
Suivre des codes-barres viraux
Pour suivre le virus avec une précision inhabituelle, les chercheurs ont utilisé un SIV spécial dans lequel chaque particule virale porte un « code-barres » génétique unique : une courte séquence inoffensive qui fonctionne comme un numéro de série. Vingt-quatre macaques ont été infectés par un mélange de milliers de ces virus codés, puis rapidement mis sous une puissante trithérapie antirétrovirale. Les médicaments ont fait chuter la charge virale sanguine jusqu’à des niveaux essentiellement indétectables et l’y ont maintenue pendant plus d’un an, reproduisant une thérapie antirétrovirale efficace et prolongée chez l’humain. Parce que chaque code-barres marquait une lignée virale distincte, l’équipe a pu identifier ensuite quelles lignées spécifiques se réveillaient à l’arrêt du traitement et où dans le corps cet éveil prenait initialement racine.
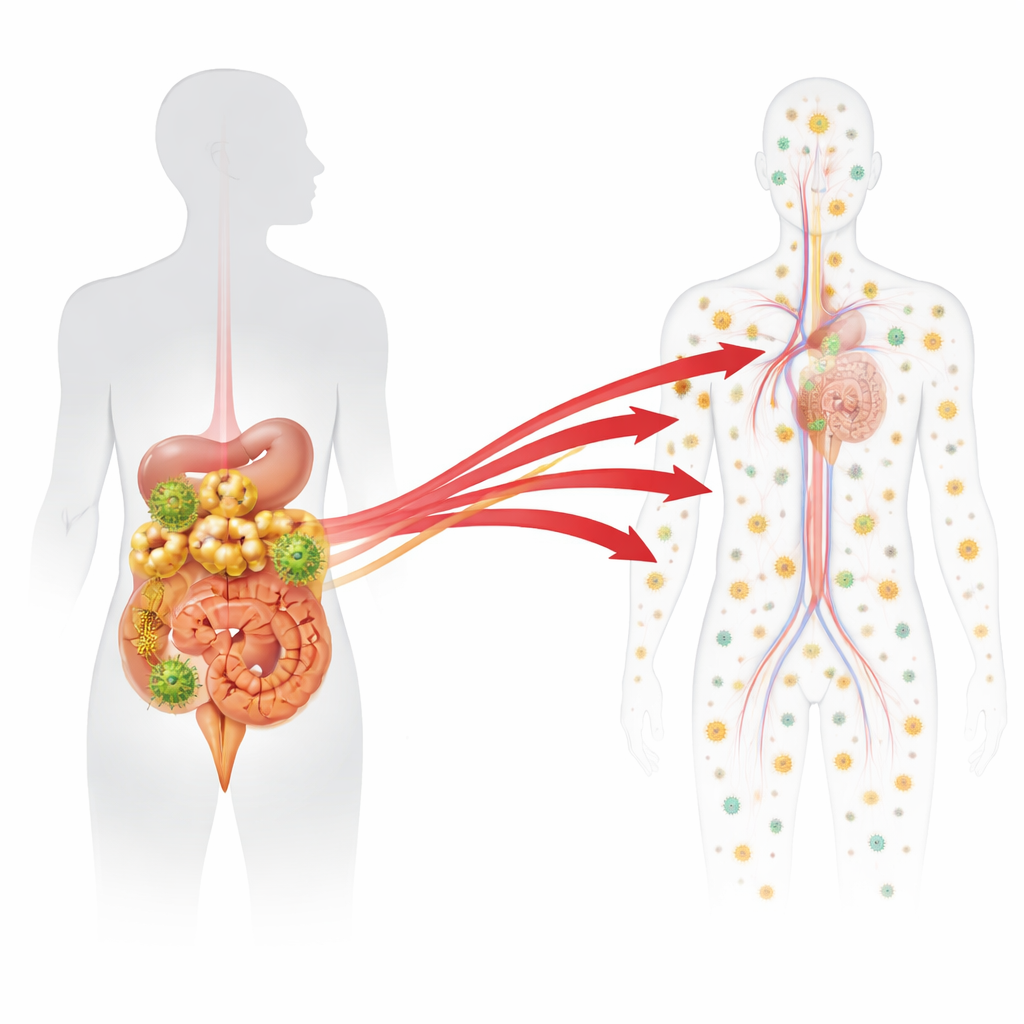
Explorer les tissus pendant et après le traitement
À la fin de cette longue période de traitement, les macaques ont été répartis en groupes. Certains ont été examinés alors qu’ils étaient encore sous traitement pour définir le schéma de fond normal des faibles quantités de matériel génétique viral qui persistent malgré les médicaments. D’autres ont vu le traitement interrompu puis ont été examinés soit cinq, soit sept jours plus tard, avant ou au moment où le virus commençait à réapparaître dans le sang. Chez chaque animal, les scientifiques ont prélevé et analysé environ 90 échantillons tissulaires couvrant l’intestin, de nombreux types de ganglions lymphatiques, des organes hématopoïétiques comme la moelle osseuse, et des organes non immunitaires tels que le foie et le poumon. Pour chaque tissu, ils ont mesuré la quantité d’ADN viral (signe de cellules infectées) et d’ARN viral (signe de production virale active) présente pour chaque code-barres. Ils ont ensuite utilisé des modèles statistiques pour repérer tout code-barres dont le niveau d’ARN dans un tissu donné dépassait nettement ce que l’on attendrait d’une simple activité de fond de faible intensité pendant le traitement.
Repérer les premières étincelles de reprise
Ces codes-barres anormalement actifs, que les chercheurs ont qualifiés d’« outliers », ont mis en évidence des lignées virales probablement en train de subir de nouvelles poussées de réplication et de propagation locale après l’arrêt des médicaments. Chez l’ensemble des animaux, ils ont identifié 32 de ces outliers. Crucialement, lorsque le virus est réapparu dans le sang, environ la moitié des codes-barres détectés dans le plasma correspondaient à ces outliers tissulaires, reliant directement des sites tissulaires spécifiques à la phase la plus précoce de la reprise systémique. La plupart des outliers n’apparaissaient que dans un seul échantillon tissulaire, cohérent avec un point de départ très local, tandis qu’une fraction plus petite s’était déjà étendue à des segments intestinaux voisins et à leurs ganglions lymphatiques drainants. Dans un seul animal présentant des niveaux viraux sanguins nettement plus élevés, l’équipe a observé des preuves que plusieurs tissus — y compris des sites distants — avaient déjà été resemmencés. Cela suggère une progression par étapes : d’abord une ignition discrète en un point, puis une expansion locale, puis une dissémination à l’échelle du corps.
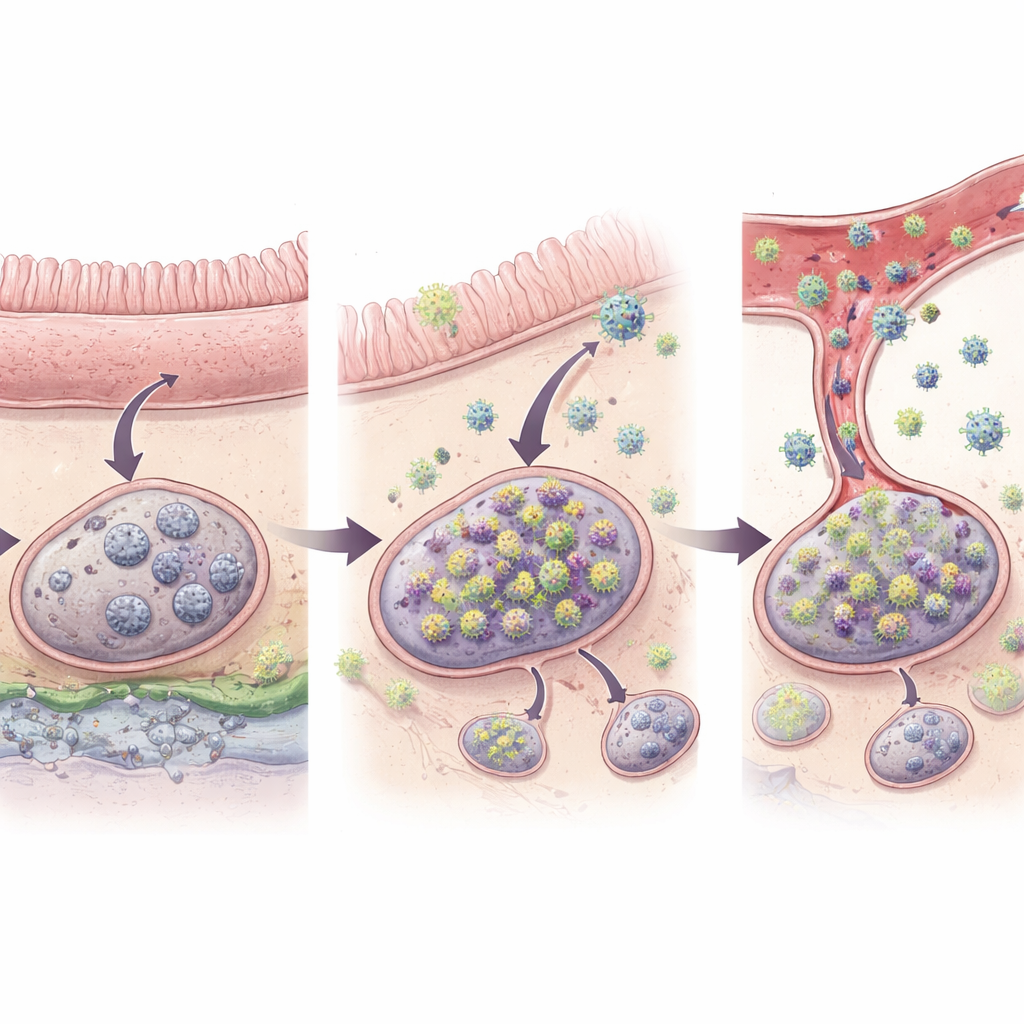
Pourquoi l’intestin compte le plus
Un constat a été particulièrement marquant : presque tous les événements précoces de reprise revenaient au tractus digestif et aux tissus immunitaires qui le desservent. Sur les 27 codes-barres jugés représenter de véritables origines de reprise, 96 % se trouvaient dans l’intestin lui-même ou dans les ganglions lymphatiques associés à l’intestin, tels que les ganglions mésentériques drainant l’intestin grêle et le côlon. Un seul site d’origine est apparu dans un ganglion lymphatique non lié à l’intestin, et aucun n’a été identifié dans des organes comme le foie, le poumon ou la moelle osseuse. Les analyses statistiques ont montré que, même en tenant compte du nombre de cellules infectées présentes, les tissus lymphoïdes associés à l’intestin étaient environ dix fois plus susceptibles que d’autres sites lymphoïdes de donner naissance à un virus en reprise. L’environnement particulier de l’intestin — constamment exposé à la nourriture et aux microbes et souvent enflammé dans des infections de type VIH — peut maintenir les cellules infectées plus actives et plus facilement susceptibles d’être stimulées à produire à nouveau du virus.
Ce que cela signifie pour les futurs traitements curatifs
En résumé, ce travail montre que lorsque des médicaments puissants contre des virus proches du VIH sont arrêtés, le virus redémarre presque toujours à partir de quelques réservoirs cachés dans et autour de l’intestin plutôt que de manière égale depuis toutes les régions du corps. Au début, ces flambées sont minimes et confinées à une seule zone tissulaire, mais une fois que le virus atteint le sang et des organes distants, les niveaux augmentent rapidement. Pour les stratégies visant la rémission durable ou la guérison, cela signifie que les thérapies doivent atteindre et être efficaces dans les tissus immunitaires intestinaux. Des outils capables de visualiser ou d’échantillonner ces sites difficiles d’accès chez l’humain, ou des médicaments spécialement conçus pour agir là, pourraient être essentiels pour empêcher que les premières étincelles de reprise ne prennent jamais feu.
Citation: Keele, B.F., Okoye, A.A., Immonen, T.T. et al. Initial sites of SIV rebound after antiretroviral treatment cessation in rhesus macaques. Nat Microbiol 11, 648–663 (2026). https://doi.org/10.1038/s41564-025-02258-3
Mots-clés: Reprise du VIH, réservoirs viraux, tissu lymphoïde intestinal, modèle du macaque rhésus, interruption de la thérapie antirétrovirale