Clear Sky Science · fr
Analyse comparative des jeux de données de balayage mutagène profond chez les entérovirus A et B identifie une divergence fonctionnelle et des cibles thérapeutiques
Pourquoi ces petits virus à ARN nous concernent
Les entérovirus forment un vaste groupe de petits virus à ARN qui circulent discrètement dans le monde entier, provoquant le plus souvent des rhumes ou des gastro-entérites bénignes, mais pouvant parfois déclencher des paralysies, des lésions cardiaques ou d’autres maladies graves. Nous disposons de peu de vaccins et encore moins de médicaments efficaces à large spectre contre eux, en partie parce que ces virus évoluent très rapidement. Cette étude pose une question apparemment simple mais aux enjeux pratiques importants : quand ces virus mutent, quelles parties de leur machinerie peuvent changer librement, et quelles parties sont si vitales que l’évolution les maintient presque figées ? Les réponses indiquent de nouvelles stratégies pour concevoir des traitements difficiles à contourner pour le virus.
Lire le manuel d’instructions du virus, mutation par mutation
Les chercheurs se sont concentrés sur deux entérovirus humains provoquant des maladies très différentes : l’entérovirus A71, lié à des atteintes neurologiques sévères chez l’enfant, et le coxsackievirus B3, associé à des inflammations cardiaques et même à un risque de cancer du pancréas. Grâce à une technique appelée balayage mutagène profond, ils ont créé des bibliothèques virales dans lesquelles presque chaque position des protéines virales a été modifiée systématiquement. Ces virus mutants ont été autorisés à infecter des cellules en culture, et le séquençage à haut débit a permis de mesurer comment chaque changement affectait la croissance virale. En comparant chaque mutant au virus d’origine, l’équipe a construit une carte détaillée des sites du protéome viral qui tolèrent les changements et de ceux qui sont fortement contraints. 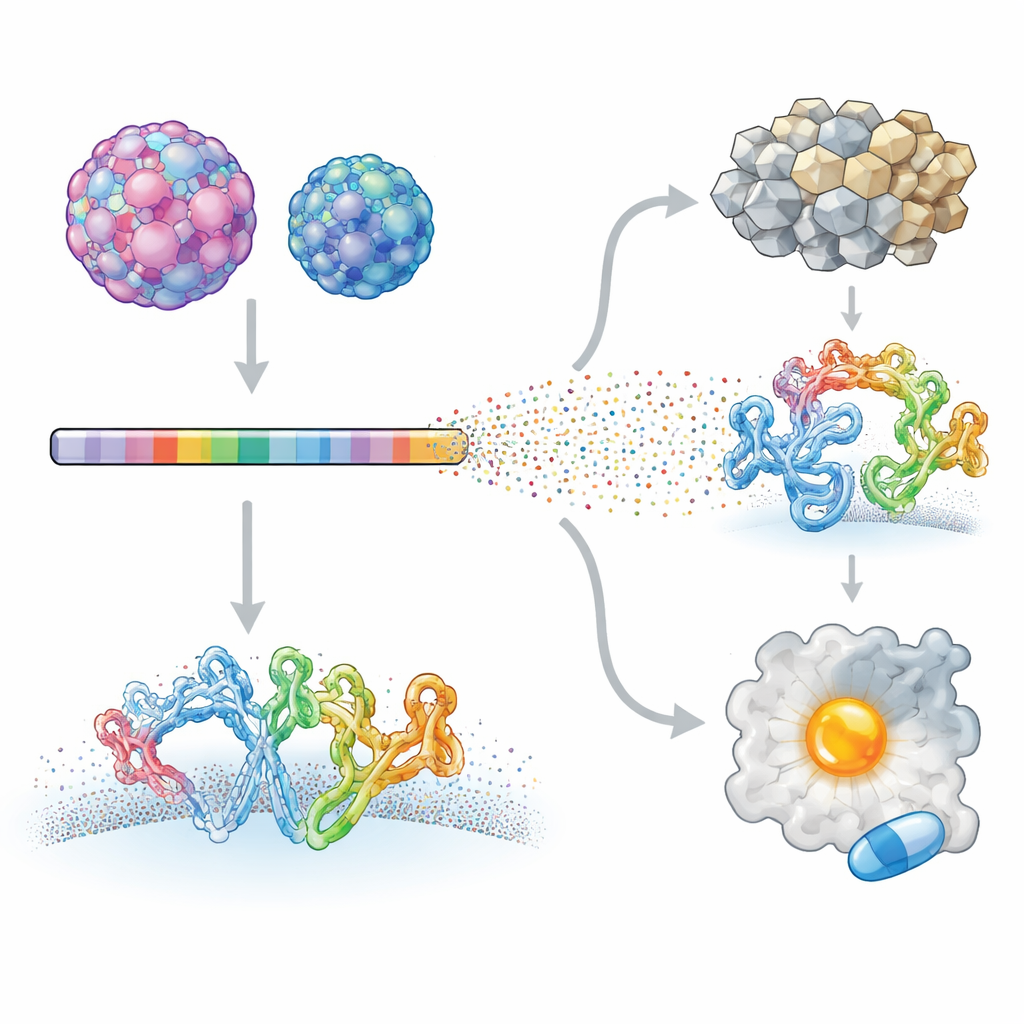
Limites communes strictes et flexibilité spécifique aux virus
Bien qu’ils ne partagent qu’environ la moitié de leurs séquences d’acides aminés, les deux virus ont montré des schémas de contrainte globale remarquablement semblables. Les « chevaux de trait » enzymatiques internes qui copient le génome, clivent les protéines virales et déroulent l’ARN étaient très sensibles aux mutations dans les deux virus. De même, les surfaces internes qui maintiennent l’architecture de la coque protéique, ou capside, se sont révélées difficiles à modifier sans compromettre le virus. En revanche, de nombreuses régions exposées et interagissant avec l’hôte étaient plus libres de changer et différaient souvent nettement entre les deux espèces. L’analyse structurale a montré que les régions conservées et intolérantes aux mutations se regroupent autour des sites actifs et des interfaces d’assemblage, alors que les régions en contact avec les récepteurs cellulaires, les membranes ou les molécules immunitaires sont des points chauds de flexibilité spécifique à chaque espèce.
Comment les virus rencontrent les cellules et échappent aux défenses
L’équipe s’est ensuite concentrée sur la poignée moléculaire entre le virus et l’hôte. L’entérovirus A71 et le coxsackievirus B3 utilisent des récepteurs cellulaires différents pour pénétrer, et l’étude a montré que les empreintes de contact exactes sur la surface de la capside figurent parmi les régions les plus divergentes en termes de tolérance aux mutations. Les résidus qui saisissent le récepteur pour un virus sont fortement contraints dans ce virus mais relativement permissifs dans l’autre, reflétant la façon dont chacun a affiné sa « plateforme » d’amarrage. Une divergence similaire est apparue dans une petite protéine membranaire appelée 3A, qui aide à remodeler les membranes cellulaires et à recruter des facteurs de l’hôte pour la réplication du génome. La modélisation suggère que les deux virus utilisent des zones de contact partiellement différentes sur 3A pour engager le même facteur de l’hôte, GBF1, et peuvent également insérer cette protéine dans les membranes à des profondeurs différentes. Ces différences aident à expliquer pourquoi des virus étroitement apparentés peuvent infecter des tissus différents et provoquer des tableaux cliniques distincts.
Ce que l’évolution en laboratoire ne révèle pas — et ce qu’elle capture
Pour replacer leurs expériences en culture cellulaire dans un contexte réel, les auteurs ont comparé leurs cartes de mutations à des milliers de séquences virales naturelles issues d’échantillons de patients. Globalement, les sites flexibles en laboratoire avaient tendance à être aussi variables dans la nature, en particulier sur des comparaisons à l’échelle des espèces. Cependant, lorsqu’ils ont examiné quels acides aminés spécifiques étaient préférés à chaque position, l’évolution naturelle et la sélection en laboratoire concordaient le plus au sein d’un même type viral. Notamment, les plus grands désaccords se concentraient à la surface externe de la capside et sur les régions en contact avec l’hôte des protéines non structurales 2A et 3A — précisément là où les réponses immunitaires et les environnements hostiles complexes sont censés jouer le rôle le plus important. Cela suggère que le balayage mutagène profond capture les contraintes mécaniques fondamentales des protéines virales, tandis que les infections réelles superposent des pressions supplémentaires venant de l’immunité et du tropisme tissulaire, difficiles à reproduire in vitro.
Trouver un point faible partagé pour de futurs médicaments
Enfin, les chercheurs ont cherché à savoir si ces cartes pouvaient mettre en évidence un talon d’Achille commun pour le développement de médicaments. À l’aide d’outils de calcul, ils ont recherché dans les deux virus des poches à la surface des protéines susceptibles, en principe, de lier de petites molécules. Ils ont ensuite superposé les données de mutationalité pour voir quelles poches étaient composées de résidus que le virus ne peut pas facilement changer sans se nuire. Une poche, située sur l’hélicase 2C — un moteur en forme d’anneau qui aide à dérouler l’ARN viral — a émergé. Sa forme et ses résidus constitutifs sont fortement conservés à travers quatre grandes espèces humaines d’entérovirus, elle se situe à l’écart des sites actifs déjà connus, et les changements y sont à la fois rares dans la nature et fortement délétères dans les tests en laboratoire. 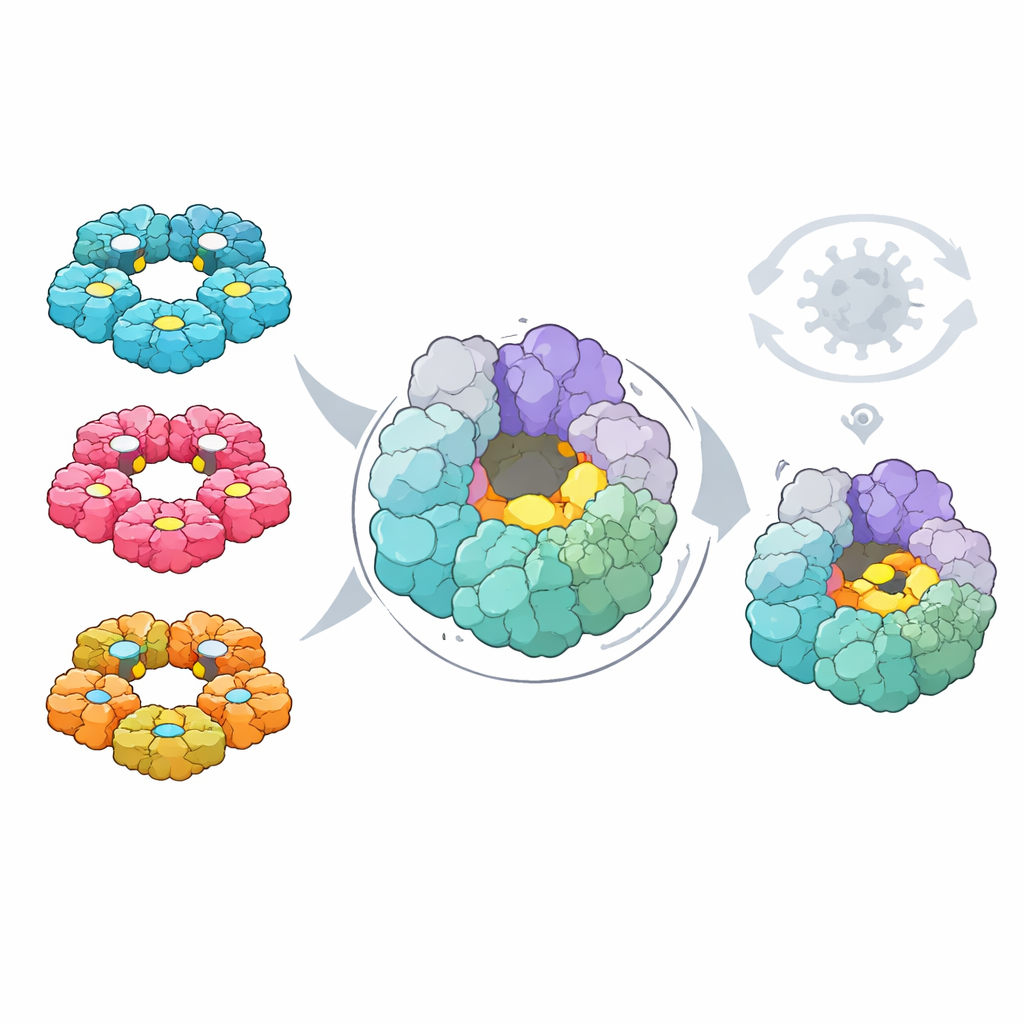
Ce que cela signifie pour les traitements futurs
En sondant systématiquement comment chaque changement d’une seule lettre affecte deux entérovirus importants, cette étude révèle une division nette entre un noyau partagé et rigide de la machinerie virale et des interfaces plus flexibles, spécifiques à chaque virus, en contact avec l’hôte. Le noyau conservé inclut une poche nouvellement mise en évidence sur l’hélicase 2C qui semble difficile à muter pour le virus sans sacrifier sa fitness, ce qui en fait une cible attrayante pour des antiviraux à large spectre avec une forte barrière à la résistance. Parallèlement, les surfaces externes et les sites de contact avec l’hôte, plus adaptables, expliquent pourquoi des virus apparentés se comportent si différemment dans l’organisme et indiquent où les vaccins et les thérapies à base d’immunité devront composer avec une évolution rapide. Ensemble, ces découvertes fournissent une feuille de route pour concevoir des traitements qui exploitent les propres limites évolutives du virus.
Citation: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Mots-clés: entérovirus, évolution virale, balayage mutagène profond, cibles antivirales, hélicase 2C