Clear Sky Science · fr
Des voies H2 natives permettent l’hydrogénation biocompatible d’alcènes métaboliques dans des bactéries
Transformer les microbes en petites usines vertes
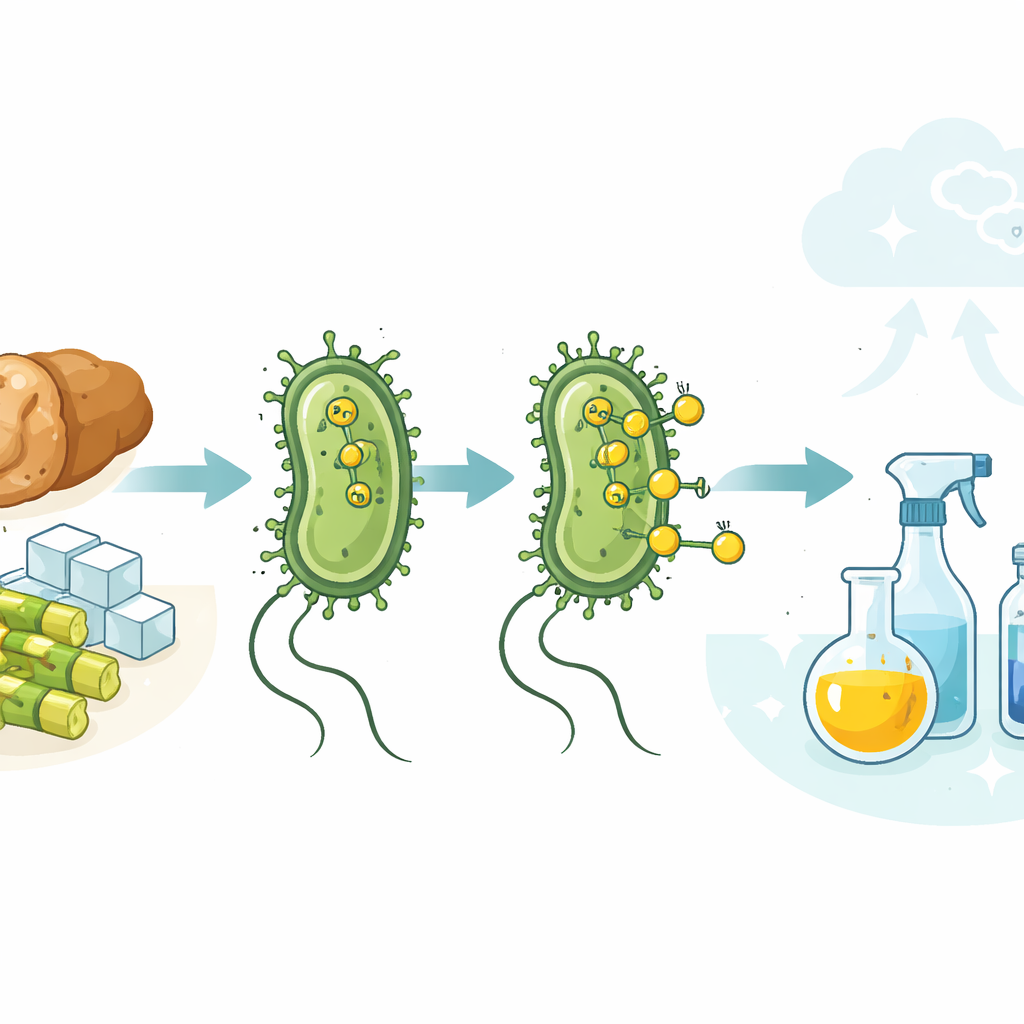
Imaginez que des bactéries intestinales courantes puissent contribuer à remplacer les combustibles fossiles dans la production de produits du quotidien — des conservateurs alimentaires aux plastiques — tout en valorisant les déchets alimentaires. Cette étude montre que des souches ordinaires d’Escherichia coli de laboratoire peuvent faire exactement cela : elles produisent naturellement de l’hydrogène à l’intérieur de leurs cellules, et cet hydrogène peut être exploité à la surface cellulaire pour alimenter des réactions chimiques de type industriel dans des conditions douces, en milieu aqueux. En associant des microbes vivants à un catalyseur métallique solide, les auteurs dessinent une voie vers une fabrication plus propre et émettant moins de carbone.
Pourquoi l’hydrogène compte pour les produits de tous les jours
La molécule d’hydrogène est au cœur de la chimie contemporaine. On l’utilise pour transformer des huiles liquides en pâtes à tartiner, améliorer des carburants bruts et synthétiser de nombreux ingrédients pour les médicaments et les plastiques. Aujourd’hui, presque tout cet hydrogène provient de combustibles fossiles, principalement du gaz naturel et du charbon, ce qui dégage de grandes quantités de dioxyde de carbone. Parallèlement, de nombreux microbes relâchent naturellement de l’hydrogène en dégradant des sucres lorsque l’oxygène vient à manquer. Le défi que relèvent les auteurs est de capter ce flux d’hydrogène biologique doux pour piloter les mêmes types de réactions que l’industrie réalise aujourd’hui sous haute pression, en solvants organiques et avec des gaz d’origine fossile.
Laisser les bactéries alimenter un catalyseur métallique
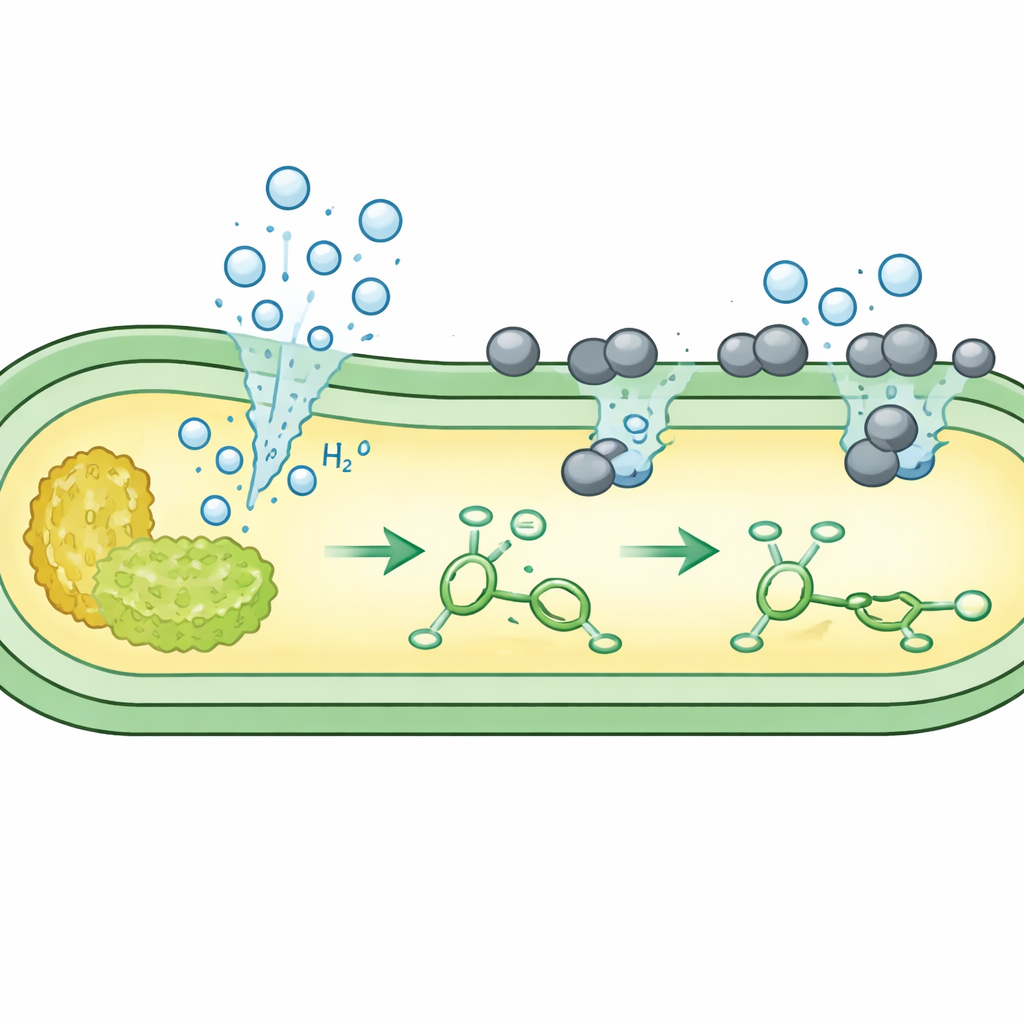
L’équipe s’est concentrée sur des réactions d’addition d’hydrogène simples, où une double liaison dans une molécule est « saturée » par l’hydrogène. Ils ont cultivé plusieurs souches d’E. coli non modifiées dans un milieu à base de sucre, puis ajouté un catalyseur de palladium finement dispersé et compatible avec les cellules vivantes. En conditions anaérobies, le métabolisme natif des bactéries convertissait le sucre en formiate puis en hydrogène au niveau intérieur de la membrane cellulaire. La microscopie a montré que les particules de catalyseur, chargées positivement, se déposent sur la surface cellulaire chargée négativement, là où elles rencontrent l’hydrogène qui s’échappe. Là, le métal utilise l’hydrogène microbien pour réduire une molécule test, l’acide caféique, en son produit saturé avec des rendements très élevés — souvent supérieurs à ceux obtenus avec une souche fortement modifiée précédemment utilisée.
Élargir la gamme de produits et de matières premières
Une fois la réaction de base démontrée, les chercheurs ont testé une large gamme de molécules contenant des liaisons doubles carbone–carbone, y compris des acides d’origine végétale et des composés gras à longue chaîne. Beaucoup ont été convertis en leurs formes saturées de façon fluide, certaines avec des rendements presque quantitatifs. Ils ont également construit des souches d’E. coli qui produisent davantage d’hydrogène en détournant plus de flux métabolique vers la voie native de formation d’hydrogène. Ces souches amplifiées ont permis des conversions similaires avec moins de catalyseur métallique. Fait remarquable, l’équipe a remplacé le sucre pur par du pain rassis liquéfié comme source alimentaire. Des enzymes ont décomposé le pain en glucose, que les bactéries ont fermenté tout aussi efficacement, transformant un déchet alimentaire courant en hydrogène biologique et en produits chimiques à valeur ajoutée.
Produire à la fois ingrédient et carburant au sein d’une même cellule
Les auteurs se sont ensuite demandé si une seule bactérie pouvait produire non seulement le « réactif » hydrogène mais aussi le « substrat » insaturé qu’il est censé modifier. Ils ont modifié E. coli de sorte que le sucre alimente d’abord des voies produisant des blocs aromatiques comme l’acide cinnamique et l’acide coumarique, et une autre voie produisant de l’hydrogène. Lorsque la culture avait accumulé ces métabolites internes, ils ont ajouté le catalyseur au palladium. À la surface cellulaire, le catalyseur a utilisé l’hydrogène produit in situ pour convertir les métabolites nouvellement formés à double liaison en produits pleinement saturés tels que l’acide hydrocinnamique, la desaminotyrosine et l’acide adipique, précurseur clé du nylon. Dans certaines conceptions, cette cométabolisation a atteint une conversion quasi complète, le tout au sein d’une même culture vivante.
Évaluer le bénéfice climatique
Pour savoir si cette biochimie astucieuse profite réellement au climat, l’équipe a réalisé une analyse du cycle de vie comparant leur approche hybride « chimio‑microbienne » aux voies d’hydrogénation classiques utilisant de l’hydrogène d’origine fossile ou électrolytique. Lorsque l’hydrogène biologique et la production intracellulaire des substrats étaient combinés dans un processus unique et économisant la chaleur, les émissions totales de gaz à effet de serre chutaient sensiblement. L’utilisation de pain rassis comme matière première a encore renforcé l’avantage : en évitant la mise en décharge ou l’incinération et en transformant des aliments jetés en produits chimiques, certains scénarios sont devenus globalement négatifs en carbone, c’est‑à‑dire qu’ils retirent plus de gaz à effet de serre qu’ils n’en émettent.
Ce que cela signifie pour la fabrication de demain
En termes simples, l’étude montre que des bactéries ordinaires peuvent être amenées à jouer à la fois le rôle de source d’énergie et d’usine d’ingrédients pour des réactions chimiques importantes, tandis qu’un métal solide à leur surface achève discrètement la transformation. Parce que tout se passe dans l’eau, à des températures proches de celle du corps et en utilisant des sucres renouvelables ou des déchets, cette approche pourrait un jour offrir des alternatives plus propres aux usines pétrochimiques traditionnelles. Avec un affinement des voies microbiennes et des catalyseurs, cette plateforme à cellules vivantes pourrait permettre une nouvelle génération de procédés durables qui transforment le carbone renouvelable et les aliments jetés en produits utiles avec une empreinte climatique bien moindre.
Citation: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Mots-clés: hydrogène microbien, chimie verte, biocatalyse, déchets-vers-produits chimiques, fabrication durable