Clear Sky Science · fr
Des pseudo-produits naturels monovalents surchargent la dégradation de l’IDO1 par son E3 natif KLHDC3
Désactiver une enzyme favorable au cancer
Notre système immunitaire surveille en permanence les cellules cancéreuses, mais les tumeurs ripostent souvent en détournant la chimie du corps. Un acteur clé de cette lutte est une enzyme appelée IDO1, qui aide les tumeurs à neutraliser les cellules immunitaires. Cette étude décrit une nouvelle classe de petites molécules qui fait plus que bloquer l’activité d’IDO1 : elle incite les cellules à se débarrasser complètement de l’enzyme. En exploitant la machinerie d’élimination naturelle de la cellule, ces composés pourraient raviver les attaques immunitaires contre les tumeurs de façons que les médicaments plus anciens ne pouvaient pas accomplir.
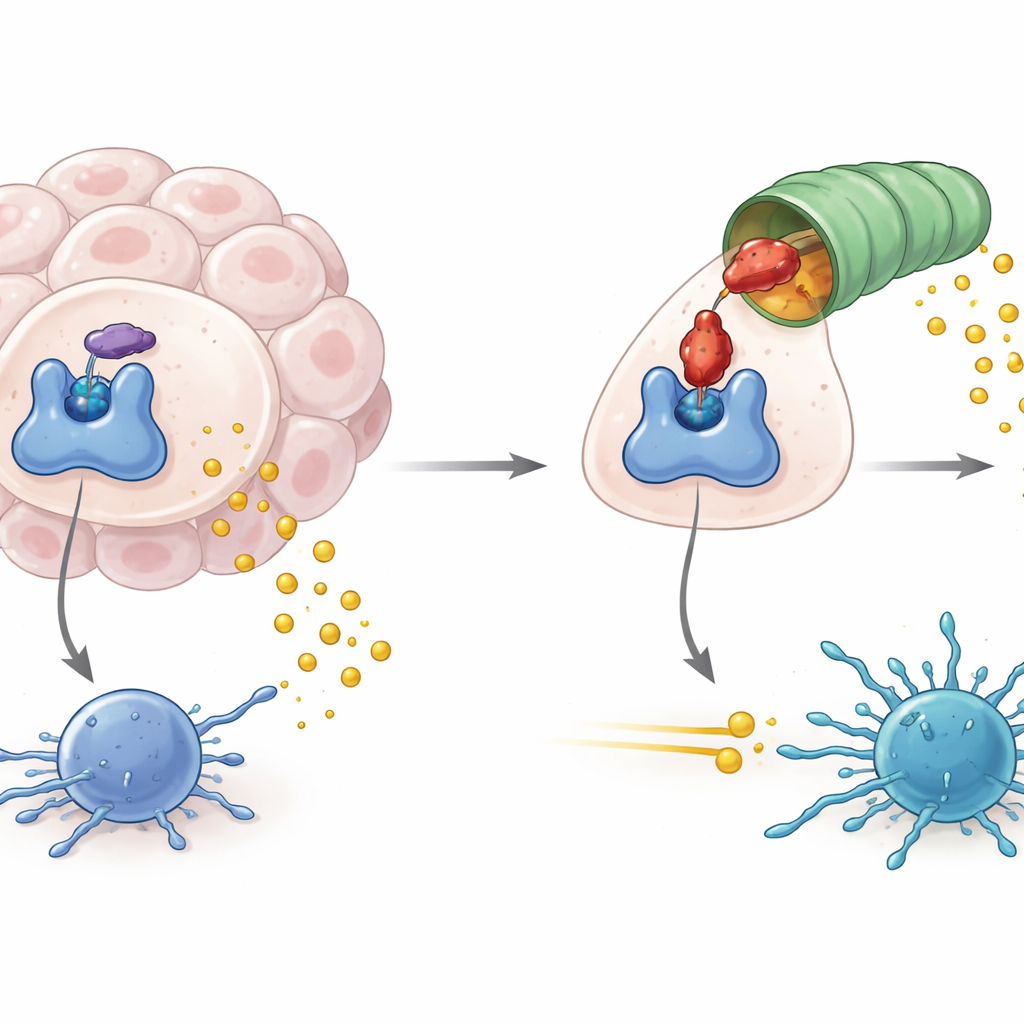
Comment les tumeurs exploitent un régulateur métabolique
IDO1 se trouve au point d’entrée d’une voie métabolique qui dégrade l’acide aminé tryptophane en un produit appelé kynurénine. Lorsque IDO1 est abondant et actif, les niveaux de tryptophane chutent et la kynurénine augmente, créant un environnement chimique qui atténue l’activité des cellules immunitaires, y compris les lymphocytes T anti-tumeur. Une forte activité d’IDO1 a été associée non seulement à une immunité antitumorale affaiblie, mais aussi à des lymphomes d’origine virale et à certaines formes de neurodégénérescence. Les développeurs de médicaments se sont donc concentrés sur le blocage de l’activité enzymatique d’IDO1, dans l’espoir de couper ce signal immunosuppresseur et d’améliorer l’efficacité des immunothérapies contre le cancer.
Pourquoi les simples inhibiteurs enzymatiques ont montré leurs limites
Malgré des résultats prometteurs chez l’animal, les essais cliniques des inhibiteurs traditionnels d’IDO1 ont été décevants. Une explication émergente est qu’IDO1 n’est pas qu’un simple catalyseur. Même quand sa chimie est bloquée, la protéine elle-même peut agir comme un centre de signalisation qui favorise encore la croissance et la dissémination tumorales. Certains inhibiteurs stabilisent même IDO1, augmentant la quantité de protéine présente dans les cellules. En d’autres termes, éteindre la fonction catalytique seule peut laisser intacts ses rôles pro‑tumoraux non enzymatiques — ou pire, les renforcer réellement.
Concevoir des composés qui déclenchent l’autodestruction
Les auteurs ont exploré une vaste bibliothèque de molécules « pseudo‑naturelles » — des composés synthétiques assemblés à partir de fragments inspirés de produits naturels mais recombinés de manière originale. Ils ont identifié une famille de molécules, baptisée iDegs, dérivée d’un bloc de construction d’origine végétale appelé (−)-myrtanol. Ces composés se lient à l’intérieur de la poche habituelle d’IDO1 pour son cofacteur contenant du fer, l’hème. En délogeant l’hème, les iDegs affaiblissent à la fois la capacité d’IDO1 à produire de la kynurénine et, surtout, remodelent une partie de la région C‑terminale de la protéine. Des structures cristallographiques à haute résolution montrent que lorsque les iDegs occupent le site de l’hème, ils assouplissent et désordonnent partiellement une hélice C‑terminale normalement maintenue dans une conformation compacte et protégée.
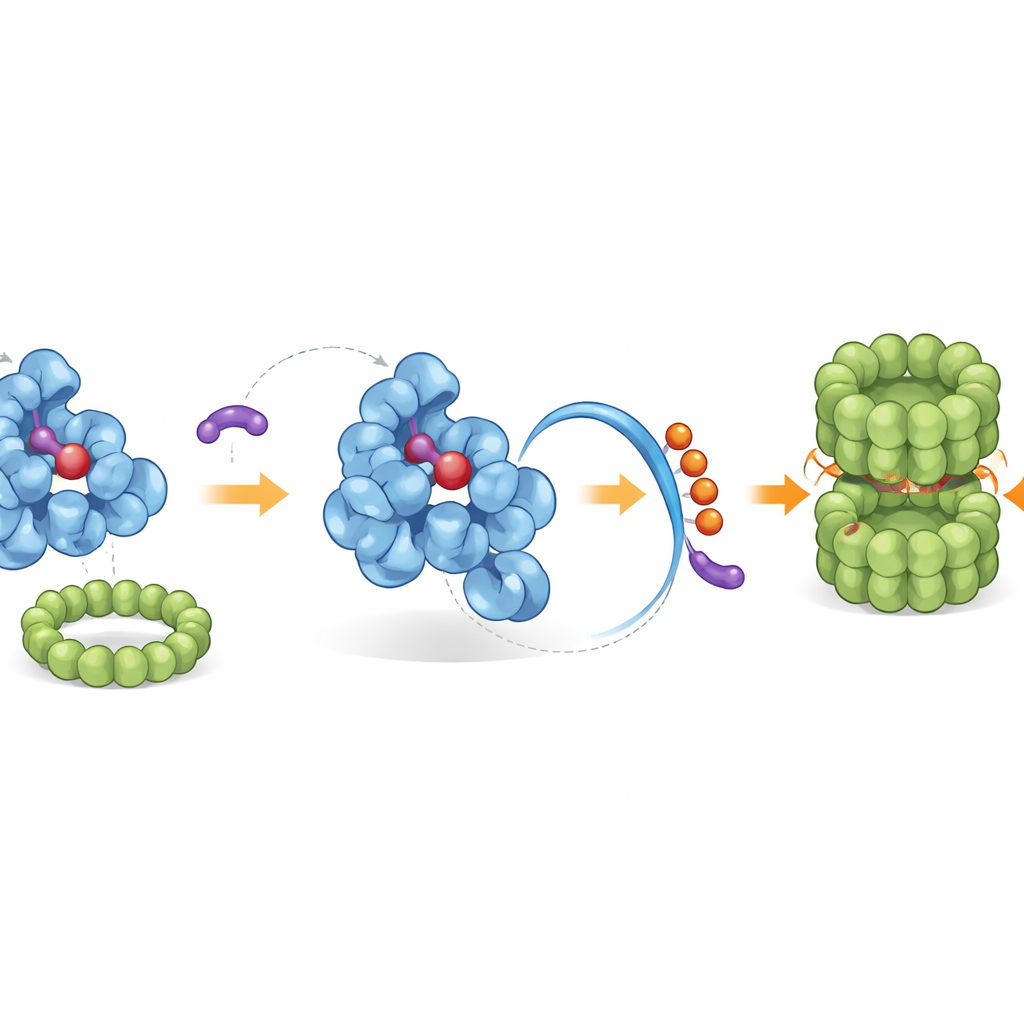
Recruter l’équipe de nettoyage natif de la cellule
La queue reconfigurée expose une « étiquette de fin » intégrée que la machinerie d’élimination cellulaire reconnaît. Grâce à des cribles génétiques et à la reconstitution biochimique, les chercheurs ont identifié un complexe de ligase spécifique, nommé CRL2–KLHDC3, qui attache naturellement de petites « marques » d’ubiquitine à la queue exposée d’IDO1, le ciblant pour destruction par le protéasome — le destructeur moléculaire de la cellule. Dans des conditions normales, seule la forme d’IDO1 dépourvue d’hème est efficacement marquée de cette manière, tandis que l’IDO1 liée à l’hème est protégée. Les iDegs font basculer cet équilibre en se liant uniquement à la forme sans hème, amplifiant ainsi la voie naturelle de dégradation. Les membres puissants de la série bloquent non seulement la production de kynurénine, mais augmentent aussi fortement le marquage par l’ubiquitine d’IDO1 et réduisent nettement ses niveaux protéiques dans plusieurs types cellulaires cancéreux.
Modifier le destin d’IDO1 — et les réponses immunitaires
Ce comportement à double action a des conséquences fonctionnelles importantes. Dans des essais de migration avec des cellules de cancer de l’ovaire, un inhibiteur d’IDO1 exploré cliniquement et qui stabilise l’enzyme a en réalité accéléré le mouvement cellulaire, en accord avec le rôle non enzymatique pro‑tumoral d’IDO1. En revanche, un composé iDeg a ralenti la migration, cohérent à la fois avec l’inhibition enzymatique et la perte de la protéine elle‑même. L’étude révèle donc une nouvelle façon de manipuler IDO1 : non pas en le forçant vers une ligase étrangère avec une grosse molécule conçue, mais en « suralimentant » une voie de dégradation native qui existe déjà dans les cellules.
Ce que cela pourrait signifier pour les thérapies anticancéreuses futures
Pour les non‑spécialistes, le message clé est que la qualité — pas seulement la quantité — de l’inhibition enzymatique compte. Ces nouvelles petites molécules agissent comme des interrupteurs de précision : elles verrouillent IDO1 dans une conformation vulnérable que la cellule est prête à détruire, coupant à la fois ses contributions métaboliques et ses fonctions de signalisation au profit de la survie tumorale. Parce que les iDegs sont compacts, de type médicament et s’appuient sur la ligase propre à la cellule pour l’élimination d’IDO1, ils pourraient offrir une approche plus subtile et plus largement applicable que les anciens médicaments « dégradeurs de protéines ». Si des stratégies similaires peuvent être appliquées à d’autres protéines problématiques, ce travail laisse entrevoir une nouvelle génération de thérapies qui incitent les cellules malades à démanteler leurs propres armes moléculaires.
Citation: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Mots-clés: IDO1, immunothérapie du cancer, dégradation ciblée des protéines, ligase ubiquitine, dégradeurs de petites molécules