Clear Sky Science · fr
Équilibrage biocompatible des ligands en coordination des métaux de transition permettant une arylation protéique in vivo sans danger
Transformer les métaux en outils doux pour la cellule
De nombreuses réactions chimiques puissantes reposent sur des métaux, mais les approcher de cellules vivantes cause généralement des problèmes : dommages, stress et mort cellulaire. Cette étude montre qu’avec « la bonne » enveloppe moléculaire autour d’un atome de nickel, il est possible d’exécuter une réaction sophistiquée à l’intérieur de cellules vivantes sans les endommager. Cette avancée permet aux scientifiques de marquer des milliers de sites spécifiques sur des protéines et même de suivre l’apparition d’agents pathogènes difficiles à repérer, ouvrant de nouvelles voies pour cartographier ce qui se passe réellement dans les cellules en santé et en maladie.
Pourquoi les métaux sont à la fois amis et ennemis
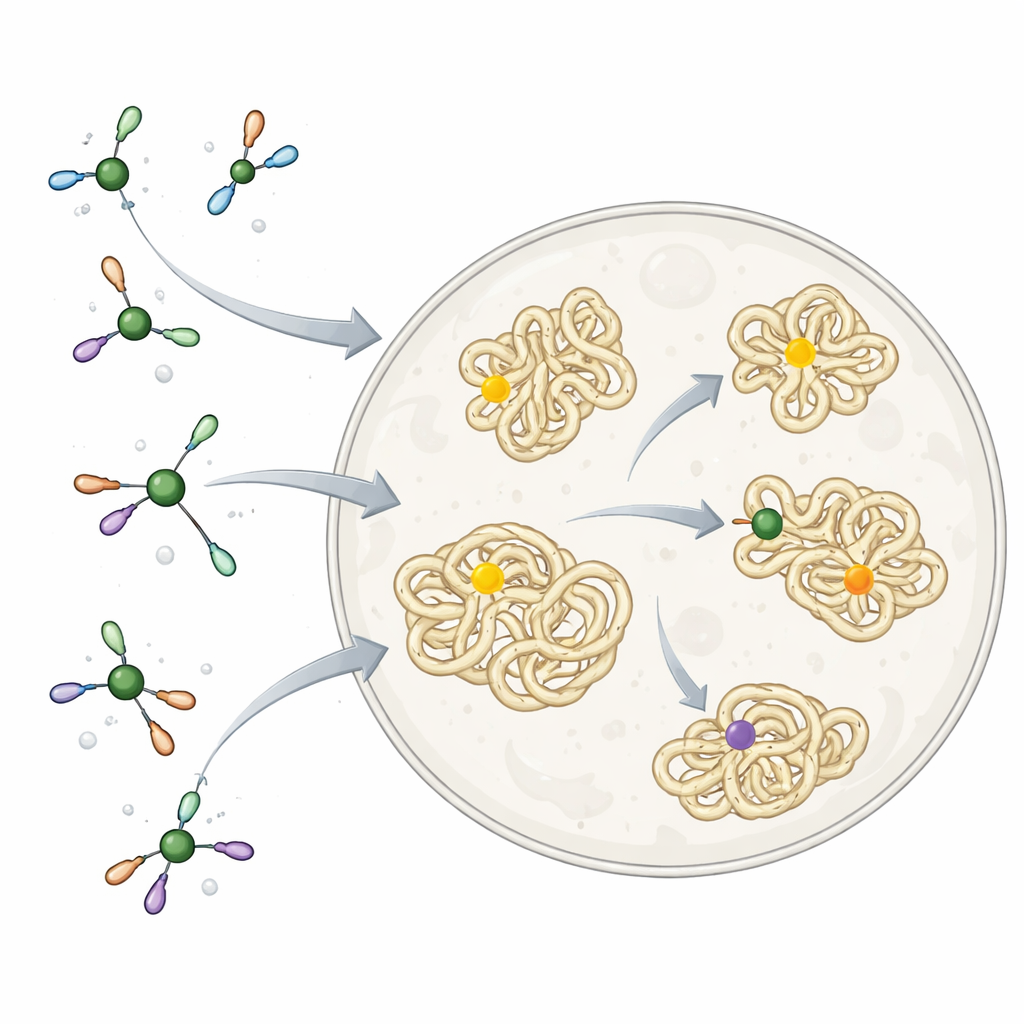
Le nickel et d’autres métaux agissent déjà discrètement dans notre organisme au sein d’enzymes naturelles, mais ils peuvent aussi être toxiques s’ils se lient au mauvais endroit. La nature résout ce problème en entourant les métaux de petites molécules et de protéines soigneusement sélectionnées, qui les dirigent vers les bonnes cibles et empêchent les réactions indésirables. Les chimistes, en revanche, utilisent souvent des réactifs métalliques extrêmement réactifs et peu adaptés au vivant. Ces réactifs sont d’excellents outils pour assembler des molécules complexes en éprouvette, mais bien trop agressifs pour être utilisés librement à l’intérieur des cellules, surtout lorsque l’objectif est d’ajouter un petit « étiquette » à un acide aminé précis d’une protéine sans perturber le reste de la cellule.
Concevoir un réactif au nickel plus doux
Les auteurs se sont inspirés de la façon dont les cellules gèrent elles‑mêmes le nickel. Ils ont synthétisé une série de complexes de nickel enveloppés d’un ligand simple et biocompatible appelé TMEDA. Cette petite molécule agit comme une pince souple : assez serrée pour empêcher le nickel de se lier aux mauvais composants cellulaires, mais assez lâche pour lui permettre d’effectuer la réaction clé. La réaction joint un fragment aryle — un groupe plat en anneau courant dans les médicaments — à l’atome de soufre de l’acide aminé cystéine dans les protéines. Sur des protéines purifiées en solution, ces complexes de nickel ont très rapidement et sélectivement fixé des groupes aryles sur des sites cystéine uniques, et ils ont fonctionné sur de nombreuses formes et positions protéiques, montrant que la chimie était largement compatible avec des molécules biologiques réelles.
Modifier des protéines à l’intérieur de cellules vivantes
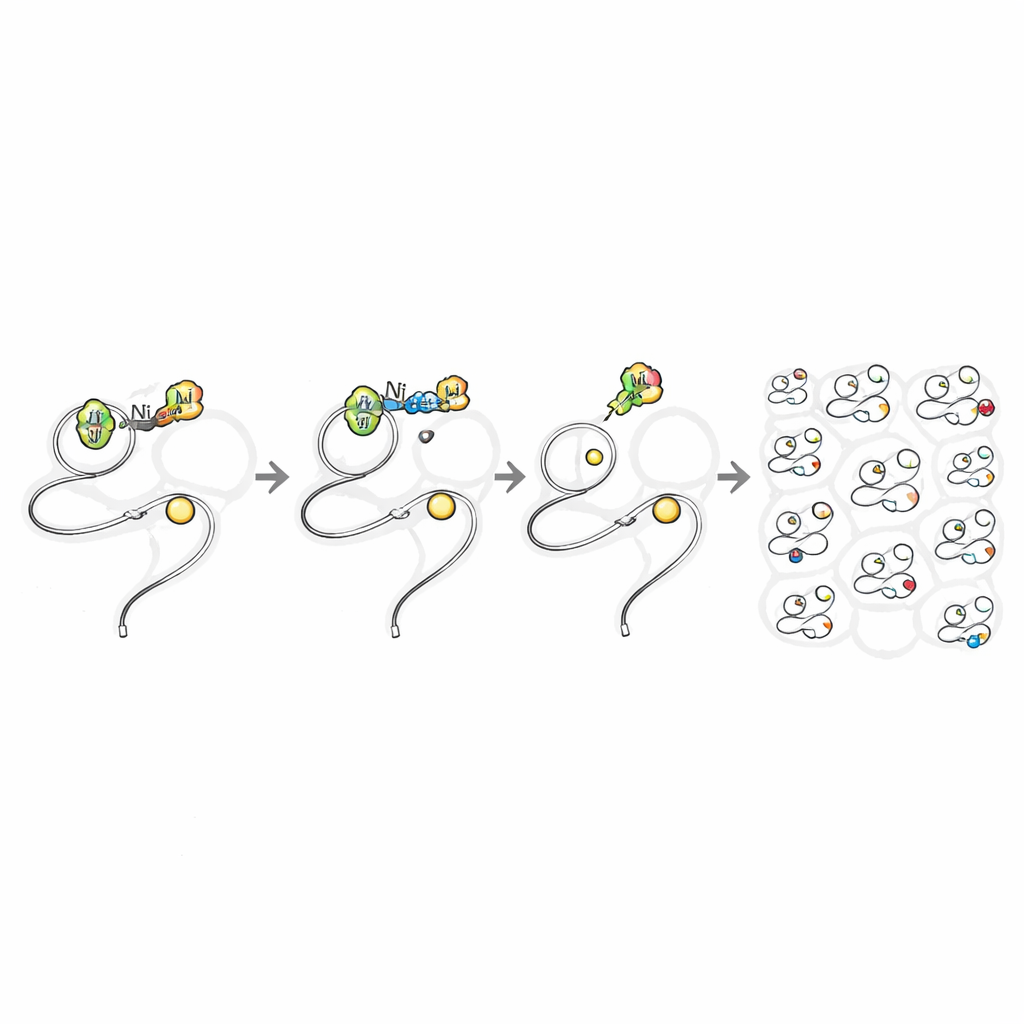
Les chercheurs ont ensuite testé si ces mêmes réactifs pouvaient fonctionner à l’intérieur de cellules vivantes sans être toxiques. Ils ont comparé des sels de nickel simples, connus pour être nocifs, avec les complexes de nickel liés au TMEDA. Dans des cellules de mammifères, les sources de nickel « nues » provoquaient une mortalité cellulaire importante à des doses relativement faibles, alors que les complexes équilibrés par ligand restaient bien tolérés même à des concentrations millimolaires. Cette fenêtre de sécurité a permis aux chercheurs d’immerger des cellules bactériennes et de mammifères dans les réactifs au nickel suffisamment longtemps pour qu’ils pénètrent et modifient des protéines. En incorporant une « poignée » azide dans une version du groupe aryle, ils ont pu cliquer des colorants fluorescents ou des étiquettes biotine après la réaction, révélant un marquage net des protéines dans le cytoplasme et le noyau des cellules vivantes dépendant de la dose.
Cartographier les sites protéiques réactifs à l’échelle du protéome
Avec une réaction in vivo sûre et rapide en main, les auteurs l’ont transformée en outil de découverte. Ils ont traité des cellules humaines vivantes avec le réactif au nickel porteur d’azide, puis utilisé une étiquette biotine photodégradable et une spectrométrie de masse avancée pour identifier précisément quelles cystéines avaient été modifiées. Lors d’une seule expérience, ils ont détecté près de 11 000 sites de cystéine répartis sur presque 5 000 protéines — environ deux fois plus de protéines que l’ensemble des études précédentes de profilage des cystéines en cellules vivantes. Le marquage était hautement sélectif pour la cystéine et montrait peu de biais pour des types de protéines, des localisations ou des sites actifs connus particuliers. Remarquablement, de nombreuses protéines ciblées étaient considérées comme « non ligandables » selon les standards actuels de découverte de médicaments, y compris des protéines de signalisation de faible abondance et des commutateurs redox sensibles difficiles à étudier uniquement par génétique.
Suivre des agents pathogènes cachés en temps réel
La même chimie s’est également avérée suffisamment sensible pour détecter des protéines étrangères produites lors d’infections. Dans des cellules humaines portant des séquences virales latentes, la méthode a détecté des facteurs de transcription viraux présents à des niveaux extrêmement faibles, y compris des formes issues d’épissages alternatifs. L’équipe a ensuite infecté des cellules avec deux agents pathogènes très différents : la bactérie intracellulaire Chlamydia trachomatis et le virus Sindbis, un virus à ARN apparenté au chikungunya. En traitant brièvement les cellules infectées avec le réactif au nickel à différents moments, ils ont pu piéger des sites cystéine sur des protéines ribosomales et régulatrices bactériennes clés au fur et à mesure que la bactérie changeait de stade du cycle de vie, et sur des protéines virales non structurales critiques qui pilotent la réplication de l’ARN. Ces sites marqués ressortent désormais comme des points faibles potentiels pour de futures stratégies antivirales ou antibactériennes.
Ce que cela signifie pour la chimie cellulaire future
En équilibrant soigneusement la couche de ligands autour du nickel, ce travail montre qu’un métal traditionnellement risqué peut réaliser une réaction covalente précise d’édition protéique profondément à l’intérieur de cellules vivantes avec un dommage minimal. Cela permet de dresser une carte fonctionnelle détaillée des sites cystéine réactifs à l’échelle du protéome, y compris pour des protéines rares, transitoires ou difficiles à cibler par des médicaments. Cela offre également un moyen de suivre et d’explorer les agents pathogènes dans leurs cellules hôtes au niveau d’acides aminés individuels. Plus largement, l’étude suggère que de nombreuses autres chimiothérapies « interdites » par le passé pourraient être domptées de manière similaire, ouvrant une nouvelle ère où les puissants outils de la chimie synthétique opèrent en sécurité à l’intérieur des systèmes vivants.
Citation: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Mots-clés: profilage de la cystéine, bioconjugaison au nickel, marquage des protéines en cellules vivantes, chimio-protéomique, cartographie des protéomes des agents pathogènes