Clear Sky Science · fr
La traduction locale spécifique aux ARNm est modelée par des condensats pour la croissance des cellules multinucléées
Comment les grandes cellules synchronisent des tâches éloignées
Les cellules de nos organismes sont généralement de petites unités autonomes contenant un seul noyau. Mais certains êtres vivants, notamment certains champignons et cellules musculaires, forment de vastes compartiments remplis de nombreux noyaux partageant le même cytoplasme. Dans ces géantes, les signaux et les molécules mettent du temps à diffuser d’un point à un autre, posant une question : comment coordonnent-elles croissance et division sur de telles distances sans perdre le contrôle ? Cette étude aborde la question dans un champignon multinucléé en révélant comment de petites gouttelettes à l’intérieur de la cellule ajustent localement la production protéique là où elle est nécessaire.
De minuscules gouttelettes qui organisent une cellule géante
Chez le champignon filamenteux Ashbya gossypii, de longs tubes appelés hyphes contiennent de nombreux noyaux qui se divisent de façon asynchrone tandis que la croissance se concentre principalement aux extrémités. Des travaux antérieurs ont montré qu’une protéine nommée Whi3 forme des gouttelettes microscopiques, ou condensats, avec des ARN messagers (ARNm) spécifiques codant des régulateurs clés du cycle cellulaire et de la croissance des pointes. Ici, les auteurs cherchent à comprendre la fonction réelle de ces condensats. Grâce à une imagerie 3D rapide, ils ont montré que les condensats à base de Whi3 varient en taille et en nombre selon leur position dans la cellule et selon l’état local de croissance et de division nucléaire. De gros condensats s’agrègent près des pointes hyphales à croissance lente, tandis que des condensats plus petits et plus variables entourent des noyaux à des stades particuliers du cycle. Des mutants incapables de former des condensats normaux présentent une croissance accélérée des pointes et des divisions nucléaires plus synchrones, suggérant que les propriétés des condensats contribuent à coordonner ces processus.
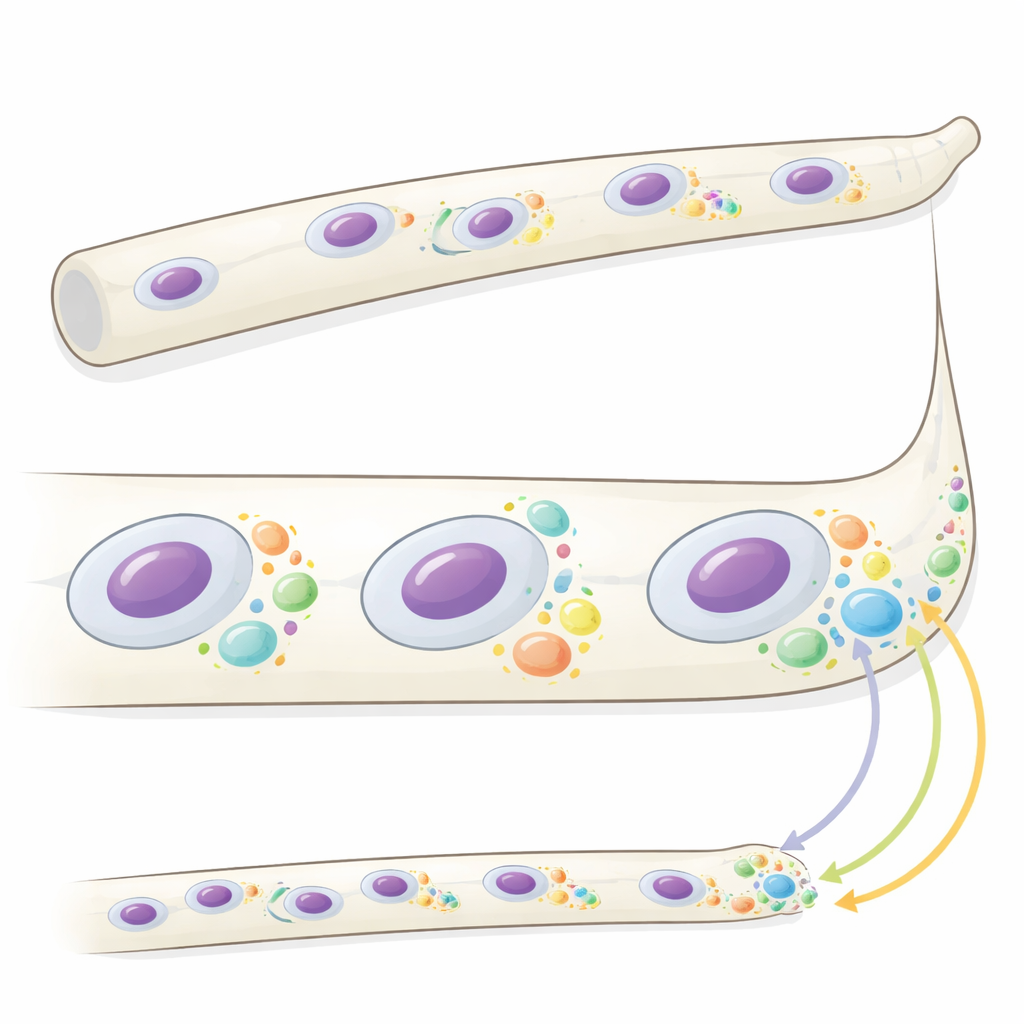
La production protéique locale écrite dans l’espace et le temps
Pour savoir si les condensats Whi3 contrôlent le lieu de synthèse des protéines, l’équipe a mesuré la traduction — le processus par lequel l’ARNm est converti en protéine — pour deux ARNm importants liés à Whi3. Le premier, CLN3, code une cycline qui aide à faire progresser le cycle de division ; le second, BNI1, code un facteur qui façonne la croissance à la pointe hyphale. En utilisant une méthode fluorescente sensible détectant les ribosomes actifs sur chaque ARNm endogène, les chercheurs ont montré que CLN3 est traduit principalement près de certains noyaux et seulement pendant des phases spécifiques de leur cycle, notamment autour des noyaux en mitose. L’ARNm BNI1 s’accumule aux pointes hyphales, mais sa traduction y est généralement peu fréquente et variable. Lorsque le comportement de Whi3 est modifié par une mutation mimant la phosphorylation, la traduction de BNI1 devient fortement enrichie aux pointes et la croissance des pointes s’accélère, révélant que Whi3 peut soit réprimer soit permettre la traduction selon son état et sa localisation.
Composants minimaux, sorties multiples
Pour tester si cet ajustement est une propriété intrinsèque des composants du condensat, les auteurs ont recréé le système dans des extraits cellulaires sans cellules. Ils ont rattaché un rapporteur luciférase aux régions régulatrices des ARNm CLN3 ou BNI1 et mélangé ces ARNm avec la protéine Whi3 purifiée à différentes concentrations. À faibles niveaux, sans formation de gouttelettes, la traduction changeait peu. À des niveaux plus élevés favorisant la formation de condensats, la traduction liée à CLN3 était fortement réprimée lorsque la concentration de Whi3 et la taille des condensats augmentaient. BNI1 se comportait différemment : des niveaux modérés de condensats augmentaient sa traduction, tandis que des condensats plus abondants ou plus volumineux basculaient le système vers la répression. Des versions mutantes de Whi3 formant des gouttelettes plus petites ou moins nombreuses, ou des ARNm avec moins de sites de liaison à Whi3, déplaçaient ces réponses, souvent en allégeant la répression et en augmentant la traduction. Ces expériences montrent que les mêmes ingrédients de base — Whi3, ses ARNm cibles et leurs condensats — peuvent produire un continuum d’états de traduction simplement en modifiant la concentration, la force d’interaction ou la taille des gouttelettes.
Où la traduction a lieu : à la périphérie de la gouttelette
Les essais en vrac moyennent le signal sur de nombreuses molécules et ne peuvent pas révéler où la traduction se déroule à l’intérieur ou autour des condensats. Pour le visualiser directement, l’équipe a utilisé un rapporteur « MoonTag » qui s’allume quand de nouvelles chaînes protéiques émergent des ribosomes. In vitro, ils ont observé des signaux MoonTag s’accumuler sur et à l’intérieur des gouttelettes Whi3–ARN, prouvant que ces condensats peuvent effectivement être des sites actifs de traduction et non de simples réservoirs. Fait remarquable, ribosomes et signaux de protéines naissantes étaient les plus intenses à l’interface de la gouttelette, formant un anneau lumineux autour de chaque condensat. Les condensats plus petits, offrant plus de surface relative par rapport au volume, soutenaient plus de traduction par ARNm que les gouttes plus grandes, qui étaient globalement plus répressives. Modifier la valence des ARNm ou l’état de charge de Whi3 déplaçait cette zone permissive de traduction vers la surface ou plus en profondeur, indiquant que des caractéristiques moléculaires subtiles du condensat règlent l’accès de la machinerie de traduction aux ARNm résidents.
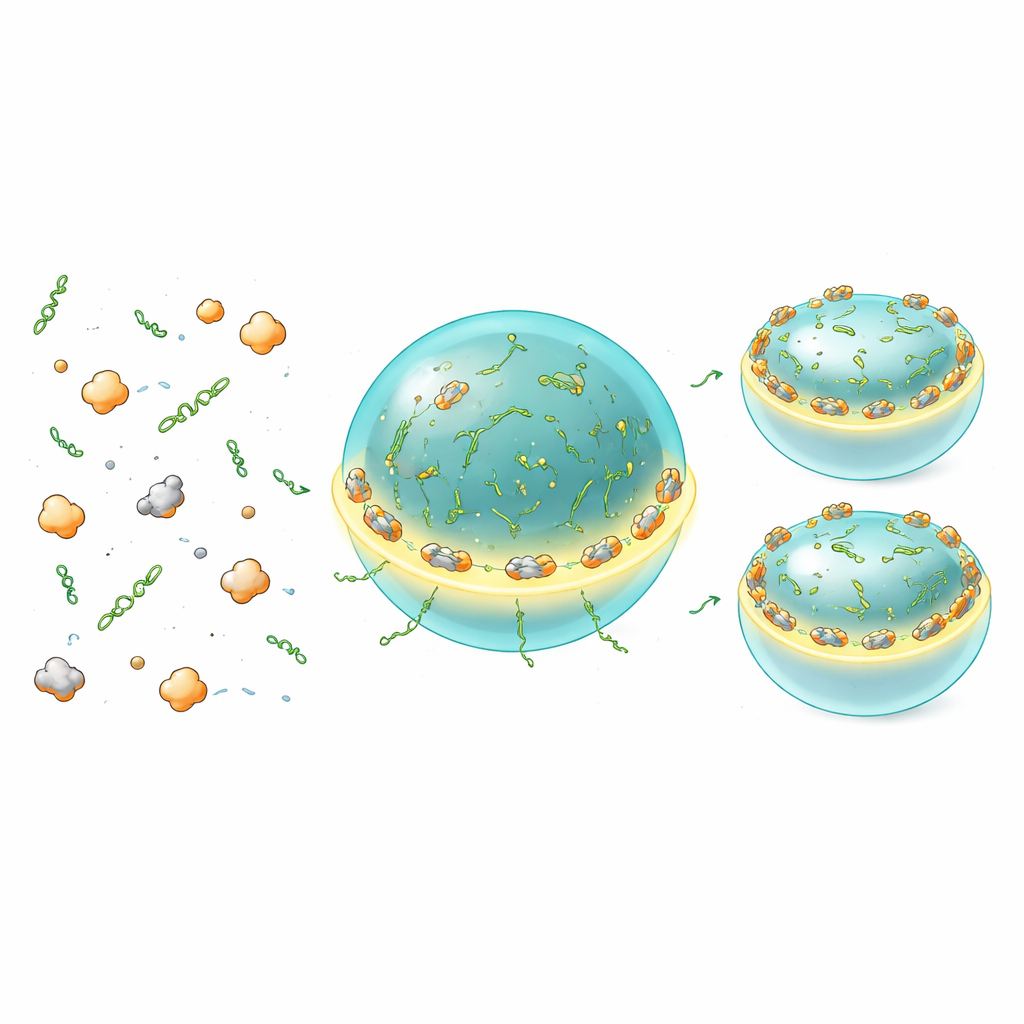
Dosages finement réglés pour une croissance équilibrée
Au total, ce travail présente les condensats Whi3–ARN comme des vannes ajustables qui délivrent localement des protéines plutôt que comme de simples interrupteurs tout-ou-rien. Chez le champignon, cela signifie que la cycline CLN3 peut être produite par pulsations autour de noyaux sélectionnés pour maintenir leurs cycles de division décalés, tandis que BNI1 peut être synthétisé par rafales intermittentes aux pointes hyphales pour soutenir la croissance sans permettre une expansion débridée en un seul point. Lorsque la formation ou les propriétés des condensats sont perturbées, ce contrôle nuancé disparaît : la production protéique devient plus uniforme dans l’espace et le temps, les noyaux se divisent de manière synchrone, les schémas de ramification changent et la morphologie générale est altérée. Pour un lecteur non spécialisé, le message clé est que les cellules peuvent utiliser de minuscules gouttelettes séparées par phase comme des réacteurs réglables spatialement et temporellement, permettant à de grandes cellules multinucléées de coordonner croissance et division sur de longues distances en sculptant localement quand et où les protéines sont produites.
Citation: Geisterfer, Z.M., Jalihal, A.P., Cole, S.J. et al. RNA-specific local translation is patterned by condensates for multinucleate cell growth. Nat Cell Biol 28, 507–519 (2026). https://doi.org/10.1038/s41556-026-01887-y
Mots-clés: condensats biomoléculaires, traduction locale, contrôle du cycle cellulaire, hyphes fongiques, ségrégation de phase