Clear Sky Science · fr
Ubitiquination sur la lysine-11 entraîne l'induction des interférons de type I/III par cGAS–STING et les récepteurs Toll-like 3 et 4
Comment nos cellules donnent l'alerte
Lorsque des virus ou des molécules dangereuses envahissent l'organisme, nos cellules doivent décider en quelques minutes si elles déclenchent de puissants signaux antiviraux appelés interférons. Ces signaux peuvent nous protéger contre des infections sévères — mais lorsqu'ils sont mal régulés, ils provoquent aussi des maladies auto-immunes délétères. Cette étude met au jour un « pupitre » moléculaire jusque-là caché à l'intérieur des cellules qui aide à décider quand activer les réponses à l'interféron et quand les freiner. Comprendre ce pupitre offre des pistes pour améliorer les vaccins, les thérapies antivirales et les traitements des affections liées aux interférons.
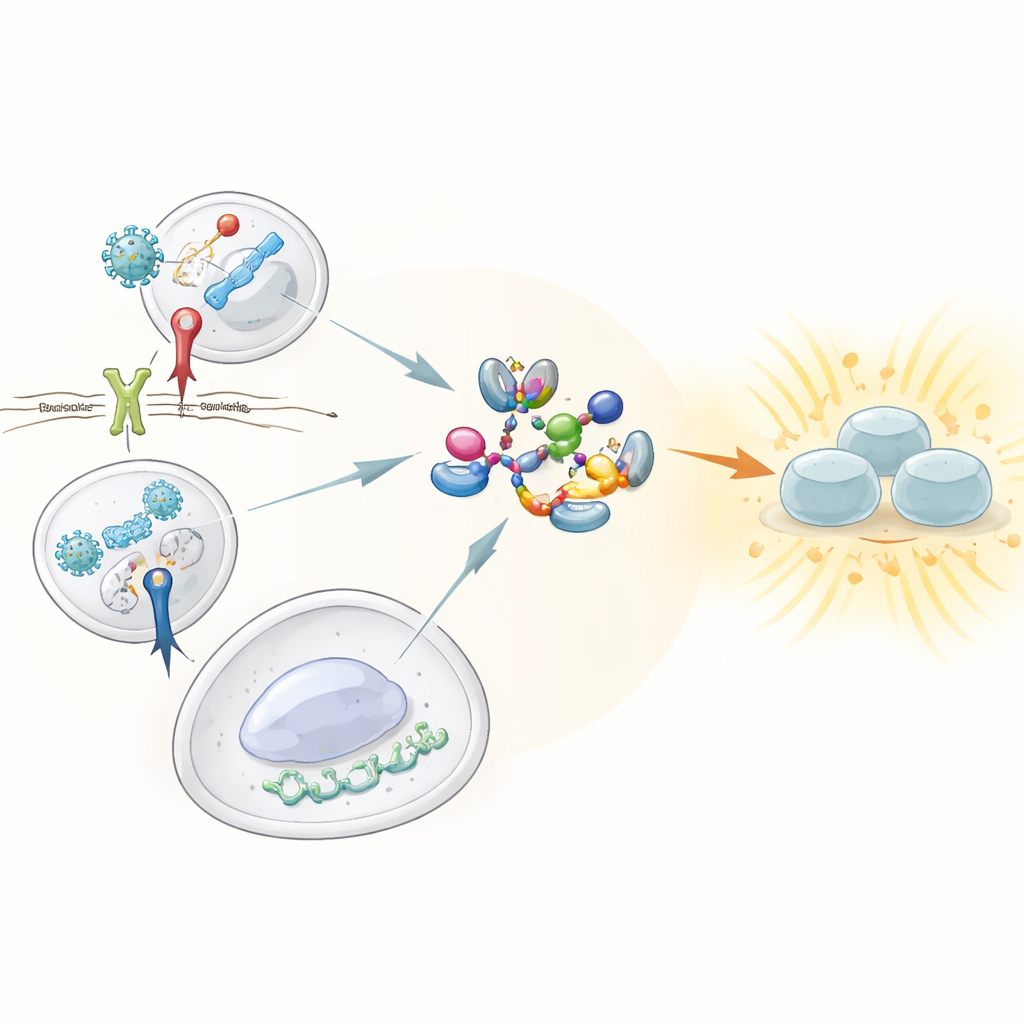
Les sentinelles qui détectent le danger
Notre système immunitaire inné repose sur des sentinelles appelées récepteurs de reconnaissance de motifs, qui patrouillent à la recherche des signatures caractéristiques des virus et des bactéries. Parmi eux, trois se distinguent par leur capacité à déclencher de fortes réponses en interférons : le récepteur Toll-like 3 (TLR3), qui détecte l'ARN viral double brin ; le récepteur Toll-like 4 (TLR4), qui repère un composant des parois bactériennes ; et la voie cGAS–STING, qui détecte l'ADN étranger au mauvais endroit dans la cellule. Les trois doivent activer une enzyme centrale, TBK1, qui à son tour active le facteur de transcription IRF3 pour induire la production d'interférons de type I et III. Jusqu'à présent, on ne comprenait pas bien comment ces senseurs convergeaient vers TBK1 pour le mettre en état actif.
Un connecteur moléculaire caché
Les chercheurs ont découvert qu'une protéine nommée ANKIB1 agit comme un connecteur crucial entre ces senseurs et TBK1. ANKIB1 est une enzyme qui attache de petites étiquettes moléculaires, appelées chaînes d'ubiquitine, à d'autres protéines. De manière importante, elle construit un type spécifique de chaîne, fondé sur une liaison dite « K11 », connue jusqu'alors surtout pour des rôles dans la division cellulaire plutôt que dans l'immunité. Dans des cellules humaines dépourvues d'ANKIB1, la stimulation de TLR3 ou l'activation de STING n'entraînaient plus une activation correcte de TBK1 et d'IRF3, et les gènes d'interféron s'exprimaient à peine. La restauration d'ANKIB1 rétablit la réponse, montrant que cette seule enzyme est à la fois nécessaire et suffisante pour piloter cette branche de l'alarme antivirale.
Construire une plateforme d'amarrage pour des protéines relais
Un examen plus approfondi a révélé comment ANKIB1 exerce son influence. Lorsque TLR3 ou STING détectent un danger, ils assemblent des plateformes multiprotéiques appelées signalosomes. ANKIB1 est recruté sur ces plateformes via une région qui reconnaît l'ubiquitine. Une fois présent, il décore plusieurs composants clés — y compris les protéines adaptatrices TRIF et STING elles-mêmes, ainsi que d'autres molécules de signalisation — avec des chaînes d'ubiquitine liées en K11. Ces chaînes ne marquent pas simplement les protéines pour leur destruction ; elles agissent plutôt comme un Velcro moléculaire. Une autre protéine, Optineurine (OPTN), est attirée spécifiquement vers ces sites modifiés. Servant d'adaptateur relais, OPTN amène alors TBK1 dans le complexe afin qu'il puisse être activé et transmettre le signal à IRF3 et aux gènes d'interféron. Lorsqu'OPTN a été supprimée, l'activation de TBK1 s'effondra, soulignant que le marquage en K11 par ANKIB1 et la liaison d'OPTN forment un axe unique et essentiel.
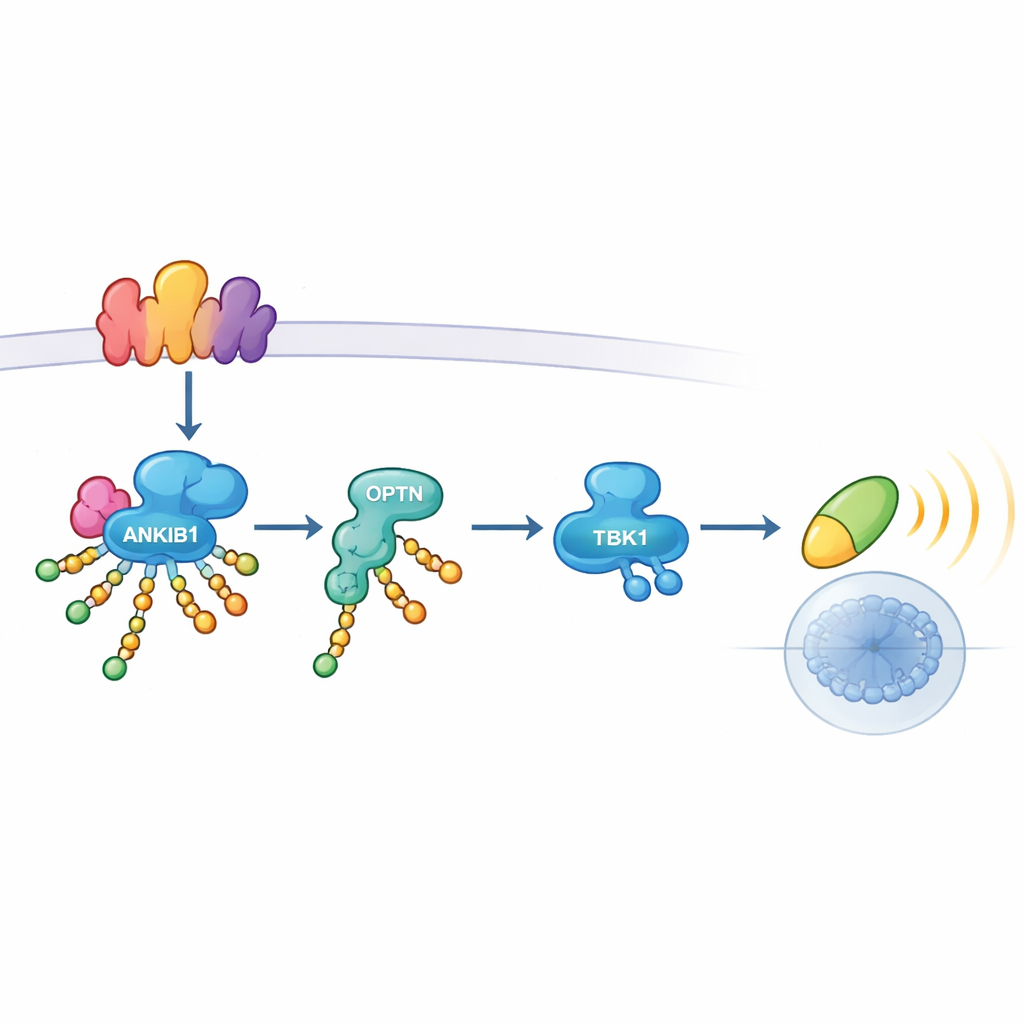
Quand cette voie compte — et quand elle ne compte pas
L'équipe a ensuite cherché à savoir si ce mécanisme était universel à tous les senseurs antiviraux. Ils ont constaté qu'ANKIB1 est vital pour l'induction d'interférons via TLR3, le bras dépendant de TRIF de TLR4, et la voie cGAS–STING, qui utilisent toutes OPTN comme adaptateur principal vers TBK1. En revanche, un autre senseur, RIG-I, qui détecte l'ARN viral, s'appuie sur un ensemble différent de protéines adaptatrices et n'a pas besoin d'ANKIB1 ni d'OPTN pour activer TBK1. Des expériences chez la souris ont corroboré ces observations en cellules. Les animaux dépourvus d'Ankib1 produisaient beaucoup moins d'interféron après activation de TLR3 ou STING, étaient protégés contre un syndrome inflammatoire létal entraîné par les interférons, mais devenaient beaucoup plus vulnérables à l'infection par l'herpès simplex virus 1, un virus à ADN qui dépend fortement de l'interféron induit par cGAS–STING pour être contrôlé. Les réponses au virus de la grippe, principalement détecté par RIG-I, restaient en grande partie intactes.
Équilibrer protection et dommage
Ensemble, ces résultats révèlent que les chaînes d'ubiquitine liées en K11 générées par ANKIB1 constituent une monnaie centrale dans une branche majeure de la signalisation antivirale innée. En créant des sites d'amarrage pour OPTN, ANKIB1 aide à assembler le relais moléculaire précis qui transforme le danger détecté par TLR3, TLR4 (via TRIF) et cGAS–STING en une production robuste d'interférons. Cet axe est à double tranchant : il est essentiel pour la défense contre certains virus, mais alimente aussi les maladies inflammatoires liées aux interférons lorsqu'il est suractivé. Étant donné que l'activité catalytique d'ANKIB1 et des domaines spécifiques sont requis pour cette fonction, ils constituent des cibles attractives pour de futurs médicaments visant soit à atténuer des réponses nuisibles d'interféron dans les affections auto-immunes, soit à renforcer l'immunité antivirale lorsque celle-ci est insuffisante.
Citation: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Mots-clés: immunité innée, signalisation des interférons, ubiquitination, voie cGAS–STING, infection virale