Clear Sky Science · fr
Le tissu adipeux péri-tumoral favorise l’évasion immunitaire du cancer colorectal via une transformation adipeuse–mésenchymateuse
Pourquoi la graisse abdominale autour des tumeurs compte
Le cancer colorectal se développe dans la paroi de l’intestin, mais il est adjacent à un coussinet épais de graisse abdominale. La plupart des gens considèrent cette graisse comme un rembourrage passif. Cette étude révèle quelque chose de surprenant : la graisse entourant la tumeur peut discrètement détourner les cellules immunitaires combattant le cancer loin de la tumeur, aidant ainsi le cancer à se cacher du système immunitaire. Comprendre cette lutte silencieuse suggère de nouvelles façons de prédire qui répondra à l’immunothérapie et comment améliorer l’efficacité de ces traitements.
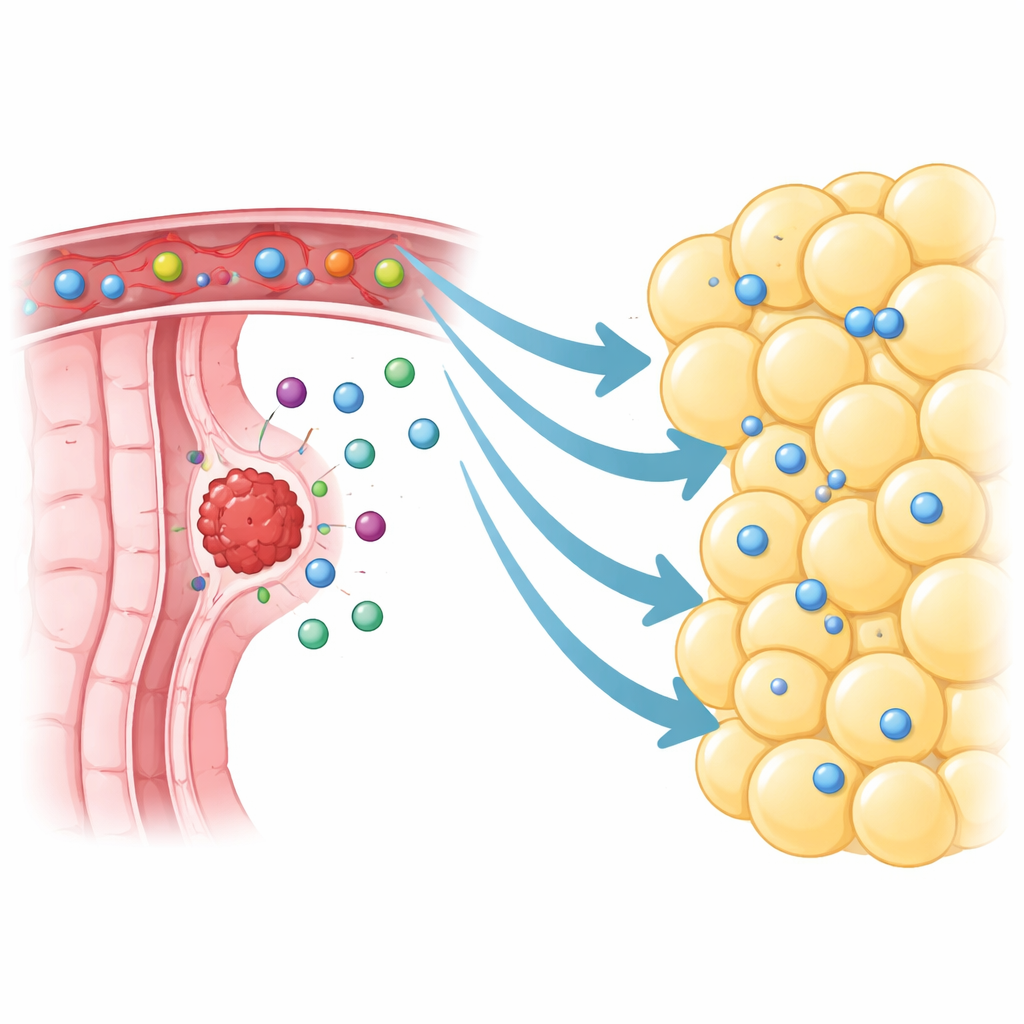
Un voisinage immunitaire animé à côté de la tumeur
Les chercheurs se sont concentrés sur la graisse viscérale entourant directement les tumeurs colorectales, appelée tissu adipeux pératumoral. Grâce au séquençage ARN unicellulaire, ils ont cartographié plus de 370 000 cellules individuelles provenant des tumeurs, de la graisse proche, de la graisse éloignée et des tissus normaux. Au lieu d’être silencieuse et inerte, la graisse proche des tumeurs foisonnait de cellules immunitaires, en particulier de lymphocytes T et B. Ils ont même trouvé des regroupements organisés ressemblant à de petits ganglions lymphatiques, signes que ce tissu peut héberger des réactions immunitaires actives. Comparée à la graisse prélevée plus loin, la graisse pératumorale contenait beaucoup plus de lymphocytes, notamment des lymphocytes mémoire et des lymphocytes T cytotoxiques spécifiques de la tumeur qui, en principe, devraient patrouiller contre le cancer.
Quand des cellules immunitaires utiles se retrouvent au mauvais endroit
Pour déterminer si cette graisse riche en cellules immunitaires aidait ou nuisait, l’équipe a utilisé des modèles murins où des tumeurs étaient implantées près d’un dépôt de graisse reproduisant la situation humaine. Ils ont ensuite retiré chirurgicalement cette graisse proche ou l’ont dissoute chimiquement. Contre-intuitivement, l’ablation de la graisse pératumorale a ralenti la croissance tumorale. Les tumeurs des souris ayant perdu cette graisse contenaient davantage de lymphocytes T CD4 et CD8, y compris des T reconnaissant des antigènes tumoraux. Des expériences supplémentaires suivant des cellules immunitaires donneuses ont montré que, lorsque la graisse était présente, nombre de ces cellules s’accumulaient dans le dépôt graisseux au lieu de la tumeur. Retirer la graisse a redirigé les cellules vers la tumeur, renforçant la réponse anti-tumorale. En d’autres termes, la graisse agissait comme un réservoir compétitif qui absorbait les cellules immunitaires et les empêchait d’atteindre leur véritable cible.
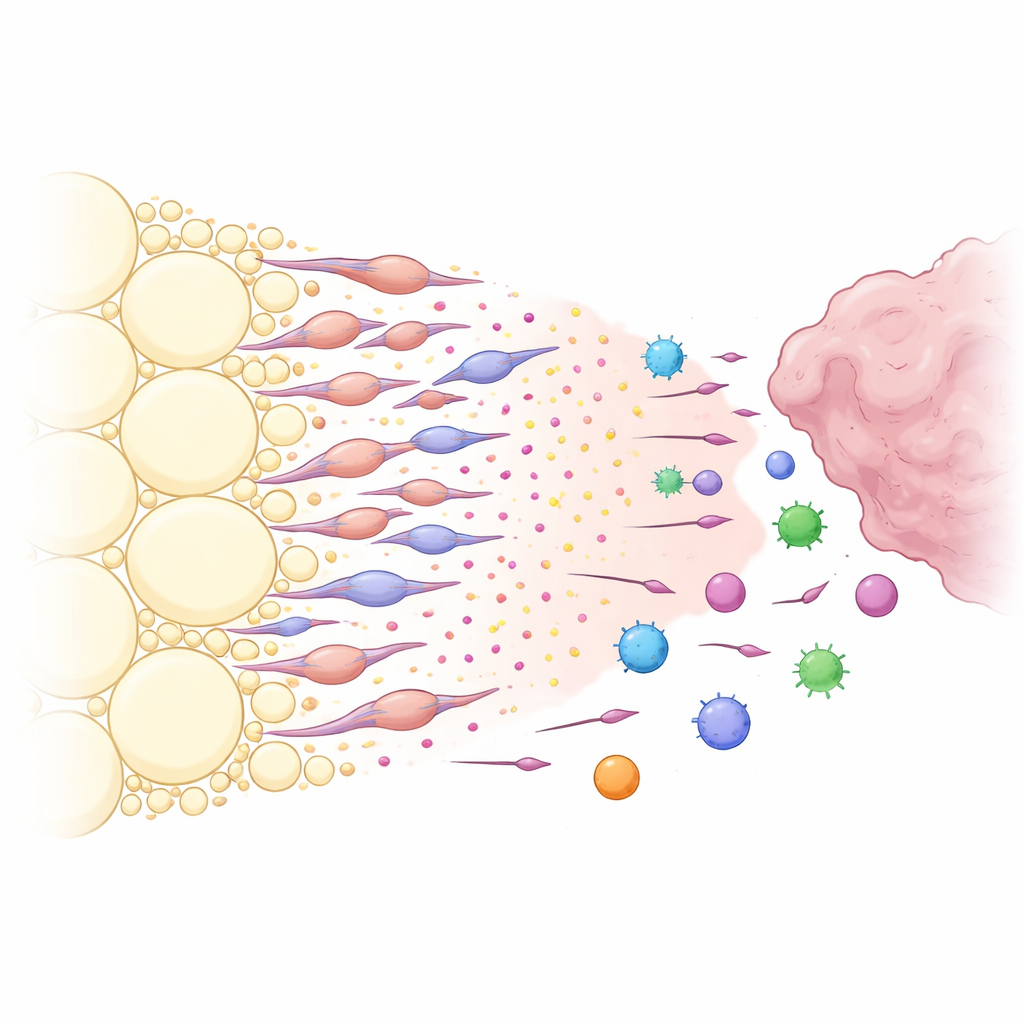
Un leurre chimique construit par des cellules adipeuses transformées
Qu’est-ce qui rendait la graisse pératumorale si efficace pour capturer les cellules immunitaires ? En analysant les signaux de communication entre types cellulaires, les chercheurs ont identifié une voie chimique puissante centrée sur la molécule CXCL12 et son récepteur CXCR4. Les cellules stromales dans la graisse proche de la tumeur produisaient de fortes quantités de CXCL12, tandis que de nombreuses cellules immunitaires exprimaient CXCR4, les rendant sensibles à ce signal. Bloquer localement CXCL12 dans la graisse, ou le supprimer génétiquement dans le stroma adipeux, a provoqué la réduction des tumeurs et a permis à davantage de cellules immunitaires CXCR4-positives de pénétrer dans la tumeur au lieu d’être détournées. L’équipe a ensuite découvert que les principaux producteurs de CXCL12 n’étaient pas des adipocytes ordinaires, mais un groupe spécial de cellules fibroblastiques dérivées du tissu adipeux qu’ils ont qualifiées de fibroblastes associés au cancer d’origine adipeuse. Des facteurs libérés par la tumeur, en particulier le facteur de croissance TGF-β1, ont poussé les cellules stromales adipeuses locales à se transformer en ces cellules de type fibroblastique, lesquelles sécrétaient alors de grandes quantités de CXCL12 et d’autres signaux favorisant la croissance.
Transformer un bouclier en point faible
Parce que ces cellules transformées contribuent à détourner les cellules immunitaires loin des tumeurs, les chercheurs ont testé si démanteler cet « puits immunitaire » pouvait améliorer l’immunothérapie. Chez des souris génétiquement modifiées de manière à pouvoir éliminer sélectivement ces fibroblastes associés au cancer d’origine adipeuse, le traitement par un anticorps bloquant PD-1 est devenu bien plus efficace : les tumeurs ont moins progressé, et davantage de lymphocytes T spécifiques de la tumeur et CXCR4-positifs ont infiltré le cancer. De même, des médicaments ou anticorps bloquant soit CXCL12 soit son récepteur CXCR4 ont agi en synergie avec le blocage de PD-1, dans des modèles de cancer colorectal sous-cutanés et orthotopiques. Ces combinaisons ont non seulement réduit la taille tumorale mais aussi remodelé le paysage immunitaire à l’intérieur de la tumeur.
Indices provenant des scans des patients et perspectives
L’équipe s’est ensuite demandé si leurs observations étaient pertinentes chez l’humain. Dans un groupe de patients atteints de cancer colorectal localement avancé recevant une chimiothérapie, une radiothérapie et une immunothérapie anti–PD-1 combinées, ceux ayant obtenu une réponse complète avaient tendance à présenter un volume plus faible de graisse viscérale pératumorale à l’IRM avant le traitement. Quantitativement, la surface de cette graisse prédisait la réponse thérapeutique mieux que certains marqueurs tissulaires standards, et les patients présentant de grands volumes de graisse pératumorale avaient des taux de réponse beaucoup plus faibles. Pour un non-spécialiste, la conclusion est frappante : non seulement la tumeur elle-même, mais aussi la graisse qui l’entoure immédiatement, peut déterminer l’efficacité de l’immunothérapie. En se concentrant sur cette graisse — soit en la mesurant pour guider les décisions thérapeutiques, soit en ciblant ses cellules stromales transformées et le signal CXCL12–CXCR4 — il pourrait être possible de transformer un bouclier protecteur de la tumeur en un point faible thérapeutique.
Citation: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Mots-clés: cancer colorectal, microenvironnement tumoral, graisse viscérale, immunothérapie, CXCL12 CXCR4