Clear Sky Science · fr
Le remodelage du RE est une caractéristique du vieillissement et dépend de l'ER-phagie
Pourquoi les replis internes de la cellule comptent avec l’âge
Les cellules de notre corps contiennent un réseau membranaire enchevêtré appelé réticulum endoplasmique, ou RE. Cette structure participe à la synthèse des lipides et des protéines, régule le sucre et le calcium, et communique en permanence avec d’autres compartiments cellulaires. Comme tant de fonctions vitales transitent par ce réseau, toute reconfiguration durable du RE pourrait influencer le vieillissement des tissus, leur résistance au stress et, en fin de compte, la durée de vie en bonne santé. Cette étude pose une question simple en apparence : le RE lui‑même vieillit‑il de manière spécifique et organisée, et, si oui, ce changement est‑il une usure nuisible ou une stratégie protectrice intégrée ?
Un changement discret sur l’établi cellulaire
À l’aide de microscopes avancés et de marqueurs fluorescents chez le petit ver Caenorhabditis elegans, les auteurs ont suivi le RE à l’intérieur d’animaux vivants alors qu’ils passaient de l’âge adulte jeune à l’âge avancé. Chez les cellules juvéniles, le RE forme de larges feuillets empilés, parsemés de machines de fabrication de protéines, évoquant des ateliers bien ordonnés. Avec l’âge, ces feuillets rétrécissent en volume et laissent place à un réseau plus fin et tubulaire qui occupe moins d’espace. Les mesures ont montré une baisse marquée de la quantité totale de RE parallèlement à ce changement de forme, ce qui indique non pas un dommage aléatoire mais un rétrécissement et une reconfiguration coordonnés de l’organite.
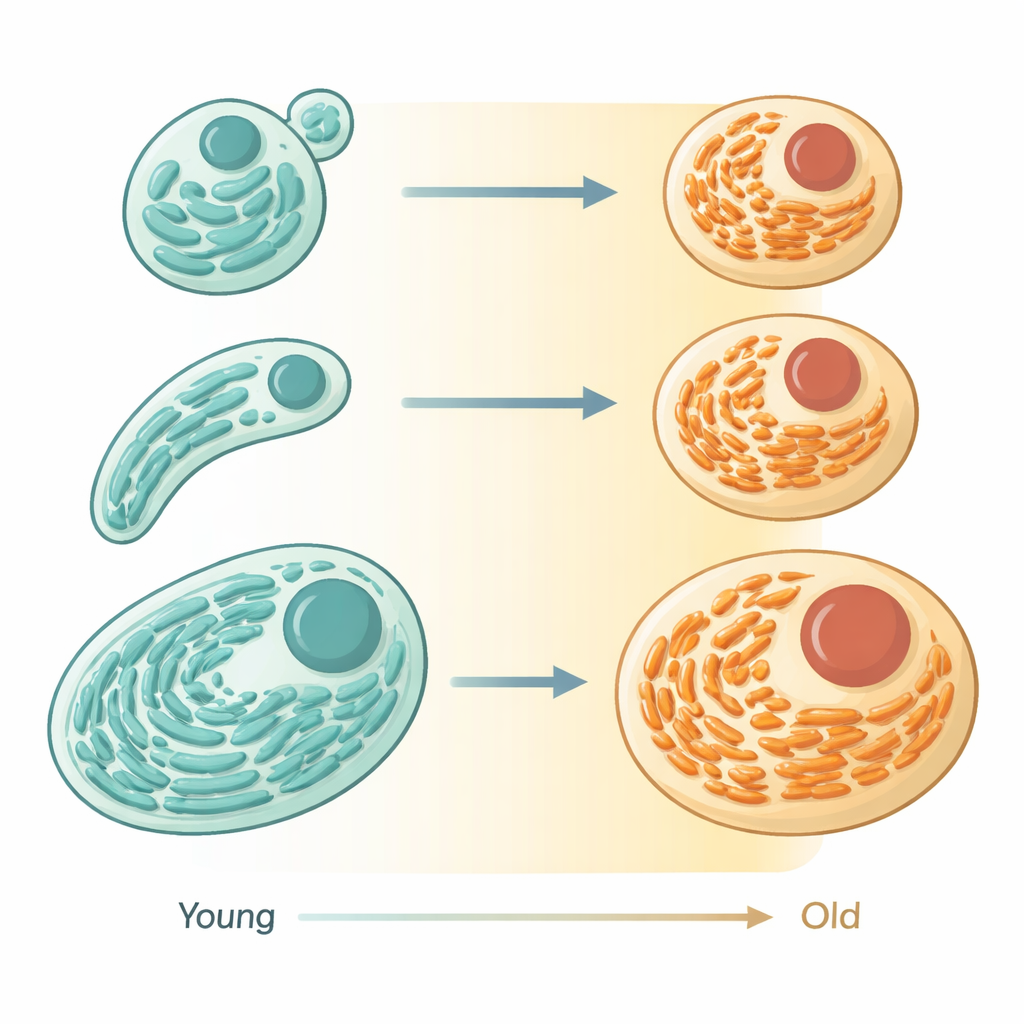
De la production de protéines à la gestion des lipides
La forme en biologie signale souvent la fonction, et cela se vérifie ici aussi. Les chercheurs ont comparé l’évolution des protéines liées au RE au fil du temps dans les tissus du ver. Les protéines impliquées dans la synthèse, le repliement et le contrôle qualité des protéines ont décliné avec l’âge, en parallèle avec la perte des feuillets. En revanche, de nombreuses protéines du RE impliquées dans le métabolisme des lipides et des membranes sont restées stables voire ont augmenté. Ensemble, ces tendances suggèrent que les cellules vieillissantes réduisent la production massive de protéines et réorientent les ressources du RE vers la gestion des lipides et des membranes. Fait marquant : en examinant de larges jeux de données de souris vieillissantes, les auteurs ont observé une histoire similaire : les protéines du RE dédiées à la sécrétion et au traitement des protéines ont tendance à diminuer, tandis que celles liées au métabolisme lipidique et à l’autophagie sont relativement préservées ou augmentées.
Une voie de recyclage cellulaire derrière le remodelage
Qu’est‑ce qui pilote cette refonte à grande échelle ? L’équipe a attribué les changements à l’ER‑phagie, une forme d’auto‑dégradation sélective dans laquelle la cellule empaquette des portions de RE dans des vésicules de recyclage pour leur dégradation dans les lysosomes. Le blocage de gènes centraux de l’autophagie chez le ver a empêché la perte normale de masse du RE liée à l’âge et le passage des feuillets aux tubules, montrant que cette voie de recyclage ne se contente pas de nettoyer des débris mais sculpte activement l’organite. Des expériences indépendantes chez la levure ont confirmé que des composantes du RE sont redirigées vers le centre de recyclage cellulaire au cours du vieillissement, là aussi de manière dépendante de l’autophagie. La microscopie électronique a révélé des fragments de RE à l’intérieur de compartiments dégradatifs, fournissant une preuve physique que des portions du réseau sont retirées de façon ciblée.

Un contrôle spécifique aux tissus d’un programme de vieillissement commun
Bien que le remodelage du RE ait été observé dans de nombreux tissus du ver — intestin, hypoderme (tissu cutané), muscle et neurones —, les déclencheurs se sont avérés spécifiques aux tissus. Dans l’hypoderme, une protéine membranaire auparavant peu connue, TMEM‑131, a relié le renouvellement du RE à la gestion du collagène. Lorsque TMEM‑131 était diminuée, la perte liée à l’âge du RE dans ce tissu était largement prévenue, ce qui implique que le RE est réduit quand ses « clients » collagènes diminuent. À l’inverse, dans l’intestin, le régulateur clé était le bras IRE‑1–XBP‑1 de la réponse aux protéines mal repliées, une voie centrale de détection du stress. L’inhibition de cette voie a préservé le RE intestinal pendant le vieillissement, suggérant que, dans cet organe, la signalisation de stress du RE contribue à décider quand des parties du RE doivent être sacrifiées.
Reconfigurer le RE pour une vie plus longue
L’étude relie également le remodelage du RE à la longévité. Chez le ver, plusieurs interventions bien connues prolongeant la vie — atténuation des signaux de type insuline, diminution de la détection nutritive mTOR, ablation de la lignée germinale ou léger ralentissement de la synthèse protéique — ont toutes induit un redimensionnement du RE et une augmentation des réseaux tubulaires tôt à l’âge adulte, plutôt que d’attendre la vieillesse. De manière importante, lorsque l’ER‑phagie était désactivée, les longues durées de vie normalement produites par l’inhibition de mTOR chez la levure et le ver étaient fortement réduites ou perdues. Cela indique qu’un élagage maîtrisé du RE n’est pas seulement un effet secondaire du vieillissement ou d’un traitement, mais constitue l’un des mécanismes par lesquels les cellules atteignent un état plus durable.
Ce que cela signifie pour un vieillissement en bonne santé
Pour un observateur non spécialiste, perdre une fraction substantielle d’une structure cellulaire clé durant le vieillissement peut sembler purement néfaste. Ce travail brosse un tableau plus nuancé. Le RE semble être activement remodelé — via l’auto‑dégradation sélective et des régulateurs adaptés aux tissus — de sorte que les cellules vieillissantes produisent moins de protéines nouvelles, investissent davantage dans la gestion des lipides et des membranes et réduisent possiblement le risque de stress chronique. Ce remodelage paraît conservé de la levure aux mammifères et est requis pour au moins certaines formes d’extension de la durée de vie. À long terme toutefois, la réduction du RE peut entraîner des compromis, influençant la capacité des cellules à réparer d’autres organites et à gérer le déclin tardif. En révélant l’ER‑phagie et la dynamique du RE comme des traits centraux du vieillissement normal et retardé, cette recherche met en lumière une nouvelle série de leviers qui pourraient un jour être modulés pour favoriser des tissus plus sains et résilients.
Citation: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Mots-clés: réticulum endoplasmique, autophagie, vieillissement cellulaire, homéostasie des protéines, métabolisme des lipides