Clear Sky Science · fr
Génomique fonctionnelle résolue dans le temps via l’apprentissage profond révèle un contrôle hiérarchique global de l’autophagie
Comment les cellules se recyclent — et savent quand s’arrêter
Nos cellules traversent les périodes difficiles en recyclant leurs propres éléments par un processus appelé autophagie — littéralement « s’auto‑manger ». Trop peu de recyclage, et les composants endommagés s’accumulent ; trop, et la cellule se cannibalise. Cette étude pose une question apparemment simple mais aux grandes implications pour le vieillissement et la maladie : comment une cellule vivante active et désactive-t‑elle l’autophagie aux bons moments, à mesure que les nutriments baissent et remontent ?
Suivre des milliers de cellules lors d’un cycle abondance‑jeûne
Pour répondre à cela, les chercheurs ont utilisé la levure de boulanger comme modèle et ont observé près de six mille souches mutantes différentes pendant des épisodes de privation et de récupération. Chaque souche de levure portait des marqueurs fluorescents indiquant des structures impliquées dans l’autophagie, permettant à un microscope puissant de capturer des images toutes les heures pendant la suppression puis la restauration des nutriments. Plutôt que de trier manuellement ces images, l’équipe a entraîné des algorithmes d’apprentissage profond à reconnaître quand une cellule était en état d’autophagie, uniquement à partir des caractéristiques d’image et non du jugement humain. Cela a produit des séries temporelles précises de l’activité autophagique pour presque tout le génome de la levure, révélant la rapidité et l’intensité de la réponse de chaque mutant aux fluctuations de nutriments. 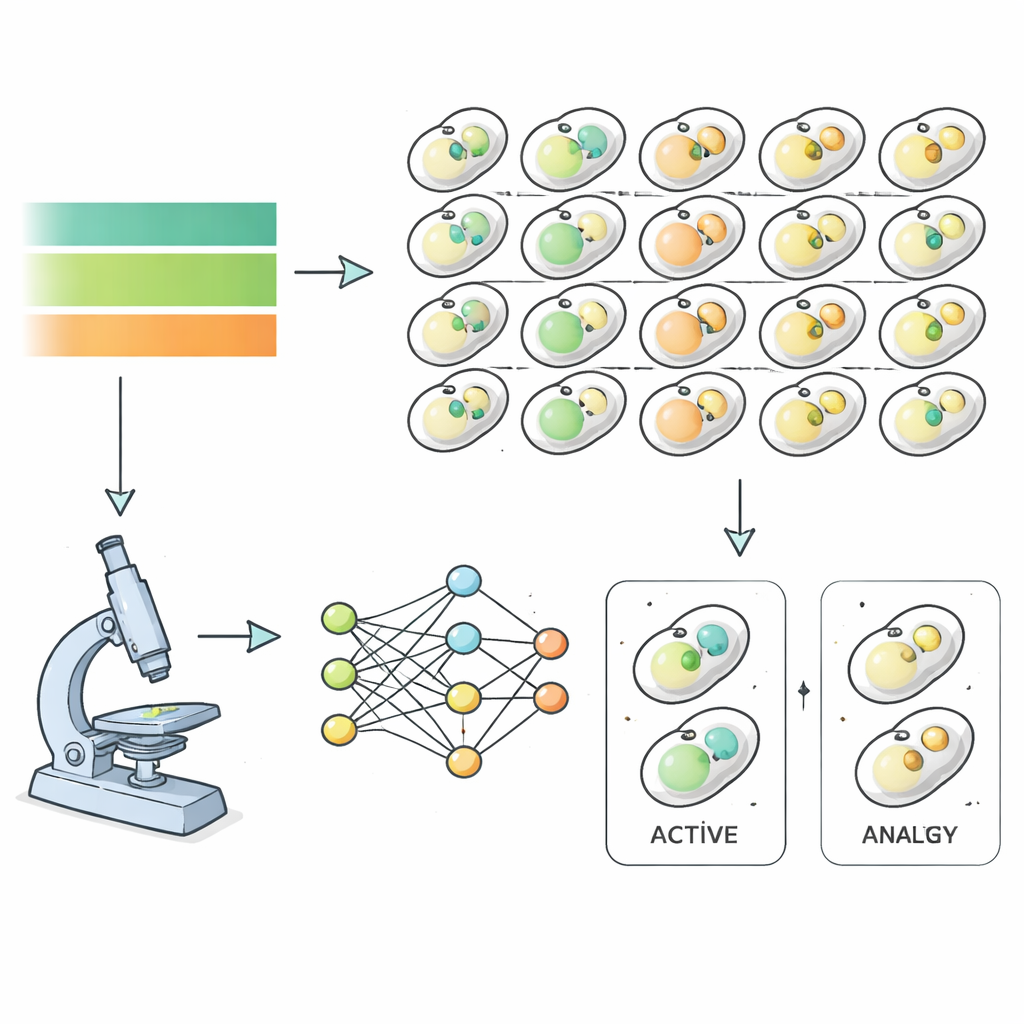
Six manières distinctes dont les cellules gèrent mal le recyclage
En ajustant mathématiquement ces séries temporelles, les auteurs ont extrait des « empreintes cinétiques » détaillées pour chaque mutant : la vitesse d’activation de l’autophagie, la durée pendant laquelle elle reste élevée, et la rapidité de son extinction. Le regroupement de ces signatures a mis en évidence six grands types de comportements. Certains mutants étaient « ultrasensibles », répondant très vite à la privation et au retour des nutriments. D’autres étaient « hyposensibles », réagissant lentement. Un groupe « hyperactif » présentait un recyclage basal anormalement élevé, tandis que plusieurs groupes montraient divers degrés d’incapacité à monter une réponse appropriée. De façon importante, des gènes centraux connus de l’autophagie se retrouvaient dans les classes les plus sévères, validant que la méthode capture une biologie réelle plutôt que du bruit de mesure.
Cartographier une hiérarchie de contrôle de l’autophagie
L’autophagie ne se produit pas isolément ; elle est intégrée aux réseaux régulateurs plus larges de la cellule. L’équipe a superposé leurs profils dynamiques sur de grandes cartes d’interactions génétiques et protéiques chez la levure. Les gènes dont la perte provoquait de forts défauts d’autophagie avaient tendance à se situer près du « noyau » connu de la machinerie autophagique dans ces réseaux, tandis que les mutants plus subtils étaient plus éloignés, en accord avec un contrôle plus indirect. En examinant les processus cellulaires enrichis dans chaque classe de comportement, ils ont constaté que l’activation déclenchée par la privation est fortement façonnée par les voies traitant l’ARN, la production protéique et le métabolisme énergétique, alors que l’arrêt de l’autophagie après le retour des nutriments dépend davantage du trafic membranaire et des étapes de fusion qui débarrassent les vésicules de recyclage.
Approfondir la formation et l’élimination des vésicules
L’autophagie progresse en deux étapes principales : la construction de vésicules chargées de cargos, puis leur fusion avec le compartiment de recyclage de la cellule pour la dégradation. Pour disséquer ces étapes, les chercheurs ont fouillé « l’espace latent » à l’intérieur de leur réseau neuronal — la représentation compressée qu’il utilise pour distinguer les images. En projetant cette représentation interne sur une carte bidimensionnelle, ils ont pu observer les populations cellulaires passer d’une région sans vésicules, à une région avec de nombreuses vésicules libres, puis à une région où les vésicules avaient été éliminées. En comparant statistiquement avec des mutants de référence bloqués à différents stades, ils ont quantifié pour chaque gène s’il affectait principalement la formation de vésicules, leur élimination, ou les deux. Cette analyse a montré que le contrôle de la formation de vésicules est très sensible aux niveaux d’azote au fil du temps, alors que la machinerie d’élimination se comporte de façon plus stable et constitue souvent le principal goulot d’étranglement du flux global de recyclage. 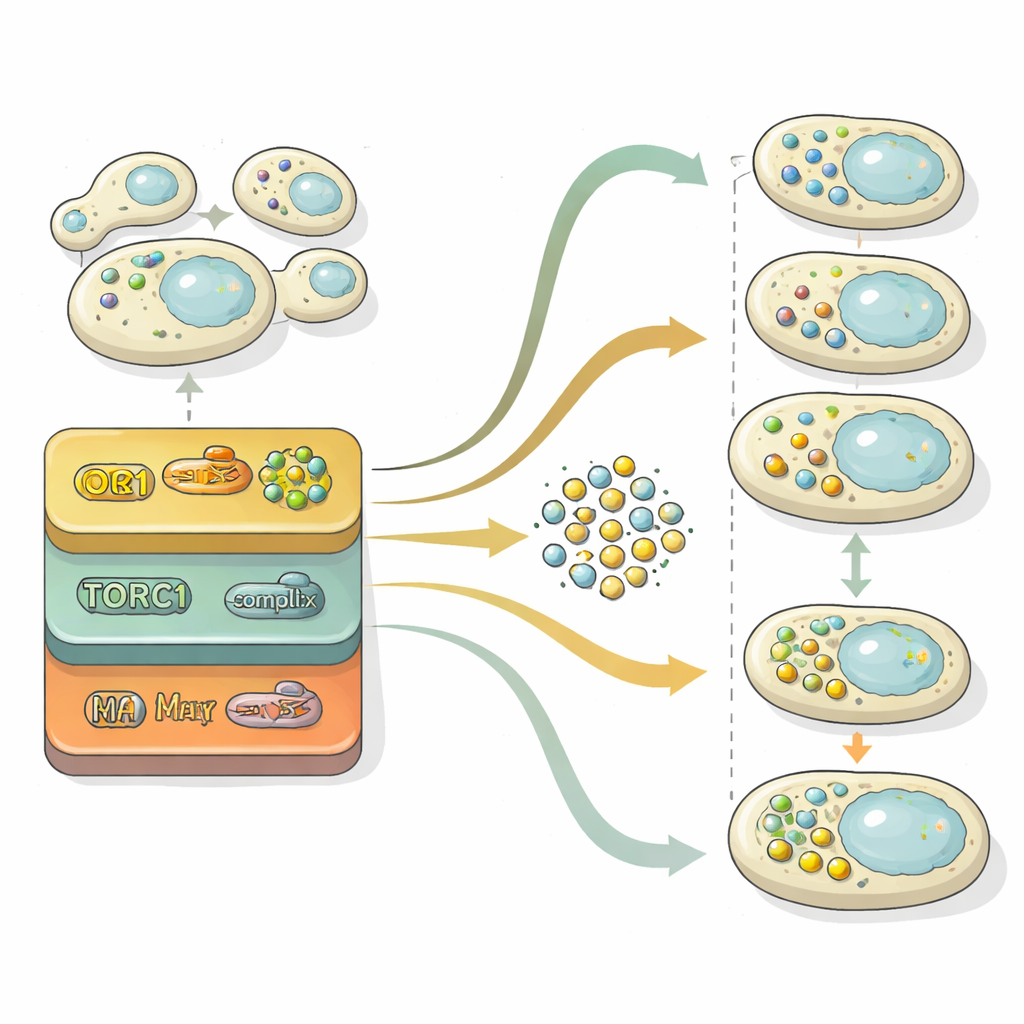
Un frein caché au recyclage : la voie rétrograde
Une des découvertes les plus marquantes concernait la voie dite rétrograde (RTG), qui transmet des signaux des mitochondries au noyau. Les cellules de levure dépourvues de composants RTG produisaient trop d’autophagosomes même en conditions riches en nutriments et peinaient à les éliminer une fois les nutriments rétablis. Des expériences de suivi détaillées ont montré que cette voie contrôle l’expression de gènes clés de l’autophagie, en particulier le lanceur maître ATG1, en grande partie indépendamment du senseur de nutriments bien connu TORC1 ciblé par des médicaments comme le rapamycine. En pratique, la signalisation RTG agit comme un frein variant dans le temps qui empêche une autophagie débridée en conditions riches et aide à terminer la réponse lorsque les conditions s’améliorent.
Pourquoi cela importe pour la santé et la thérapie
Dans l’ensemble, ce travail fournit une carte génomique résolue dans le temps de la manière dont les cellules ajustent l’autophagie face à des conditions nutritives changeantes. Il révèle que l’activation et l’arrêt ne sont pas des images miroir : beaucoup plus de gènes influencent le déclenchement du recyclage que son arrêt, et l’équilibre à long terme dépend fortement de l’élimination des vésicules et de freins transcriptionnels tels que la voie RTG. Pour le lecteur général, l’idée essentielle est que l’autocannibalisme cellulaire est soumis à un contrôle en couches et hiérarchique, et que nous pouvons désormais cartographier ces couches avec une grande précision. Ce type de vue au niveau des systèmes pourrait à terme guider des thérapies plus nuancées qui ajustent l’autophagie à des phases spécifiques — stimulant le recyclage bénéfique sans déclencher les effets nocifs d’une autodigestion chronique et incontrôlée.
Citation: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Mots-clés: autophagie, apprentissage profond, génétique de la levure, détection des nutriments, recyclage cellulaire