Clear Sky Science · fr
Phénotypage affiné des réponses vaccinales révèle des déterminants transcriptomiques de l'hétérogénéité des anticorps neutralisants
Pourquoi certains vaccins fonctionnent mieux pour certaines personnes
Lorsque nous nous faisons vacciner contre la COVID-19, on pourrait supposer que le système immunitaire réagit de la même façon pour tous. En réalité, les individus diffèrent fortement dans la rapidité et l'intensité avec lesquelles ils développent des anticorps protecteurs. Cette étude a suivi des adultes ayant reçu des vaccins inactivés contre le SARS-CoV-2 et montre que les réponses vaccinales se répartissent en profils distincts, chacun piloté par des signaux immunitaires précoces différents inscrits dans nos gènes et nos cellules sanguines. Comprendre ces profils pourrait un jour permettre d'ajuster les calendriers de vaccination afin que chacun obtienne la protection nécessaire.
Trois trajectoires vers la protection après la même injection
Les chercheurs ont suivi 73 adultes en bonne santé ayant reçu deux doses d'un vaccin inactivé contre la COVID-19. Ils ont mesuré les anticorps neutralisants — ceux capables de bloquer le virus — avant la vaccination, une semaine après la seconde dose, puis environ un mois plus tard. Plutôt que de classer simplement les individus en « forts » et « faibles » répondeurs, ils ont utilisé des méthodes basées sur les données pour regrouper les personnes selon l'évolution de leurs taux d'anticorps dans le temps. Trois profils nets sont apparus : un groupe « faible‑retardé » avec une hausse lente et modeste des anticorps ; un groupe « rapide‑stabilisé » dont les anticorps ont grimpé rapidement puis se sont stabilisés ; et un groupe « augmentation‑continue » dont les anticorps ont continué d'augmenter jusqu'aux niveaux les plus élevés. Ces profils ne s'expliquaient pas par l'âge, le sexe ou le poids corporel et n'étaient que partiellement liés à la marque du vaccin inactivé reçue.
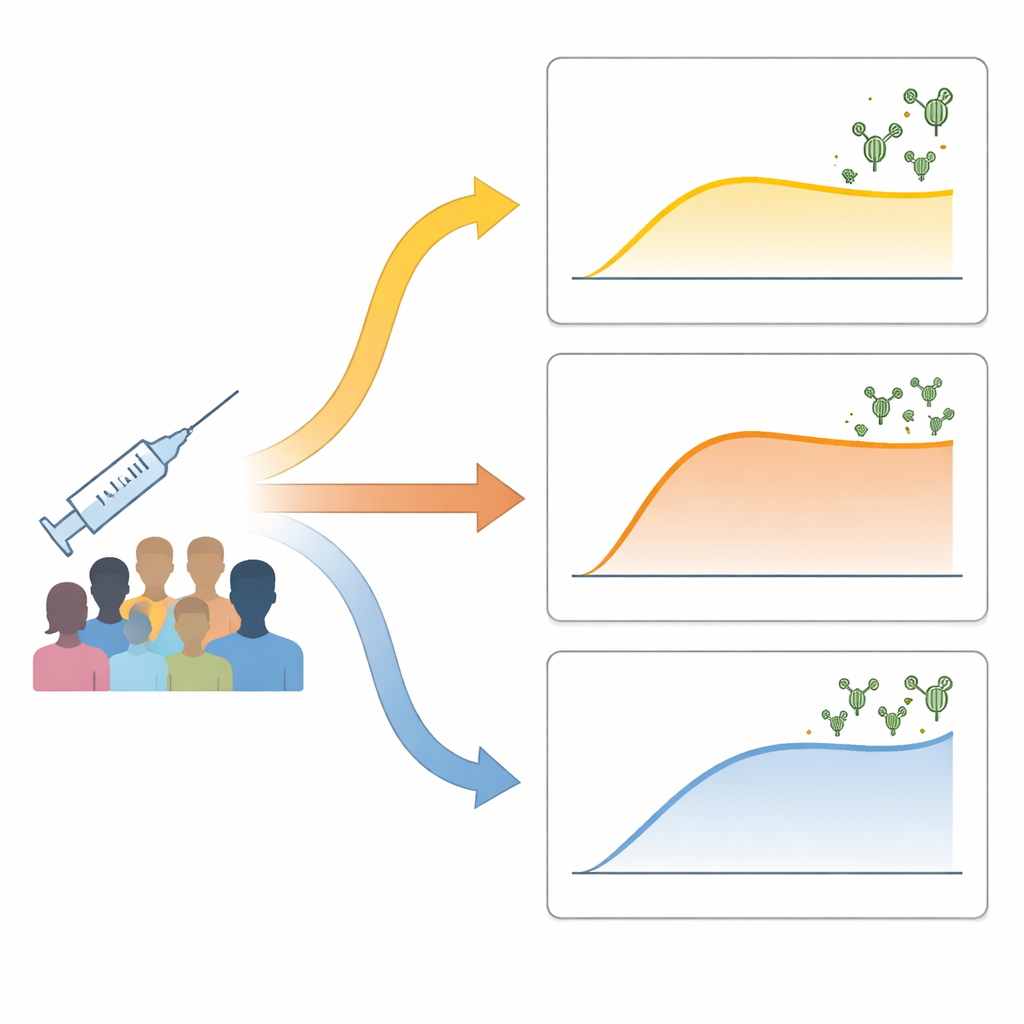
Comment l'activité immunitaire précoce façonne le résultat
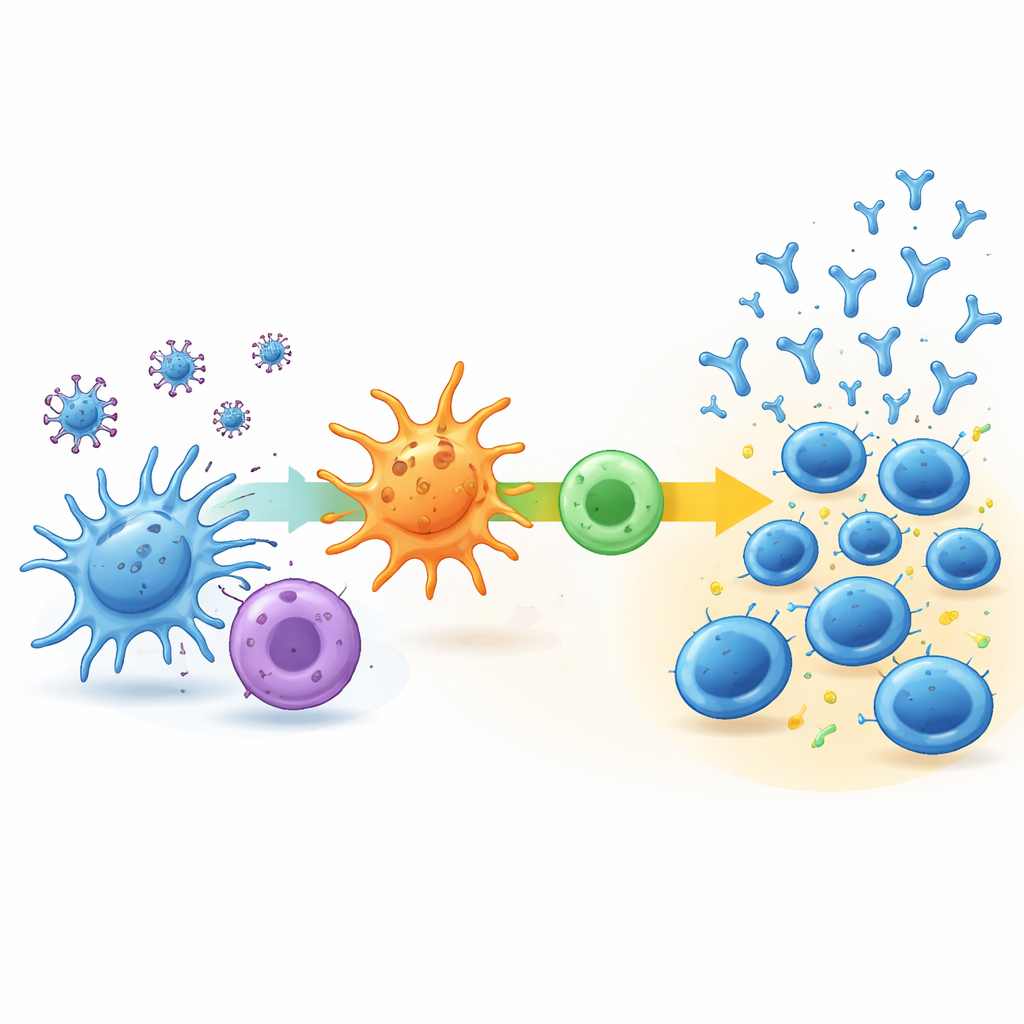
Pour comprendre ce qui pilote ces trajectoires différentes, l'équipe a analysé l'activité génétique des cellules immunitaires dans le sang au départ et une semaine après la seconde injection. Dans le groupe faible‑retardé, très peu de choses changeaient : les voies immunitaires clés étaient à peine activées et la composition des types cellulaires immunitaires dans le sang restait largement la même. En revanche, les groupes rapide‑stabilisé et augmentation‑continue montraient des signes clairs d'activation immunitaire précoce. Chez les répondeurs les plus forts, on observait une activation coordonnée de voies impliquées dans le traitement des fragments viraux, leur présentation à d'autres cellules immunitaires, et le soutien d'un type de réponse des cellules T auxiliaires connu pour stimuler la production d'anticorps. Ces personnes avaient aussi tendance à présenter davantage de cellules B naïves et de cellules T auxiliaires prêtes à répondre, et montraient ensuite une activité des cellules T spécifiques au virus quelque peu plus marquée.
Couches cachées de contrôle dans l'ARN et les cellules B
Au‑delà des simples modifications on/off des gènes, les scientifiques ont examiné des couches de régulation plus subtiles intégrées dans l'ARN, les molécules intermédiaires entre l'ADN et les protéines. Dans le groupe des meilleurs répondeurs, les gènes immunitaires impliqués dans la présentation des fragments viraux au système immunitaire présentaient des patrons d'épissage différents et des régions terminales plus courtes à l'extrémité de leur ARN. Ces caractéristiques sont censées faciliter la production de certaines protéines et maintenir une signalisation robuste. L'équipe a également reconstruit le répertoire des récepteurs des cellules B — les antennes uniques des cellules productrices d'anticorps — à partir des mêmes échantillons sanguins. Bien que la diversité globale paraisse similaire entre les groupes, chaque profil de réponse utilisait des combinaisons et des formes de récepteurs légèrement différentes, et les répondeurs les plus forts favorisaient des types de récepteurs déjà associés à des anticorps puissants dirigés contre la protéine spike du coronavirus.
Repérer les faibles répondeurs probables avant la vaccination
Comme les individus du groupe faible‑retardé risquent d'être moins protégés après un calendrier vaccinal standard, les chercheurs se sont demandé s'il était possible de les identifier à l'avance. Ils se sont concentrés sur un petit ensemble de gènes dont l'activité différait modestement au départ entre les répondeurs les plus faibles et les plus forts. À l'aide de méthodes d'apprentissage automatique, ils ont construit un modèle basé sur l'activité de seulement huit gènes mesurés avant la vaccination. Ce modèle pouvait distinguer les répondeurs faible‑retardé avec une grande précision dans leur jeu de données, deux gènes impliqués dans la signalisation cellulaire de base et l'inflammation apportant la majeure partie du pouvoir prédictif. Bien que ce travail doive être validé sur des cohortes plus larges et plus diverses, il suggère qu'un simple test sanguin pourrait un jour orienter des schémas de vaccination plus personnalisés.
Ce que cela signifie pour les vaccins futurs
Globalement, cette étude montre que les individus ne se contentent pas de produire des réponses en anticorps « fortes » ou « faibles » ; ils suivent des chronologies différentes façonnées par des événements immunitaires précoces difficiles à détecter. Les personnes les mieux protégées activent des réseaux coordonnés de gènes et de cellules qui leur permettent de reconnaître rapidement le vaccin et de générer des anticorps durables, tandis que les faibles répondeurs présentent une réaction précoce atténuée. En cartographiant ces différences internes et en développant des outils pour prédire qui répondra mal, ce travail ouvre la voie à une vaccination personnalisée — par exemple des rappels plus précoces ou des formulations alternatives pour les personnes à risque — afin que les bénéfices des vaccins puissent être partagés de manière plus équitable.
Citation: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Mots-clés: réponses vaccinales, anticorps neutralisants, vaccination COVID-19, hétérogénéité immunitaire, vaccins personnalisés