Clear Sky Science · fr
Immunogénicité et protection de candidats vaccinaux grippe octavalents utilisant des protéines adjuvantées ou des ARNm‑LNP chez des souris naïves
Pourquoi un meilleur vaccin contre la grippe compte
Les vaccins saisonniers contre la grippe sauvent de nombreuses vies, mais leur efficacité peut varier fortement d’une année à l’autre. L’une des raisons est que les vaccins actuels entraînent principalement le système immunitaire à reconnaître une seule protéine virale, laissant d’autres cibles utiles sous‑exploitées. Cette étude chez la souris explore des vaccins antigrippaux de nouvelle génération qui apprennent au système immunitaire à reconnaître simultanément deux protéines virales clés et compare une approche traditionnelle à base de protéines à une technologie ARNm plus récente, similaire à celle utilisée pour les récents vaccins contre la COVID‑19.
Deux cibles au lieu d’une
Les vaccins actuels se concentrent surtout sur l’hémagglutinine, ou HA, une protéine qui aide le virus à s’attacher à nos cellules. Les chercheurs ont ajouté une seconde protéine virale, la neuraminidase, ou NA, qui aide le virus à s’échapper des cellules infectées et à se propager. En combinant quatre variantes de HA et quatre variantes de NA issues des souches saisonnières 2018–2019, ils ont élaboré un vaccin « octavalent » destiné à couvrir deux types d’influenza A et deux lignées d’influenza B. Ils ont ensuite conditionné ces huit composants de deux façons : sous forme de protéines purifiées mélangées à un adjuvant stimulant le système immunitaire, et sous forme d’ARNm encapsulé dans de petites bulles lipidiques (ARNm‑LNP) qui incitent les propres cellules de l’organisme à produire les protéines virales.
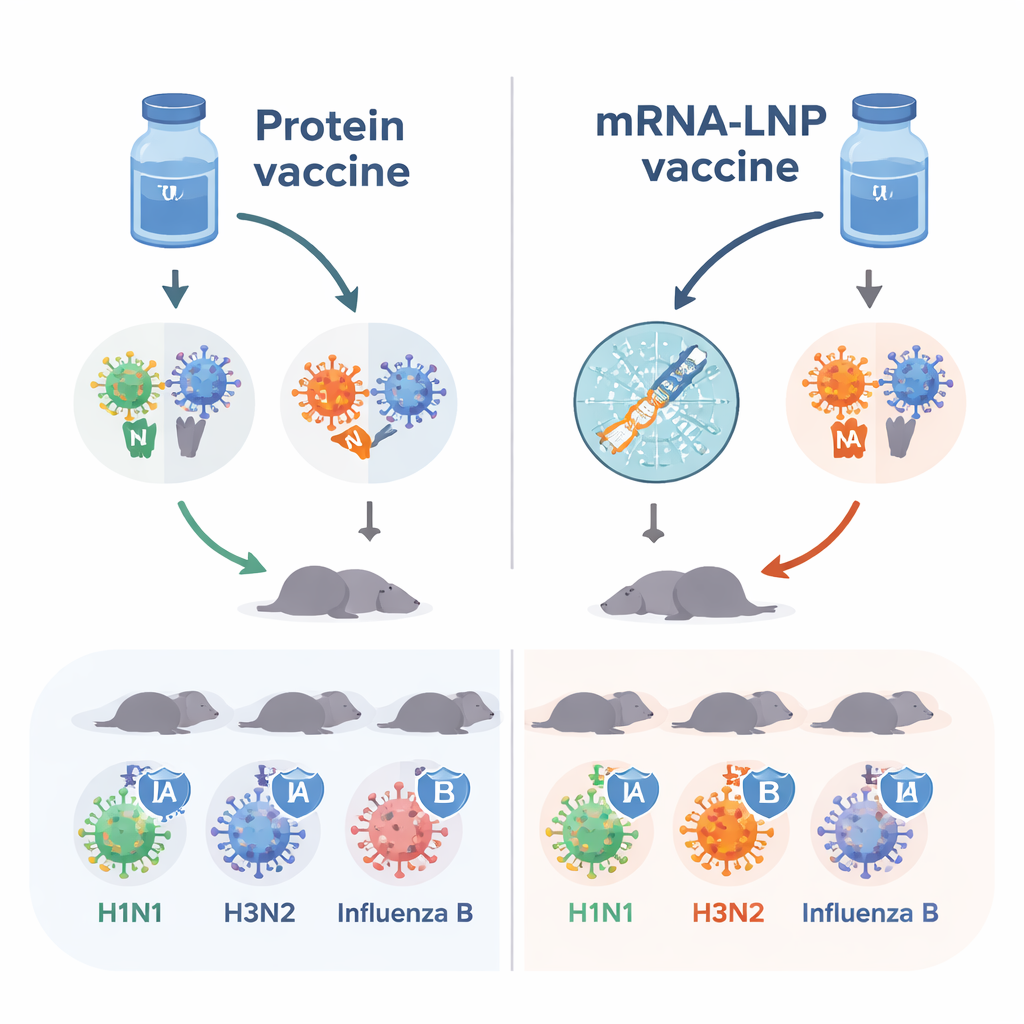
Réponses anticorps plus fortes avec l’ARNm
Des souris naïves — n’ayant jamais été exposées aux virus de la grippe ni aux vaccins — ont reçu deux doses soit du vaccin protéique soit de la version ARNm‑LNP. L’équipe a mesuré dans le sang les anticorps reconnaissant la HA et la NA. Les deux vaccins ont généré des réponses utiles, mais les injections ARNm‑LNP ont systématiquement produit des niveaux d’anticorps plus élevés contre la plupart des composants HA et NA. En particulier, les anticorps inhibant l’activité de la NA, qui contribuent indépendamment à la protection, étaient généralement plus forts après vaccination par ARNm‑LNP. Ces résultats suggèrent que, du moins dans ce modèle animal, la plateforme ARNm rend les mêmes cibles virales plus visibles pour le système immunitaire.
Protection contre des souches appariées et actuelles
Le vrai test était de savoir si ces vaccins pouvaient préserver les souris d’une maladie sévère. À des doses ajustées pour être similaires à une dose humaine, les deux formats vaccinals ont complètement protégé les animaux contre une infection létale par des virus H1N1 et influenza B étroitement appariés aux composants du vaccin, ainsi que contre des virus de type H3N2 conçus artificiellement utilisés lorsque les souches humaines standard ne rendent pas les souris malades. Les souris vaccinées ont maintenu leur poids corporel et survécu, tandis que les animaux non vaccinés ont perdu du poids et sont souvent morts. Pour ces souches proches, les vaccins protéiques traditionnels et les vaccins ARNm‑LNP ont montré des performances similaires en termes de survie, même si les profils d’anticorps différaient.
Avantage face aux vieux virus grippaux décalés
Là où l’approche ARNm‑LNP s’est distinguée, c’est dans des tests plus exigeants de « décalage » (mismatch). Les chercheurs ont défié des souris vaccinées avec des souches H3N2 historiques de 1968, 1975 et 1982 — des virus différents des souches modernes que le vaccin cherchait à imiter. Toutes les souris non vaccinées et la plupart des animaux ayant reçu les vaccins protéiques sont mortes, mais chaque souris ayant reçu le vaccin octavalent ARNm‑LNP a survécu, bien qu’elles aient encore présenté des signes de maladie. Cet avantage de survie a persisté jusqu’à près d’un an après la vaccination, indiquant une protection durable. Lorsque l’équipe a transféré du sérum sanguin d’animaux vaccinés à des souris non vaccinées, seul le sérum contenant des anticorps induits par les vaccins ARNm‑LNP dirigés contre la HA a protégé de la mort provoquée par un virus décalé, ce qui pointe les anticorps HA à activité croisée comme facteur clé.
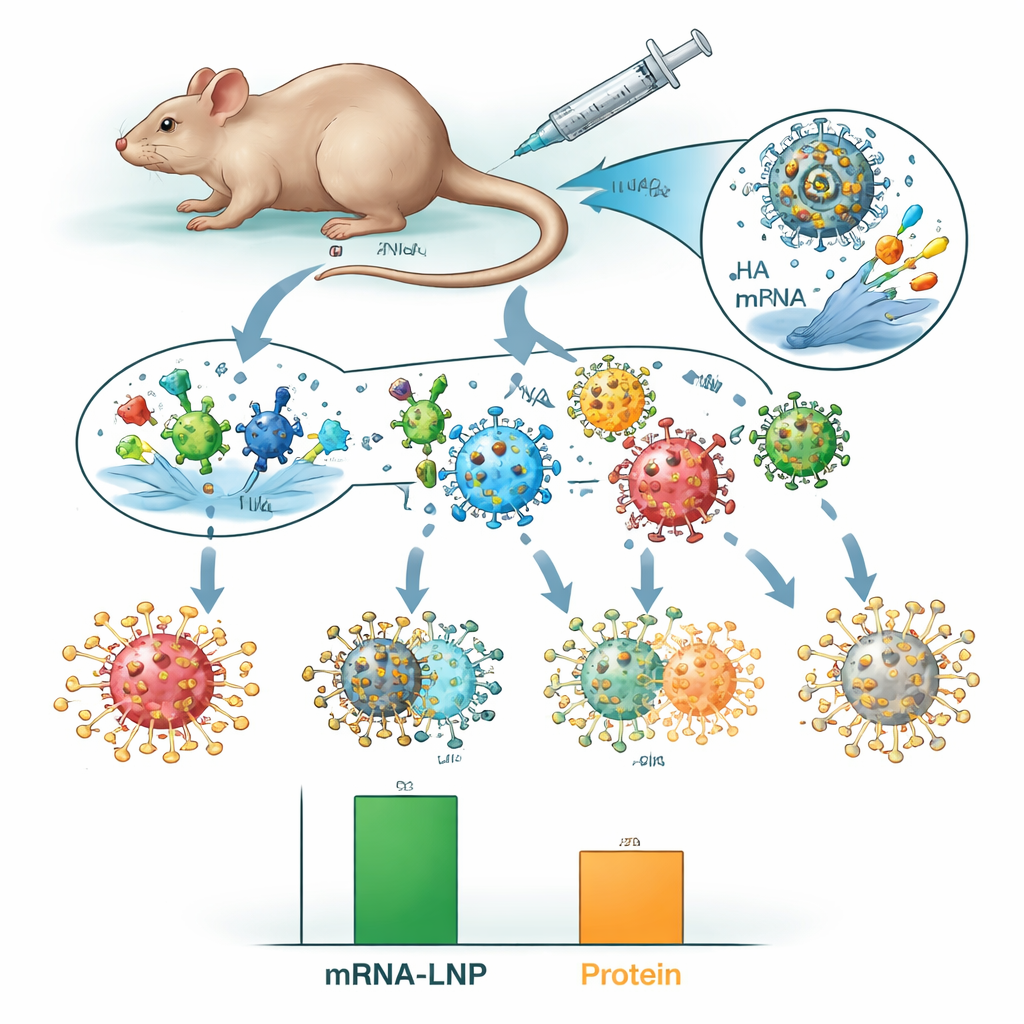
Ce que cela signifie pour les futurs vaccins antigrippaux
Pour un non‑spécialiste, le message est que les deux types de vaccins ont protégé les souris contre les souches pour lesquelles ils avaient été conçus, mais que la version ARNm‑LNP offrait en plus une protection plus large et plus durable contre des virus plus anciens et hors date. En incluant les deux principales protéines de surface de la grippe et en utilisant l’ARNm pour les présenter au système immunitaire, cette stratégie pourrait contribuer à réduire l’écart entre des saisons grippales efficaces et moins efficaces. Bien que des résultats chez la souris n’assurent pas le succès chez l’humain, et que des adjuvants plus puissants pourraient encore améliorer les vaccins protéiques, le travail soutient l’idée que des vaccins antigrippaux multicomposants à base d’ARNm pourraient un jour offrir une protection plus fiable contre un éventail plus large de souches grippales circulantes et émergentes.
Citation: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Mots-clés: vaccin contre la grippe, ARNm‑LNP, hémagglutinine, neuraminidase, protection croisée