Clear Sky Science · fr
Adjuvant vaccinal potentialisant la présentation croisée d’antigènes pour l’expansion des lymphocytes T et la synergie avec les anti‑PD‑1
Transformer le système immunitaire en un combattant tumoral de précision
On présente souvent les vaccins anticancéreux comme un moyen d’apprendre au système immunitaire à reconnaître et détruire les tumeurs, mais en pratique ils ont rarement tenu cette promesse. Cette étude explore une nouvelle manière de « suralimenter » ces vaccins afin qu’ils génèrent des lymphocytes T cytotoxiques plus forts et durables, et qu’ils agissent mieux en synergie avec des médicaments d’immunothérapie populaires comme les anti–PD‑1. Pour les lecteurs intéressés par la façon dont les traitements du futur pourraient combiner médicaments biologiques, vaccins et ingénierie immunitaire, ce travail donne un aperçu de ce à quoi pourrait ressembler une immunothérapie de nouvelle génération, très ciblée.
Pourquoi les vaccins contre le cancer ont besoin d’un meilleur soutien
Les vaccins thérapeutiques contre le cancer ne visent pas à prévenir la maladie, mais à traiter des personnes déjà porteuses de tumeurs en suscitant des réponses immunitaires puissantes et spécifiques aux tumeurs. Les acteurs clés sont les lymphocytes T CD8 « tueurs », capables de reconnaître et d’éliminer les cellules cancéreuses affichant des antigènes caractéristiques. Malheureusement, les antigènes tumoraux stimulent faiblement car ils ressemblent souvent à des versions altérées des protéines endogènes. Une exposition continue pendant le développement tumoral peut aussi laisser les T cells épuisés ou tolérants, atténuant l’effet du vaccin. Pour contrer cela, les vaccins doivent être associés à des adjuvants — des composants d’aide qui réveillent l’immunité innée, améliorent la présentation des antigènes et constituent un réservoir large et résilient de lymphocytes T spécifiques de la tumeur.
Un booster immunitaire hybride construit à partir de deux signaux puissants
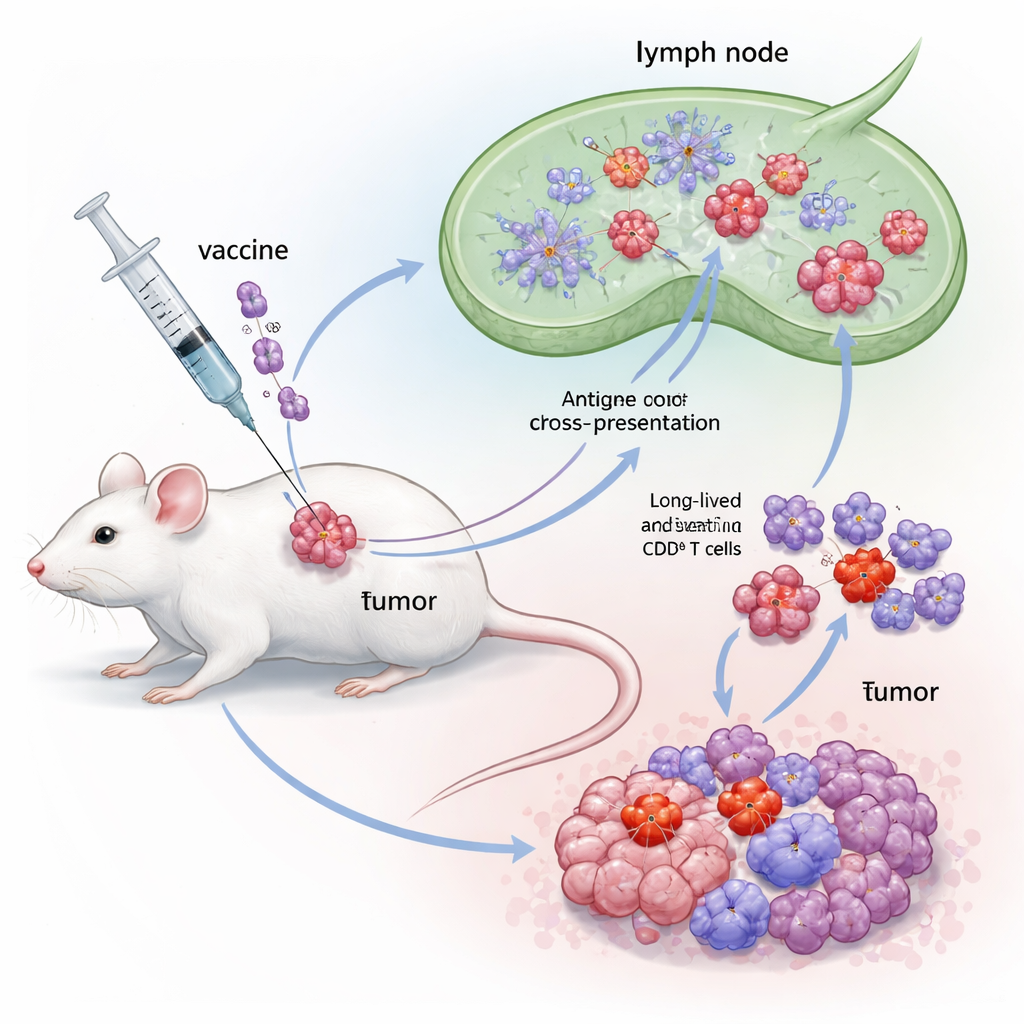
Les chercheurs ont conçu un adjuvant hybride appelé Flt3L‑FlaB, ou FB, en fusionnant deux molécules immunostimulatrices en une seule protéine. Une moitié, Flt3L, est un facteur de croissance naturel qui expandent un groupe spécialisé de cellules dendritiques connu sous le nom de cDC1. Ces cellules excellent dans la « présentation croisée » — elles prennent des fragments de matériel tumoral et les présentent aux lymphocytes T CD8 d’une manière qui déclenche des réponses fortes. L’autre moitié, FlaB, est un fragment de flagelline bactérienne qui active un senseur inné appelé TLR5 et agit comme un signal de danger puissant. En les liant, les auteurs visaient à la fois à augmenter le nombre de cDC1 et à les convertir en un état hautement actif, améliorant la façon dont les antigènes tumoraux sont présentés aux T cells et la durée de cette stimulation.
Évaluer le nouvel adjuvant dans des modèles tumoraux
Pour tester FB, l’équipe a utilisé un modèle tumoral murin bien établi basé sur des cellules modifiées pour porter des protéines oncogéniques du papillomavirus humain (VPH). Les souris ont d’abord reçu un petit implant tumoral puis un vaccin thérapeutique contenant un antigène E7 du VPH, associé soit à Flt3L seul, à FlaB seul, ou à la nouvelle fusion FB. Tous les vaccins ont été administrés à proximité de la tumeur. Si chaque adjuvant seul ralentissait un peu la croissance tumorale, le vaccin à base de FB se démarquait : il retardait beaucoup plus la progression tumorale, prolongeait significativement la survie et laissait une fraction notable de souris complètement débarrassées de la tumeur. Les analyses immunitaires ont montré que la vaccination par FB générait des réponses CD8 spécifiques à E7 exceptionnellement fortes dans le sang, les ganglions lymphatiques et la rate, avec des niveaux élevés d’interféron‑gamma et une forte prolifération des T cells — preuve que la fusion faisait plus que simplement additionner les effets de ses deux composantes.
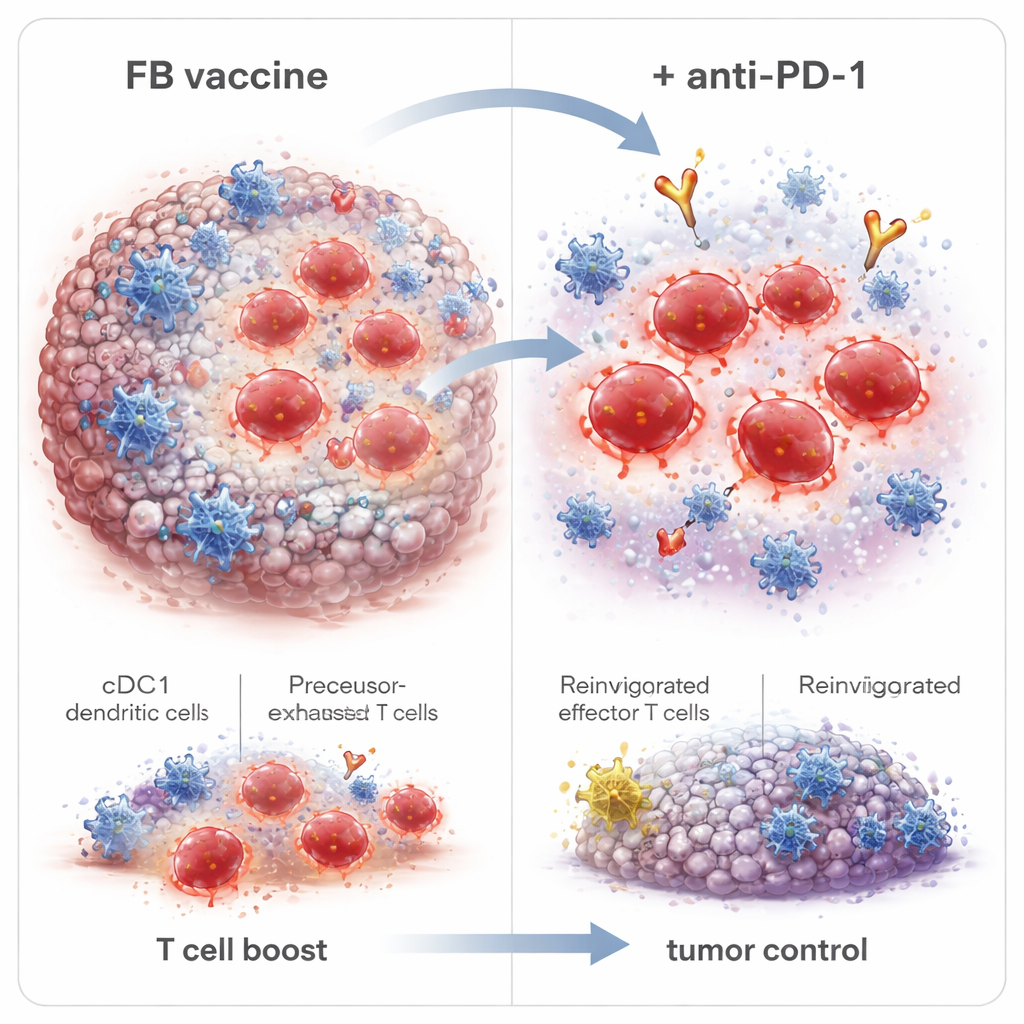
Construire une mémoire immunitaire durable et un meilleur partenaire pour les anti–PD‑1
En approfondissant, les scientifiques ont constaté que FB modifiait non seulement le nombre de lymphocytes T CD8 présents, mais aussi leurs types. Il augmentait les cellules effectrices à courte durée de vie qui attaquent immédiatement les tumeurs, ainsi que les cellules précurseures de mémoire et les cellules mémoire de type « stem‑like » qui peuvent persister et répondre de nouveau ultérieurement. Fait important, FB a également élargi un groupe appelé cellules précurseures‑épuisées (Tpex) au sein des tumeurs — des cellules situées à la frontière entre l’épuisement et l’activité complète et particulièrement réceptives aux médicaments anti–PD‑1. Lorsque les survivants sans tumeur ont été mis au défi avec des doses plus élevées de cellules cancéreuses longtemps après la vaccination, la plupart ont résisté à la repousse, montrant une mémoire immunitaire durable. Le blocage de la sortie des cellules immunitaires des ganglions lymphatiques a éliminé les bénéfices de FB, ce qui indique que les T cells tueuses de tumeurs étaient primées dans ces ganglions par les cDC1 puis migraient vers la tumeur.
Plus forts ensemble : vaccins et blocage des points de contrôle
Étant donné que la thérapie anti–PD‑1 marche mieux lorsqu’un réservoir de T cells réceptives est déjà présent, l’équipe a combiné la vaccination adjuvantée par FB avec un anticorps anti–PD‑1. Dans le modèle tumoral VPH, l’ajout d’anti–PD‑1 en plus de la vaccination FB a encore ralenti la croissance tumorale, augmenté le nombre de souris ayant complètement éliminé leur cancer, et assuré une protection complète contre une rechallenge tumorale à dose extrêmement élevée. L’ajustement du calendrier importait : commencer l’anti–PD‑1 après la deuxième dose de vaccin plutôt qu’après la première améliorait modestement l’éradication complète des tumeurs, cohérent avec l’attente que les cellules Tpex aient eu le temps de s’étendre. L’adjuvant FB a aussi amélioré les réponses aux vaccins à base de peptides, y compris des néo‑antigènes tumoraux dans un modèle de cancer du côlon, suggérant que cette stratégie pourrait s’appliquer largement au‑delà des maladies liées au VPH.
Ce que cela pourrait signifier pour les soins oncologiques futurs
Pour les non‑spécialistes, le message clé est que ce travail affine la manière d’« enseigner » au système immunitaire à combattre le cancer. En combinant un facteur de croissance des cellules dendritiques avec un fort signal de danger dans une seule protéine stable, l’adjuvant FB crée davantage les cellules présentatrices d’antigènes appropriées, les aide à présenter plus efficacement les antigènes tumoraux et façonne une population de lymphocytes T tueurs à la fois puissants immédiatement et prêts à répondre ultérieurement à une thérapie par points de contrôle. Bien que ces résultats aient été obtenus chez la souris et que de nombreuses étapes restent à franchir avant une utilisation chez l’homme, l’étude trace une feuille de route claire : des adjuvants plus intelligents qui orchestrent la présentation croisée et la stemness des T cells pourraient faire des vaccins thérapeutiques contre le cancer un partenaire bien plus efficace pour des médicaments comme les anti–PD‑1, conduisant potentiellement à un contrôle tumoral plus profond et plus durable chez les patients.
Citation: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Mots-clés: vaccins contre le cancer, immunothérapie, cellules dendritiques, blocage de PD‑1, tumeurs liées au VPH