Clear Sky Science · fr
Conception d’un vaccin muqueux universel à large spectre pour les coronavirus humains inspirée par des anticorps artificiels
Pourquoi un meilleur vaccin contre les coronavirus reste important
Même si la COVID-19 tend vers une infection saisonnière, de nouvelles vagues de variants continuent d’apparaître et plusieurs autres coronavirus humains provoquent encore des maladies graves. Les vaccins actuels protègent bien contre les formes sévères mais sont moins efficaces pour bloquer l’infection et la transmission, en particulier dans le nez et la gorge où ces virus s’installent d’abord. Cette étude décrit un nouveau type de vaccin intranasal, inspiré d’anticorps conçus artificiellement, qui vise à offrir une protection durable et large contre de nombreux coronavirus au niveau des surfaces muqueuses du corps.
Construire un échafaudage vaccinal plus intelligent
Les chercheurs sont partis d’une molécule familière : l’IgG1 humaine, le principal type d’anticorps utilisé dans de nombreux médicaments par anticorps approuvés. Ils ont redessiné sa chaîne lourde pour qu’elle puisse servir d’« échafaudage » flexible présentant les domaines de liaison au récepteur (RBD) de la protéine spike des coronavirus — les éléments que le virus utilise pour saisir nos cellules. En supprimant la chaîne légère habituelle et en ajoutant des mutations spécifiques, ils ont réduit la liaison aux récepteurs immunitaires associés à des effets secondaires comme les orages cytociniques, tout en renforçant la liaison au récepteur Fc néonatal (FcRn). Le FcRn est abondant sur les surfaces muqueuses et aide à traverser la barrière et à prolonger la durée de vie des anticorps. Sur cette charpente optimisée, l’équipe a greffé un, deux, trois ou quatre RBD différents provenant du SARS, du MERS, de coronavirus saisonniers et de plusieurs variants du SARS‑CoV‑2, y compris des lignées Omicron, créant des candidats vaccinaux mono-, bi-, tri- et tétravalents.
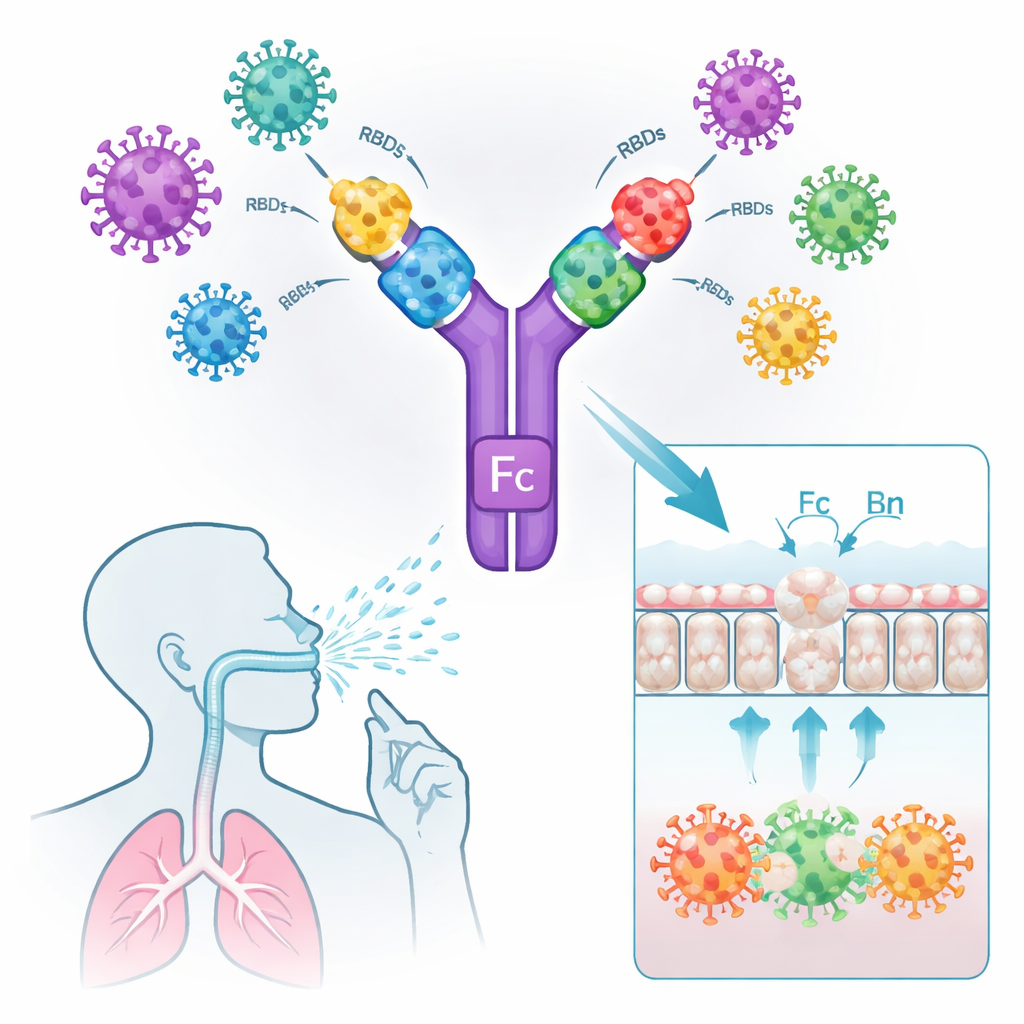
Traverser la barrière muqueuse et activer les défenses locales
Pour fonctionner comme spray nasal, les antigènes vaccinals doivent atteindre et persister sur l’épithélium respiratoire et être efficacement repérés par les cellules immunitaires. Dans des systèmes de culture cellulaire, les constructions portant la région Fc se liaient fortement à la fois à ACE2 (le récepteur d’entrée du SARS‑CoV‑2) et au FcRn humain ou murin, et étaient activement transportées à travers une couche de cellules muqueuses. Un dimère RBD similaire dépourvu de la portion Fc n’a pas réussi à traverser. Lorsqu’on a administré des versions fluorescentes des vaccins dans le nez de souris, les antigènes contenant le Fc sont restés dans la muqueuse pulmonaire pendant des heures, tandis que le dimère RBD seul a rapidement disparu. La microscopie a montré que les vaccins modifiés par le Fc attiraient et activaient les cellules présentatrices d’antigène juste sous la surface muqueuse, comme l’indiquaient des niveaux plus élevés du marqueur immunitaire CD80 et une colocalisation avec FcRn.
Renforcer anticorps et cellules T là où c’est nécessaire
L’équipe a ensuite comparé les réponses immunitaires après injection intramusculaire versus administration intranasale chez la souris. Pour plusieurs formulations, les vaccins basés sur Fc ont déclenché des taux très élevés d’IgG sanguines contre la souche originale du SARS‑CoV‑2 et contre Omicron XBB.1.5. L’administration intranasale, surtout lorsqu’elle était combinée à un adjuvant agoniste de la voie STING moderne (CF501), s’est distinguée en générant de fortes réponses IgA non seulement dans le sang mais aussi dans les sécrétions nasales et les lavages pulmonaires — précisément là où la protection muqueuse est la plus importante. Les constructions portant Fc ont également induit des réponses cellulaires plus puissantes que les dimères RBD nus, augmentant les lymphocytes T auxiliaires, les lymphocytes T cytotoxiques et les lymphocytes T mémoire résidents de longue durée dans les poumons. Ces types cellulaires sont considérés comme cruciaux pour éliminer les virus respiratoires et prévenir leur propagation vers des organes sensibles comme le cerveau.
Protection large contre de nombreux variants et espèces
Un test central était de savoir si un vaccin bivalent combinant les RBD du virus prototype et d’Omicron XBB.1.5 (appelé XBB.1.5 + PT‑Fc) pouvait protéger les animaux contre plusieurs défis viraux. Chez des souris exprimant l’ACE2 humaine et ayant reçu deux faibles doses intranasales, ce candidat a induit de puissants anticorps neutralisants et a complètement protégé les animaux contre une infection létale aussi bien par le virus original que par XBB.1.16 : les souris vaccinées ont maintenu leur poids, ont survécu et n’avaient aucun virus détectable dans le cerveau, les poumons ou les tissus nasaux, tandis que les animaux témoins tombaient malades et mouraient. Le même vaccin a empêché maladie et décès lorsque les souris ont été défiées par d’autres variants majeurs, y compris Beta, Delta et plusieurs sous‑lignées d’Omicron. Chez le hamster, modèle adapté aux études de transmission, les animaux vaccinés présentaient des charges virales nettement plus faibles après inoculation directe et, dans des expériences de cohabitation, étaient en grande partie protégés contre la transmission aérienne. Les niveaux d’anticorps et les cellules T mémoire chez la souris et le hamster sont restés élevés pendant au moins 48 semaines, et les animaux étaient encore entièrement protégés contre des défis létaux près d’un an après la vaccination.
Vers un spray nasal universel contre les coronavirus
Enfin, les chercheurs ont orienté la plateforme vers une conception véritablement universelle. Ils ont mélangé plusieurs constructions bivalentes couvrant le SARS‑CoV‑2, le SARS, le MERS et plusieurs coronavirus saisonniers, et ont aussi fabriqué des molécules tétravalentes portant quatre RBD distincts ou fragments de spike sur un seul échafaudage. Ces combinaisons ont élevé des anticorps reconnaissant un large panel de coronavirus humains et, dans des expériences de défi chez la souris, ont réduit les charges virales pour plusieurs représentants, y compris un virus endémique (NL63). Bien que des tests supplémentaires dans des modèles plus proches de l’humain et, in fine, des essais cliniques soient nécessaires, ce travail montre qu’un échafaudage d’anticorps ingénieré peut transporter en toute sécurité des antigènes coronavirologiques divers à travers la barrière nasale, stimuler une immunité locale et systémique robuste, et fournir une protection large et durable. Pour les non‑spécialistes, le message est que les futurs « boosters » universels contre les coronavirus pourraient ne pas être des injections mais de doux sprays nasaux basés sur les mêmes cadres d’anticorps déjà jugés sûrs dans de nombreux médicaments.
Citation: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
Mots-clés: vaccin intranasal, coronavirus à large spectre, immunité muqueuse, échafaudage d’anticorps artificiel, variants du SARS-CoV-2