Clear Sky Science · fr
L’immunisation hétérologue module la compétition entre épitopes B de peptides aides et le segment MPER dans des vaccins MPER/liposomes
Pourquoi cette étude sur le vaccin contre le VIH est importante
Concevoir un vaccin efficace contre le VIH a été extraordinairement difficile, en partie parce que le virus mute rapidement et dissimule ses parties les plus vulnérables au système immunitaire. Cette étude examine une approche astucieuse pour inciter l’organisme à se focaliser sur une de ces faiblesses cachées, appelée région MPER, en l’encapsulant dans de petites bulles lipidiques appelées liposomes et en variant soigneusement les composants « aides » entre les injections. Le travail, réalisé chez la souris, ne produit pas encore de vaccin opérationnel, mais il révèle des règles pratiques pour orienter les réponses immunitaires vers des anticorps rares et protecteurs et les détourner de cibles distrayantes.
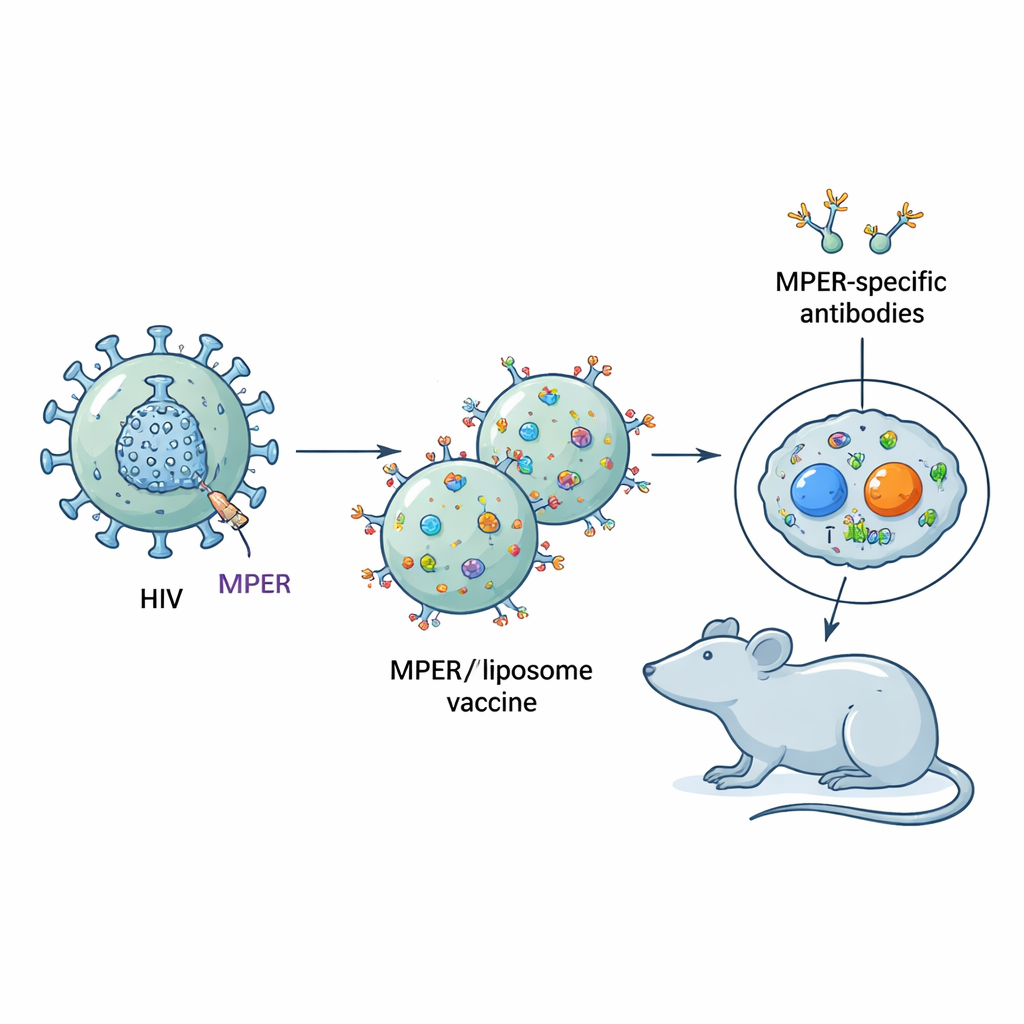
La faiblesse cachée du virus
Le VIH est recouvert d’une coque protéique parsemée de pointes que le virus utilise pour pénétrer dans les cellules. De nombreuses parties de ces pointes mutent facilement, aidant le VIH à échapper aux anticorps. En revanche, un court segment près de la base d’une de ces protéines de pointe, appelé région externe proximale à la membrane (MPER), est fortement conservé entre les souches de VIH et reconnu par certains des anticorps neutralisants les plus puissants observés chez une minorité de personnes infectées à long terme. Malheureusement, le MPER se situe juste à côté de la membrane virale et est partiellement enfoui, si bien que les cellules B — celles qui produisent les anticorps — ont du mal à le détecter pendant l’infection ou après une vaccination standard.
Imiter le MPER sur de minuscules particules vaccinales
Les chercheurs ont conçu des vaccins dans lesquels des fragments synthétiques du MPER étaient ancrés de façon dense à la surface des liposomes, créant un environnement de type membrane qui ressemble mieux à la présentation du MPER sur le virus. À l’intérieur ou attachés à ces mêmes liposomes, ils ont également inclus de courts peptides « aides », qui sont des fragments de protéines reconnus par les cellules T CD4. Ces cellules T auxiliaires fournissent un soutien essentiel aux cellules B dans les centres germinatifs, les lieux d’entraînement du système immunitaire où les cellules productrices d’anticorps rivalisent, mutent et améliorent leur affinité. Une subtilité importante est que certains peptides aides, comme un peptide appelé LACK, sont eux-mêmes de fortes cibles pour les cellules B — c’est‑à‑dire que des anticorps se forment facilement contre eux et peuvent détourner l’attention du MPER.
Compétition entre cibles utiles et distrayantes
Lorsque des souris ont reçu une première injection contenant le MPER sur liposomes associé au peptide aide LACK, leur système immunitaire a monté une forte réponse contre LACK mais seulement une réponse plus faible et de faible affinité contre le MPER. Les mesures des cellules B des centres germinatifs et des liaisons d’anticorps ont montré que les cellules B spécifiques de LACK détenaient un avantage d’affinité intrinsèque ; elles ont surpassé les cellules B spécifiques du MPER pour obtenir l’aide des cellules T et ont dominé la réponse anticorps. Cela suggère que même dans un vaccin conçu pour mettre en avant le MPER, des épitopes hors cible attachés pour des raisons techniques — comme les peptides aides — peuvent devenir des « voleurs d’attention » immunologiques et compromettre la réponse souhaitée.
Utiliser des rappels mix-and-match pour recentrer le système immunitaire
L’équipe a ensuite testé des schémas d’amorçage‑renforcement « hétérologues », où les injections ultérieures modifiaient à la fois la forme du MPER et l’identité du peptide aide. Après un amorçage avec une formulation MPER/LACK, certains groupes de souris ont reçu des rappels qui remplaçaient les constructions MPER et substituaient LACK par des peptides aides alternatifs (HIV30 et OVA) moins dominants en tant que cibles B. Ces rappels mix-and-match ont fortement augmenté le nombre de plasmocytes à longue durée de vie spécifiques du MPER dans la moelle osseuse et ont accru les niveaux d’anticorps anti‑MPER et leur force de liaison, tout en réduisant les anticorps dirigés contre LACK. Un cartographie détaillée a montré que ces schémas ont orienté les anticorps vers des résidus MPER particuliers et amélioré la reconnaissance d’une protéine Env VIH complète à la surface des cellules — une étape importante vers la reconnaissance du virus réel, même si une neutralisation large n’a pas encore été atteinte.
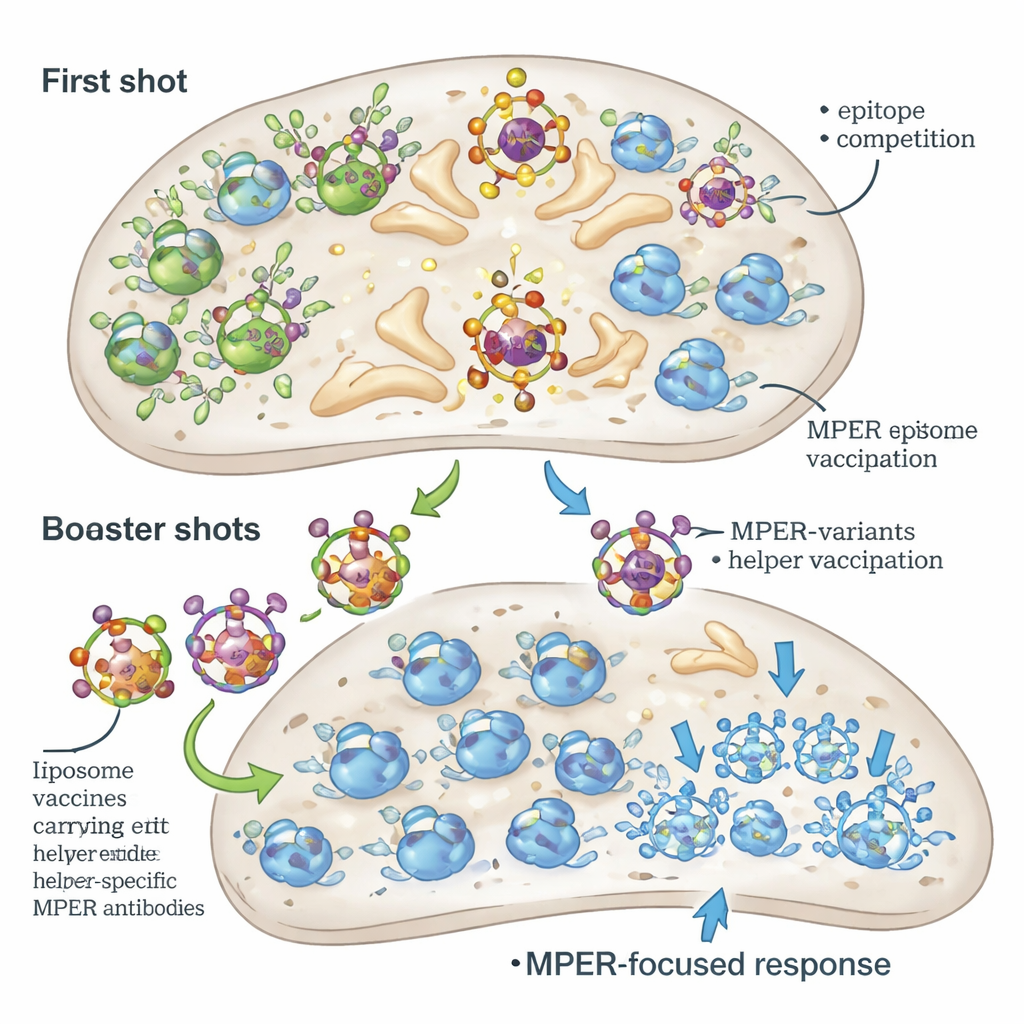
Équilibrer aide et compétition
Fait intéressant, la stratégie de rappel la plus efficace n’était pas simplement celle qui générait la plus grande réponse globale des cellules T auxiliaires. Les rappels qui continuaient d’utiliser LACK produisaient une forte activité des centres germinatifs mais favorisaient toujours les cellules B spécifiques de LACK au détriment du MPER. En revanche, des rappels avec des peptides aides alternatifs fournissaient une aide T cellulaire globale un peu plus faible mais réduisaient l’écart d’affinité entre les cellules B spécifiques du MPER et celles spécifiques des peptides aides, permettant aux cellules ciblant le MPER de mieux rivaliser. Lorsque les peptides aides étaient ancrés à la surface du liposome plutôt que simplement encapsulés, ils fournissaient une aide T robuste sans devenir des cibles B écrasantes, améliorant encore l’affinité des anticorps anti‑MPER.
Ce que cela signifie pour les futurs vaccins contre le VIH
Pour un lecteur non spécialiste, le message principal est que les vaccins doivent entraîner le système immunitaire non seulement à reconnaître une faiblesse virale, mais à la prioriser par rapport à de nombreuses autres cibles séduisantes. Cette étude montre qu’en choisissant et en alternant soigneusement les composants aides entre les injections — et en ajustant la façon dont les antigènes sont présentés sur des nanoparticules — les scientifiques peuvent atténuer les réponses distrayantes et amplifier les réponses rares et souhaitables contre la région conservée MPER. Bien que les anticorps murins produits ici ne neutralisent pas encore le VIH de manière large, ce travail trace des principes de conception concrets pour de futurs vaccins contre le VIH et d’autres vaccins contre des virus à évolution rapide : contrôler la compétition des épitopes, varier stratégiquement les rappels et associer une conception intelligente des immunogènes à des calendriers d’immunisation tout aussi réfléchis.
Citation: Khan, R.A., Chen, J., Donius, L. et al. Heterologous immunization modulates B-cell epitope competition between helper peptides and the MPER segment in MPER/liposome vaccines. npj Vaccines 11, 51 (2026). https://doi.org/10.1038/s41541-026-01371-6
Mots-clés: Vaccin contre le VIH, Anticorps MPER, Immunisation par liposomes, Renforcement hétérologue, Compétition des épitopes B