Clear Sky Science · fr
Surmonter la résistance aux ITK médiée par le niche vasculaire dans la leucémie myéloïde aiguë par l’inhibition de la miR-126
Pourquoi c’est important pour les patients atteints de cancer
La leucémie myéloïde aiguë (LMA) est l’un des cancers du sang les plus agressifs, et même avec des médicaments ciblés modernes de nombreux patients rechutent. Cette étude pose une question apparemment simple mais aux grandes implications : le problème ne vient-il pas seulement des cellules cancéreuses elles‑mêmes, mais aussi du « quartier » où elles vivent dans la moelle osseuse ? En construisant un modèle informatique détaillé fondé sur des données de laboratoire, les auteurs explorent comment de petits vaisseaux sanguins peuvent protéger les cellules souches leucémiques des médicaments — et comment bloquer un seul petit ARN peut démanteler cette protection.
La cachette secrète dans la moelle osseuse
La LMA prend naissance dans la moelle osseuse, où des blasts malins supplantent la production normale de sang. Dans cet essaim se cache une petite population de cellules souches leucémiques capables de s’auto‑renouveler et de survivre aux traitements, semant la rechute. Ces cellules souches ne flottent pas librement ; elles se nichent dans des poches spécialisées autour des petites artères et des capillaires, connues collectivement sous le nom de niche vasculaire. L’étude se concentre sur des patients dont les cellules leucémiques portent des mutations FLT3‑ITD, traitées par des inhibiteurs de tyrosine kinase (ITK). Bien que ces médicaments puissent réduire fortement la charge tumorale, de nombreux patients rechutent, ce qui suggère que certaines cellules sont dissimulées ou protégées.
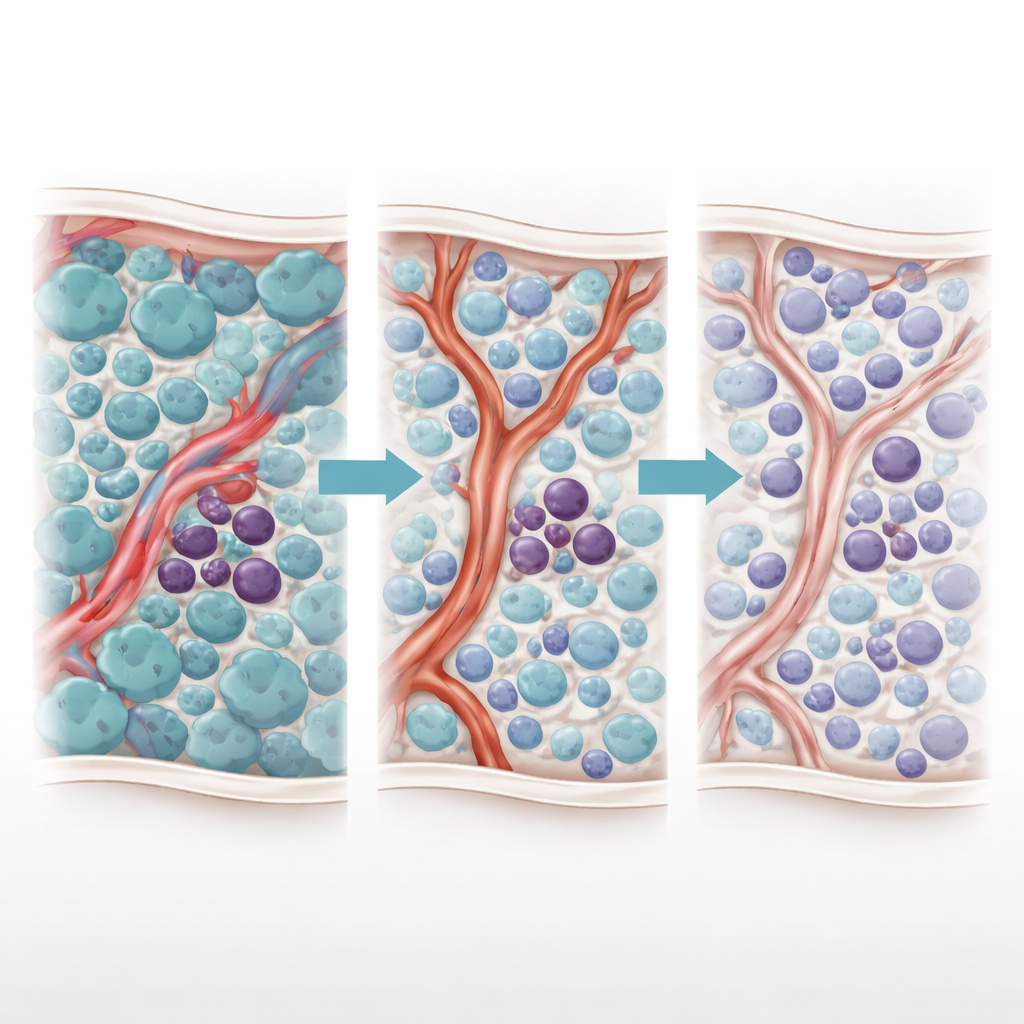
Un effet du traitement à double face
Les auteurs ont précédemment mis au jour un phénomène énigmatique de « Janus » — une réponse à deux visages au traitement par ITK. Lorsque les ITK éliminent les blasts à multiplication rapide, les niveaux d’une molécule inflammatoire, le TNF‑α, chutent. Cette baisse permet de façon inattendue aux cellules vasculaires voisines d’augmenter la production d’un petit ARN régulateur appelé miR‑126. Cette miR‑126 est transférée des cellules endothéliales aux cellules souches leucémiques, les poussant vers un état calme, non proliferatif, hautement résistant aux médicaments. Autrement dit, le traitement qui élimine la plupart des cellules cancéreuses remodèle la moelle osseuse de manière à abriter les plus dangereuses.
Construire une moelle osseuse virtuelle
Pour disséquer cette dynamique, l’équipe a créé un modèle computationnel à agents de la moelle osseuse atteinte de LMA. Chaque acteur clé — blasts, cellules souches leucémiques et cellules endothéliales tapissant les vaisseaux — est représenté comme un agent individuel suivant des règles biologiquement informées. Des molécules en diffusion telles que le TNF‑α, la miR‑126, l’ITK AC220 et un médicament bloquant la miR‑126 nommé miRisten se propagent dans le tissu simulé. Le modèle a été calibré avec des données d’imagerie murine qui cartographient des schémas vasculaires réels, y compris des zones riches ou pauvres en vaisseaux producteurs de miR‑126. Dans les simulations, le traitement standard par ITK reproduisait de façon fiable l’effet Janus : les blasts déclinaient, le TNF‑α chutait, la miR‑126 issue des vaisseaux augmentait, les cellules souches se retiraient dans des niches protectrices et la maladie rebondissait ensuite.
Désactiver le bouclier par un timing précis
Avec ce système virtuel, les chercheurs ont testé des moyens de briser le cercle vicieux. L’ajout simple de miRisten en même temps que l’ITK aidait mais ne guérissait que rarement la maladie dans le modèle. Une approche plus stratégique s’est avérée plus puissante : un court « prétraitement » par miRisten seul pour diminuer la miR‑126 vasculaire, suivi soit d’un ITK seul soit d’une thérapie combinée poursuivie. À travers de nombreux agencements vasculaires simulés, même quelques jours de prétraitement par miRisten avant le démarrage d’AC220 réduisaient ou éliminaient de façon spectaculaire la rechute tout en limitant l’exposition totale aux médicaments. Le modèle a également révélé que la proximité des cellules souches leucémiques par rapport aux vaisseaux influence fortement leur destin — les cellules nichées contre les vaisseaux gagnent la plus grande protection, sauf si la miR‑126 est bloquée.
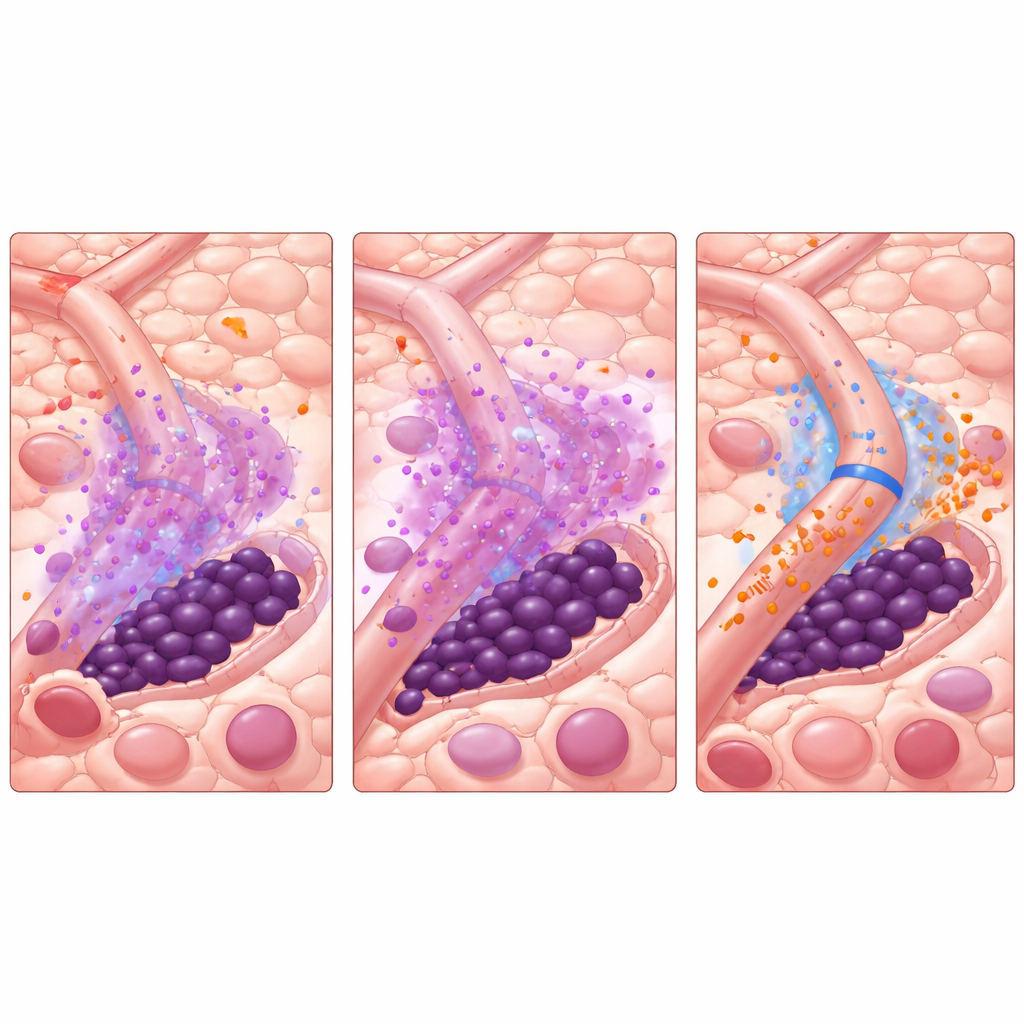
Ce que cela pourrait signifier pour les soins futurs
En termes simples, l’étude suggère que certaines cellules souches leucémiques survivent non pas parce que les ITK sont inefficaces, mais parce que les petits vaisseaux de la moelle osseuse basculent temporairement en mode « protecteur » pendant le traitement. En désactivant brièvement un signal unique, la miR‑126, avant d’administrer l’ITK, il pourrait être possible d’enlever ce bouclier, de forcer les cellules souches à sortir de leur cachette et de les rendre susceptibles d’être éliminées par les médicaments existants. Bien que ce travail repose sur des simulations informatiques ancrées dans des données de laboratoire — et non encore sur des essais cliniques — il propose une stratégie concrète : synchroniser un médicament ciblant le microenvironnement juste avant et pendant la thérapie standard. Si elle est validée, cette approche pourrait non seulement améliorer les résultats pour les personnes atteintes d’une LMA mutée FLT3, mais aussi inspirer des tactiques similaires dans d’autres cancers hématologiques et solides où le voisinage tumoral aide à échapper au traitement.
Citation: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Mots-clés: leucémie myéloïde aiguë, cellules souches leucémiques, microenvironnement de la moelle osseuse, résistance aux inhibiteurs de tyrosine kinase, inhibition de la miR-126