Clear Sky Science · fr
Développement d’un modèle sévère de syndrome de réalimentation chez le rat et modélisation mathématique de l’hypophosphatémie associée
Pourquoi recommencer à manger peut être dangereux
Lorsque des personnes ayant été gravement sous-nourries reçoivent enfin des aliments ou une nutrition intraveineuse, les médecins doivent agir avec prudence. Une arrivée soudaine de calories peut déclencher le « syndrome de réalimentation », une complication qui perturbe les équilibres minéraux et peut nuire au cœur, aux muscles et aux poumons. Un acteur clé est le phosphore, un minéral nécessaire à la production d’énergie dans chaque cellule. Cette étude a utilisé des rats et la modélisation informatique pour comprendre pourquoi le phosphore sanguin peut chuter aussi dramatiquement lors de la réalimentation, et comment mieux prévenir cette baisse dangereuse.
Un examen approfondi des problèmes de réalimentation
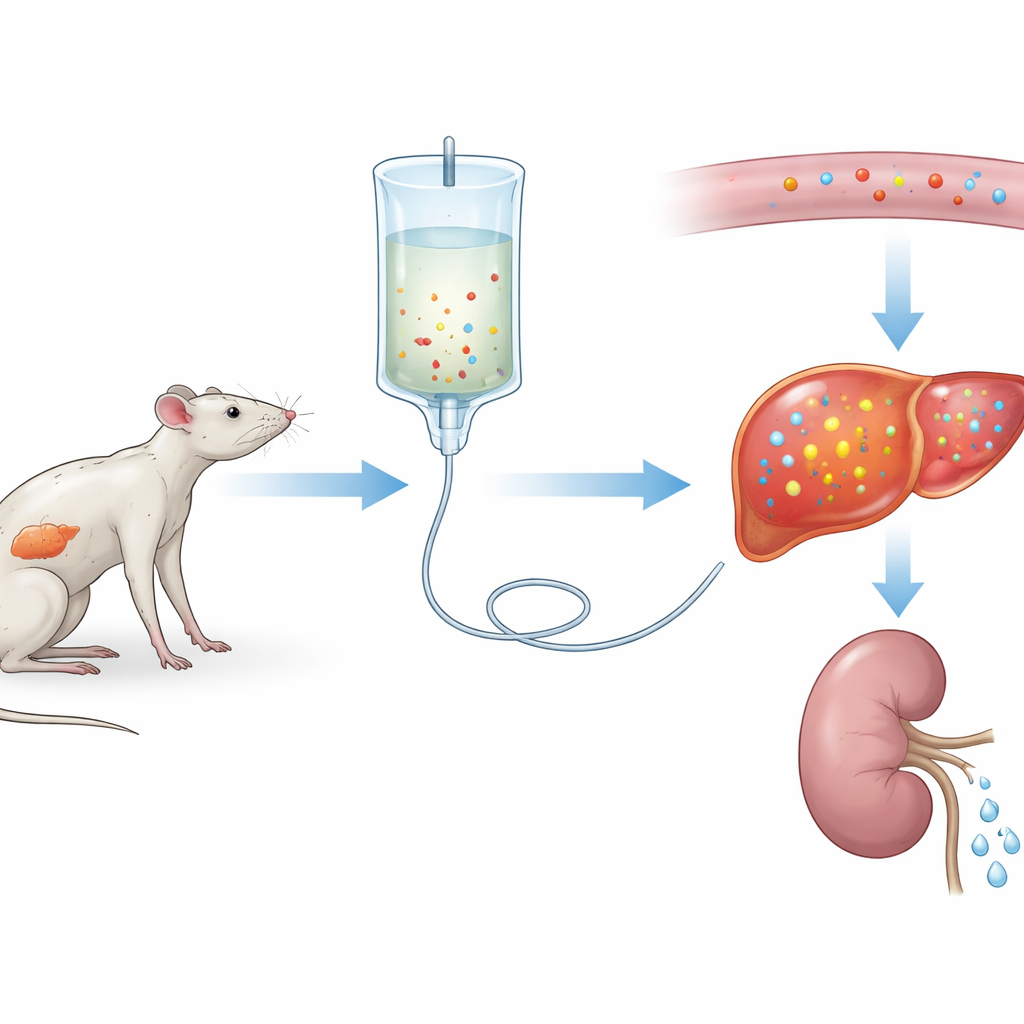
Les chercheurs ont d’abord mis au point une forme sévère de syndrome de réalimentation chez le rat. Pendant trois semaines, un groupe a reçu une alimentation normale tandis qu’un autre a eu très peu de protéines, simulant une sous-nutrition prolongée. Les deux groupes ont ensuite reçu la même nutrition intraveineuse pendant trois jours. Les rats alimentés pauvrement en protéines ont montré une chute abrupte du phosphore sanguin — environ 75 % — accompagnée de modifications d’autres électrolytes et de signes de lésions d’organes, en particulier du foie et des muscles. Ces changements ressemblaient à un syndrome de réalimentation sévère chez les patients, suggérant que l’équipe avait construit un modèle expérimental fidèle.
Que devient le phosphore pendant la réalimentation
Pour comprendre le déplacement du phosphore dans l’organisme au fil du temps, les scientifiques ont prélevé à plusieurs reprises du sang et des urines chez les mêmes rats. Ils ont constaté que le taux de phosphore sanguin chutait chez les animaux normaux et ceux carencés en protéines après le début de la réalimentation, mais la baisse était beaucoup plus profonde et durable dans le groupe sous-nutri. De manière surprenante, les reins réduisaient en réalité l’élimination du phosphore dans les urines juste après la réalimentation : le minéral n’était donc pas éliminé. Au contraire, le phosphore était attiré hors du sang vers les tissus, en particulier le foie, dont les réserves avaient été épuisées par des semaines de régime pauvre. Les calculs informatiques ont confirmé que les rats sous-alimentés démarraient avec beaucoup moins de phosphore intracellulaire puis l’absorbaient vigoureusement dès l’arrivée des nutriments.
L’insuline n’explique pas tout
Comme la réalimentation élève la glycémie et l’hormone insuline, les cliniciens ont longtemps imputé à l’insuline le transfert du phosphore vers les cellules. L’équipe a testé cette idée en atténuant la sécrétion d’insuline avec l’hormone somatostatine. Comme prévu, la glycémie a augmenté, mais la chute du phosphore sanguin s’est à peine améliorée. Parallèlement, les taux d’acides aminés libres — éléments constitutifs des protéines — ont augmenté. Dans une expérience distincte, les scientifiques ont retiré les acides aminés de la perfusion. Dans ce cas, les niveaux de phosphore sont restés beaucoup plus stables, et la chute sévère a été évitée, bien que les niveaux d’insuline fussent similaires. Ces résultats indiquent un effet combiné : l’insuline et les acides aminés, et non l’insuline seule, poussent les cellules à capter davantage de phosphore lors de la réalimentation.
Un réseau de contrôle caché dans le foie et les reins
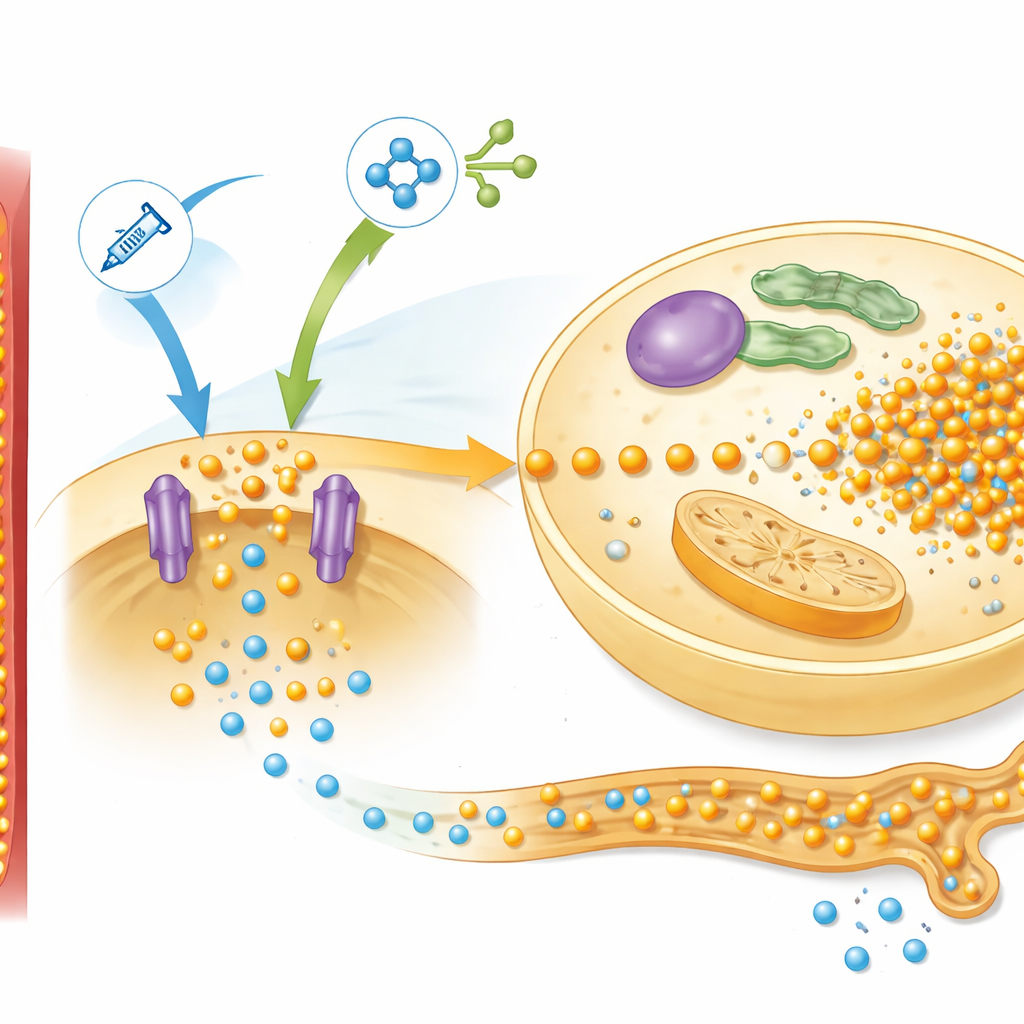
En creusant davantage, les chercheurs ont examiné les protéines hépatiques impliquées dans la détection des nutriments, en se focalisant sur une voie connue sous le nom de mTOR, qui répond à l’insuline et aux acides aminés. Chez les rats à faible apport protéique, la réalimentation a fortement activé cette voie et augmenté les niveaux d’un transporteur de phosphate appelé Pit2, qui aide les cellules hépatiques à capter le phosphore. Le schéma correspondait au comportement prédit par leur modèle mathématique, qui a regroupé ce réseau en un signal de contrôle unique qu’ils ont nommé « simTOR ». Le modèle nécessitait également un facteur de rétroaction distinct pour expliquer la façon dont les reins ajustent la perte de phosphore dans les urines. Les mesures d’une hormone osseuse, le FGF-23, correspondaient bien à ce rôle : ses niveaux ont chuté au début de l’alimentation, limitant l’excrétion du phosphore, puis ont divergé entre rats normaux et sous-nutris d’une manière qui reflétait le signal de rétroaction simulé.
Utiliser les mathématiques pour tester des stratégies de prévention
En ajustant différentes commandes dans leur modèle informatique, les auteurs ont pu poser des questions « et si » difficiles ou risquées à tester directement chez des patients. L’analyse a mis en évidence trois influences majeures sur la profondeur et la récupération de la baisse du phosphore : le phosphore intracellulaire initial, la force du système d’absorption piloté par mTOR, et le taux d’apport en phosphore via la nutrition. Les simulations ont suggéré qu’ajouter une grande quantité de phosphate au moment de la réalimentation serait difficile à équilibrer en toute sécurité. En revanche, administrer du phosphore supplémentaire avant la réalimentation — permettant aux organes de reconstituer discrètement leurs réserves internes — pourrait atténuer la chute ultérieure des taux sanguins. Diminuer la charge en acides aminés, en particulier ceux qui activent fortement mTOR et l’insuline, semblait également protecteur dans les expériences animales.
Ce que cela signifie pour les patients
Pour les personnes à risque de syndrome de réalimentation — comme celles souffrant de troubles alimentaires de longue date ou de grande fragilité — ce travail suggère que le danger ne provient pas uniquement d’un pic de glycémie. Les organes affamés abordent la réalimentation avec des réservoirs de phosphore vides, puis, sous la poussée combinée de l’insuline et des acides aminés, absorbent rapidement le minéral du sang tandis que les reins le retiennent brièvement. Le résultat est une pénurie circulatoire aiguë et temporaire qui peut endommager des tissus vitaux. Le modèle rat et le cadre mathématique développés ici ouvrent la voie à des mesures de prévention plus ciblées : usage précoce et prudent de suppléments de phosphore, contrôle attentif d’apports riches en acides aminés, et attention aux hormones régulant l’excrétion rénale. Ensemble, ces approches peuvent aider les cliniciens à réalimenter plus sûrement les patients vulnérables.
Citation: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Mots-clés: syndrome de réalimentation, hypophosphatémie, métabolisme du phosphore, signalisation mTOR, nutrition parentérale