Clear Sky Science · fr
FBA spatiale révèle des niches Warburg hétérogènes dans les tumeurs rénales et la consommation de lactate dans le cancer colorectal
Pourquoi le métabolisme tumoral dans l’espace compte
Les cellules cancéreuses ne se comportent pas toutes de la même façon, même au sein d’une seule tumeur. Certaines vivent près des vaisseaux sanguins, d’autres dans des zones profondes mal irriguées, et ces emplacements conditionnent la façon dont elles obtiennent et utilisent l’énergie. Cette étude présente une nouvelle manière de lire cette « carte métabolique » cachée à partir de données spatiales d’expression génique de pointe. Ce faisant, les auteurs mettent au jour des schémas surprenants concernant la gestion d’une molécule clé, le lactate, remettant en question l’idée classique selon laquelle les cancers se contentent d’évacuer le lactate comme déchet.
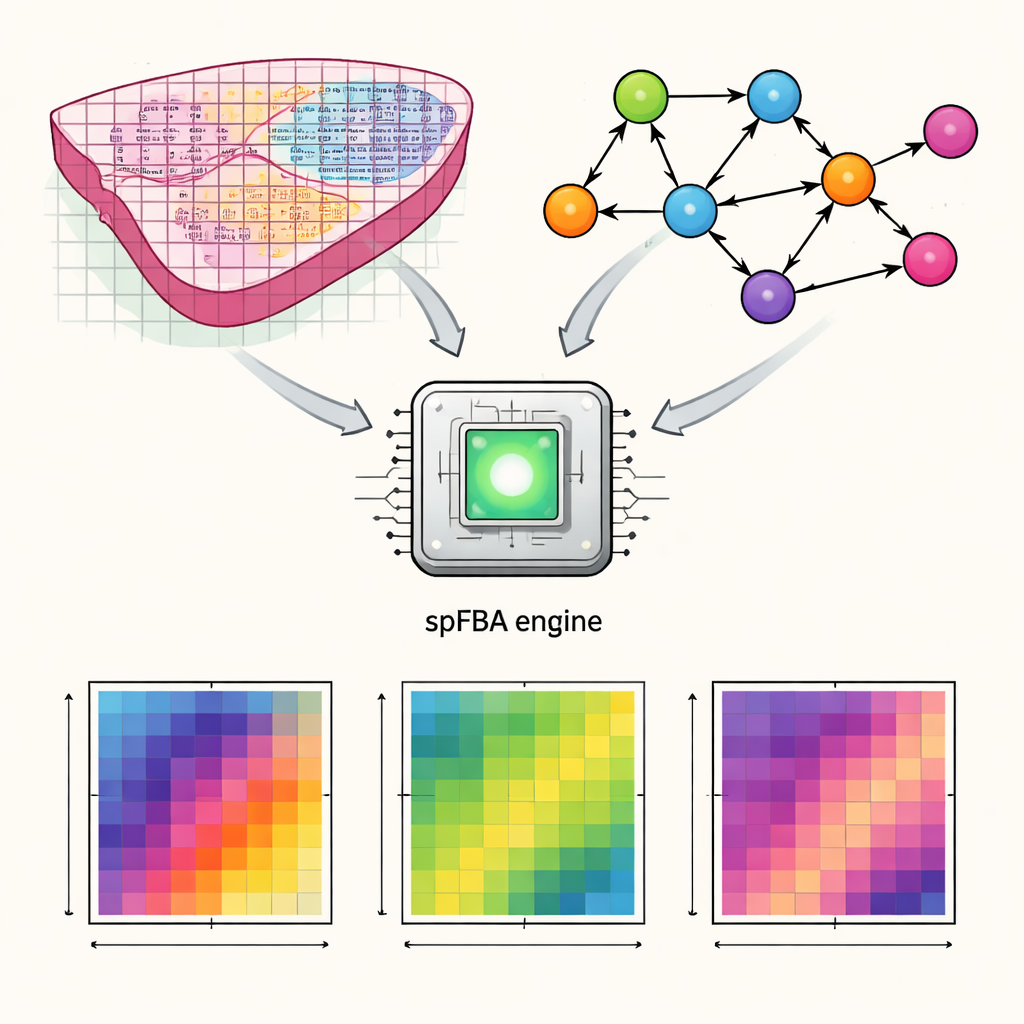
Transformer des cartes géniques en activité métabolique
Les auteurs ont développé un cadre computationnel appelé Flux Balance Analysis spatiale, ou spFBA. Les technologies de transcriptomique spatiale mesurent quelles gènes sont actifs en des milliers de petits points à travers une coupe fine de tissu. spFBA combine ces cartes d’activité génique spatiale avec des modèles détaillés du métabolisme humain, qui décrivent comment des nutriments comme le glucose, l’oxygène et les acides aminés sont transformés à l’intérieur des cellules. Plutôt que de supposer que chaque région du tissu partage le même objectif métabolique, spFBA traite chaque point de manière indépendante, explorant quels profils de réactions sont possibles localement selon les lois de la chimie et de la conservation de la masse. Le résultat est un ensemble de « scores d’enrichissement de flux » qui indiquent, pour chaque emplacement, dans quelle mesure différentes réactions métaboliques sont susceptibles de s’écouler et dans quelle direction.
Tester la méthode sur des tumeurs rénales
Pour vérifier que spFBA donne des résultats biologiquement pertinents, l’équipe a d’abord étudié le carcinome à cellules claires du rein, un cancer rénal connu pour sa dépendance marquée à la glycolyse et à la libération de lactate, phénomène appelé effet Warburg. En utilisant des données spatiales publiées provenant de dix échantillons de tumeur rénale, ils ont évalué si les motifs métaboliques prédits correspondaient à l’organisation tissulaire connue. Ils ont constaté que les points regroupés selon leurs flux métaboliques inférés correspondaient bien à l’organisation histologique observée au microscope et aux clusters basés uniquement sur l’expression génique. De manière importante, spFBA a retrouvé le contraste métabolique attendu entre tumeur et rein normal : les régions tumorales montraient une utilisation plus élevée du glucose, une production de biomasse plus forte (un proxy de la croissance cellulaire) et une sécrétion robuste de lactate. En parallèle, l’utilisation d’oxygène restait substantielle, révélant que différentes parties d’une même tumeur peuvent mêler fermentation et respiration selon l’irrigation locale.
Les cancers colorectaux offrent une autre histoire du lactate
Les chercheurs ont ensuite appliqué le même pipeline à de nouveaux jeux de données spatiales à haute résolution provenant d’un patient porteur d’un cancer colorectal primitif et de métastases hépatiques appariées, ainsi qu’à un ensemble colorectal public indépendant généré avec une autre technologie. Ici, les résultats furent nettement différents. Plutôt que d’exporter le lactate comme déchet, la plupart des régions du cancer colorectal — tant dans la tumeur colique d’origine que dans les métastases hépatiques — furent prédites importer du lactate depuis leur environnement. Les cellules stromales du tissu de soutien adjacent tendaient à libérer de faibles quantités de lactate, tandis que les cellules tumorales se comportaient en consommateurs importants. En retraçant les schémas de flux au niveau des réactions, les auteurs montrent que ces cellules métastatiques ne se contentent pas de brûler le lactate dans le cycle énergétique mitochondrial habituel. Elles convertissent plutôt le lactate en éléments de construction qui alimentent des voies de synthèse des lipides et d’autres composants nécessaires à la croissance cellulaire, un « pseudo-effet Warburg inverse » où le lactate devient matière première pour la biosynthèse.
Des niches métaboliques et la frontière tumeur-stroma
Parce que spFBA conserve la disposition spatiale, il peut localiser précisément où se produisent des échanges métaboliques particuliers. Dans les tumeurs rénales, la méthode a révélé des « voisinages » métaboliques coexistants : des interfaces mieux oxygénées et riches en sang où les cellules cancéreuses respirent et fermentent, et des noyaux plus profonds et mal vascularisés qui reposent davantage sur la fermentation. Dans les métastases hépatiques colorectales, spFBA a mis en évidence des contrastes marqués à la frontière entre tumeur et stroma, où la gestion du glutamate et du lactate changeait de sens, suggérant un échange intense au front invasif. Dans tous les jeux de données, les flux prédits liés à la croissance corrélaient avec des mesures indépendantes basées sur les gènes de la prolifération, soutenant le réalisme biologique du modèle. Surtout, le même algorithme prédit la sécrétion de lactate dans le cancer rénal mais l’absorption de lactate dans le cancer colorectal, indiquant que les différences observées proviennent des données et non d’un biais intégré au modèle.
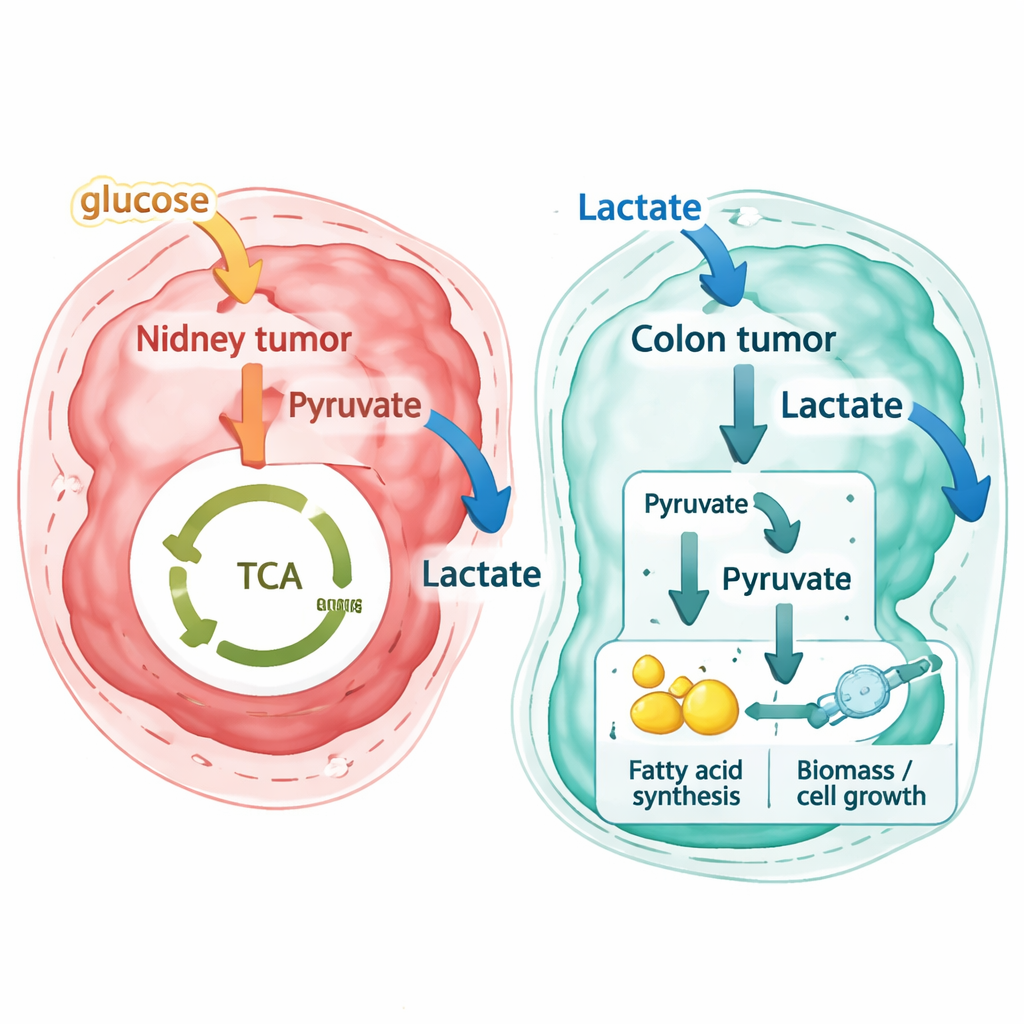
Ce que cela signifie pour la compréhension et le traitement du cancer
Pour le grand public, le message clé est que le métabolisme du cancer n’est pas seulement anormal — il est aussi fortement localisé. Une même tumeur peut abriter plusieurs niches métaboliques, et des tumeurs d’apparence similaire dans des organes différents peuvent utiliser les mêmes molécules de façon opposée. Ce travail montre qu’en superposant l’expression génique spatiale sur des modèles métaboliques détaillés, les chercheurs peuvent déduire où les tumeurs sont susceptibles d’être avides de nutriments particuliers comme le lactate. Dans le cancer colorectal, la découverte que les cellules tumorales consomment largement le lactate et le réorientent vers des processus liés à la croissance soulève de nouvelles questions sur la façon dont l’alimentation, le microbiote intestinal et le métabolisme hépatique influent sur la progression de la maladie, et sur l’opportunité de cibler l’utilisation du lactate pour rendre ces tumeurs plus sensibles aux thérapies.
Citation: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Mots-clés: métabolisme du cancer, transcriptomique spatiale, lactate, effet Warburg, cancer colorectal