Clear Sky Science · fr
Modélisation in silico de la différenciation de l’endoderme antérieur en progéniteurs épithéliaux pulmonaires
Transformer des cellules souches en cellules bâtisseuses du poumon
Les scientifiques apprennent à persuader les cellules souches d’un patient de devenir du tissu pulmonaire de remplacement, ce qui pourrait un jour réparer des lésions causées par des maladies comme la BPCO, la fibrose ou des infections sévères. Cet article examine comment des chercheurs ont utilisé la modélisation informatique pour cartographier et affiner une étape cruciale de ce processus : transformer un type cellulaire intermédiaire, l’endoderme antérieur, en progéniteurs épithéliaux pulmonaires précoces — les cellules de départ qui peuvent éventuellement former les voies aériennes et les alvéoles pulmonaires.
Pourquoi les cellules « starter » pulmonaires sont importantes
Les cellules souches pluripotentes induites humaines (iPSC) peuvent être reprogrammées à partir de tissus adultes puis guidées vers de nombreux organes. Pour construire du tissu pulmonaire, ces cellules traversent d’abord plusieurs étapes développementales. L’une d’elles est l’endoderme antérieur, une couche qui donne normalement naissance à des parties des systèmes respiratoire et digestif chez l’embryon. À partir de là, avec les signaux chimiques appropriés, les cellules peuvent devenir des progéniteurs épithéliaux pulmonaires, qui portent des marqueurs pulmonaires précoces et peuvent ensuite mûrir en cellules spécialisées des voies aériennes ou des alvéoles. Parce que les thérapies cellulaires futures nécessiteront des milliards de ces cellules, les chercheurs ont besoin de méthodes pour augmenter de manière fiable les rendements et adapter les protocoles à différentes lignées cellulaires de patients sans essais‑erreurs interminables au laboratoire.
Construire une version virtuelle de la différenciation cellulaire
L’équipe a étendu un cadre mathématique antérieur pour construire ce qui est, à leur connaissance, le premier modèle au niveau de la population de cette transition spécifique de l’endoderme vers les progéniteurs pulmonaires. Ils ont considéré deux manières de représenter les cellules : une version simple ne suivant que le nombre total de cellules vivantes, et une version plus détaillée qui suit séparément les cellules d’endoderme antérieur et les progéniteurs pulmonaires. Dans les deux cas, le modèle suit aussi le glucose et le lactate dans le milieu de culture, représentant nutriments et déchets. En utilisant des outils de biologie des systèmes, les chercheurs ont construit de nombreuses équations candidates pour décrire la croissance, la mort et la différenciation des cellules, puis ont appliqué des tests d’identifiabilité pour éliminer les modèles dont les paramètres ne pouvaient jamais être déterminés, même avec des données parfaites.
Concevoir des expériences plus intelligentes avec le modèle
Plutôt que de se contenter d’ajuster les modèles aux données disponibles, les chercheurs ont laissé le modèle guider la façon de réaliser de nouvelles expériences. Ils ont utilisé des données simulées pour déterminer à quelle fréquence il serait nécessaire de mesurer les effectifs cellulaires et les niveaux de nutriments afin d’estimer précisément les paramètres du modèle, en équilibrant précision statistique et coûts et travail liés aux prélèvements fréquents. Cela les a conduits à un plan pratique : mesures quotidiennes du glucose et du lactate, et comptages cellulaires tous les un à deux jours, sous quatre conditions variant l’intensité du fractionnement des cultures au jour 10 et le fait de renouveler ou non le milieu de croissance quotidiennement. Ils ont ensuite réalisé ces expériences, mesurant à la fois la population cellulaire totale et, par cytométrie en flux, les fractions restant endoderme ou étant devenues progéniteurs pulmonaires.
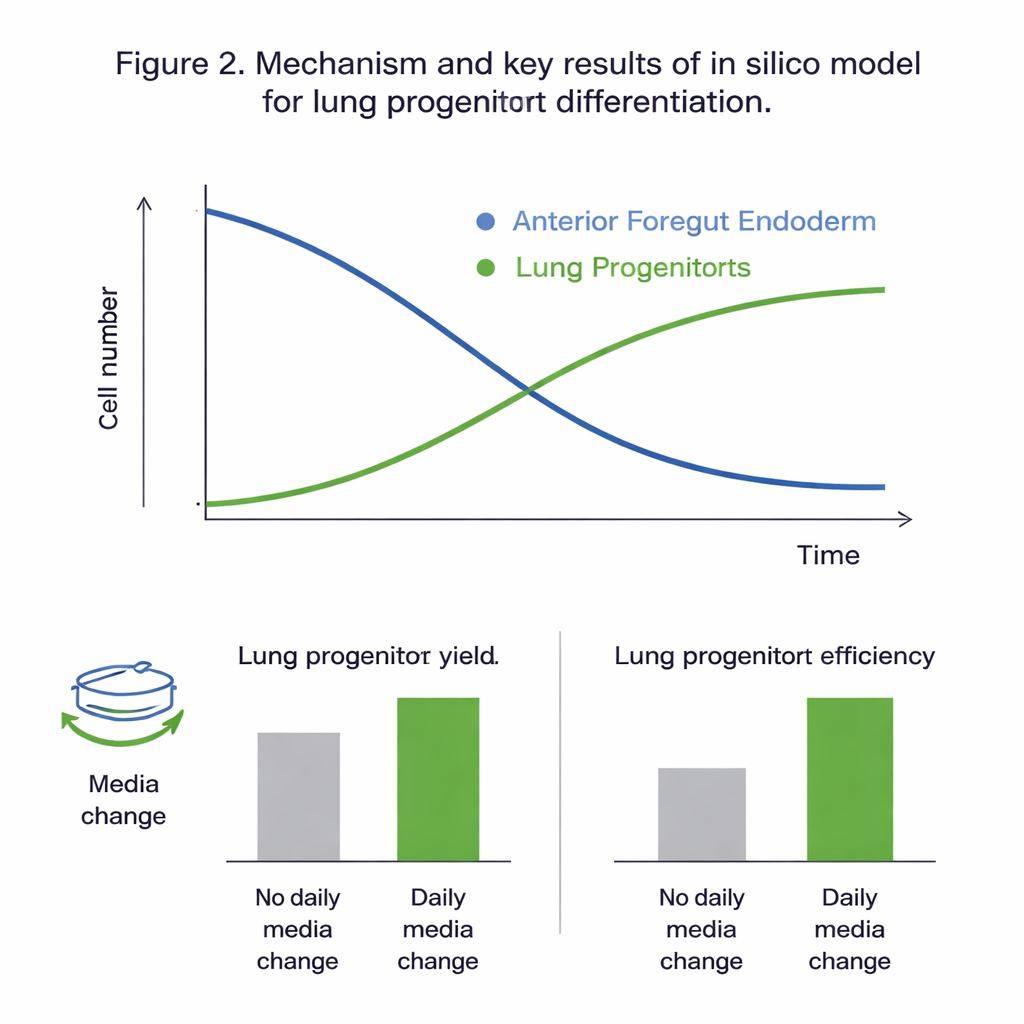
Ce que les expériences virtuelles ont révélé
L’ajustement de tous les modèles candidats aux données expérimentales a montré que le modèle à deux populations, qui suit séparément les cellules d’endoderme et les progéniteurs pulmonaires, pouvait être calibré de manière fiable et décrivait le mieux le comportement observé. Les contrôles statistiques ont indiqué que, sur la fenêtre temporelle étudiée (jours 11 à 15 du protocole), la dynamique était principalement entraînée par la prolifération et la différenciation des cellules d’endoderme, tandis que la prolifération des progéniteurs pulmonaires eux‑mêmes contribuaient peu. Une analyse de sensibilité globale a renforcé ce constat, mettant en évidence les taux de croissance, de mort et de différenciation des cellules d’endoderme — et l’influence du glucose — comme principaux leviers contrôlant le résultat. Le modèle calibré a reproduit des données non utilisées pour la calibration avec des erreurs comparables à la variabilité naturelle des expériences, suggérant qu’il était suffisamment précis pour explorer des scénarios « what‑if » in silico.
Optimiser les renouvellements de milieu et le fractionnement des cellules
Avec un système virtuel fiable en main, l’équipe a testé comment deux choix pratiques de protocole affectent les résultats : le degré de dilution de la culture (le ratio de fractionnement) au jour 10, et le fait de remplacer quotidiennement le milieu de croissance. Les simulations ont prédit que les changements quotidiens de milieu doublent presque le nombre de progéniteurs pulmonaires et le rendement par cellule de départ, principalement en évitant l’épuisement des nutriments et l’accumulation de déchets et de molécules de signalisation instables. Les expériences ont été en bon accord avec ces prédictions. Le modèle a également suggéré que des ratios de fractionnement plus élevés — répartir les cellules plus clairsemées au jour 10 — améliorent le « rendement par cellule d’entrée » d’environ un quart, même si cela réduit le nombre absolu de cellules. Dans les deux cas, ces modifications ont eu peu d’effet sur la proportion finale de progéniteurs pulmonaires dans la culture, influant surtout sur le nombre de cellules pouvant être produites efficacement.
Que signifie cela pour les thérapies pulmonaires futures
Pour un non‑spécialiste, le message clé est que les auteurs ont construit une sorte de simulateur de vol pour une étape critique de la culture de cellules pulmonaires à partir de cellules souches. En combinant des expériences soigneusement conçues avec une modélisation mathématique rigoureuse, ils montrent comment des choix protocolaires simples — comme la fréquence de renouvellement du milieu de culture et la densité d’ensemencement — peuvent influer de manière drastique sur le nombre de cellules bâtisseuses du poumon produites, sans en modifier la qualité. Ce type de modélisation in silico peut aider à rationaliser les protocoles futurs, réduire les tâtonnements expérimentaux et, en fin de compte, soutenir une production plus fiable et évolutive de progéniteurs pulmonaires pour la recherche, la modélisation des maladies et, éventuellement, les thérapies régénératives.
Citation: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Mots-clés: cellules progénitrices pulmonaires, cellules souches pluripotentes induites, modélisation in silico, différenciation cellulaire, médecine régénérative