Clear Sky Science · fr
Association des altérations du nombre de copies avec le paysage transcriptomique immunitaire dans le cancer
Pourquoi nos gènes comptent pour l’immunothérapie du cancer
L’immunothérapie du cancer agit en aidant le système immunitaire à reconnaître et à attaquer les tumeurs, mais seule une minorité de patients en tire un bénéfice durable. Cette étude pose une question fondamentale aux grandes conséquences cliniques : comment le chaos génétique à l’intérieur des cellules tumorales – en particulier les gains et pertes d’ADN de grande ampleur appelés altérations du nombre de copies – façonne-t-il la réaction immunitaire contre le cancer, et peut-on lire ces effets à partir des profils d’activité génique ?
Une vue panoramique des données sur le cancer
Pour aborder cette question, les chercheurs ont rassemblé une collection immense de 294 159 profils d’activité génique provenant de tumeurs et d’autres tissus. Ces profils, issus de plusieurs grandes bases de données publiques, captent quels gènes sont activés ou réprimés dans des milliers d’échantillons couvrant de nombreux types de cancer et conditions expérimentales. Plutôt que d’examiner les gènes un par un, l’équipe a utilisé une méthode mathématique pour décomposer chaque profil en « composants » sous-jacents – des motifs récurrents de gènes qui tendent à monter ou descendre ensemble, chacun reflétant un processus biologique comme une réponse immunitaire ou l’effet d’une altération de l’ADN.
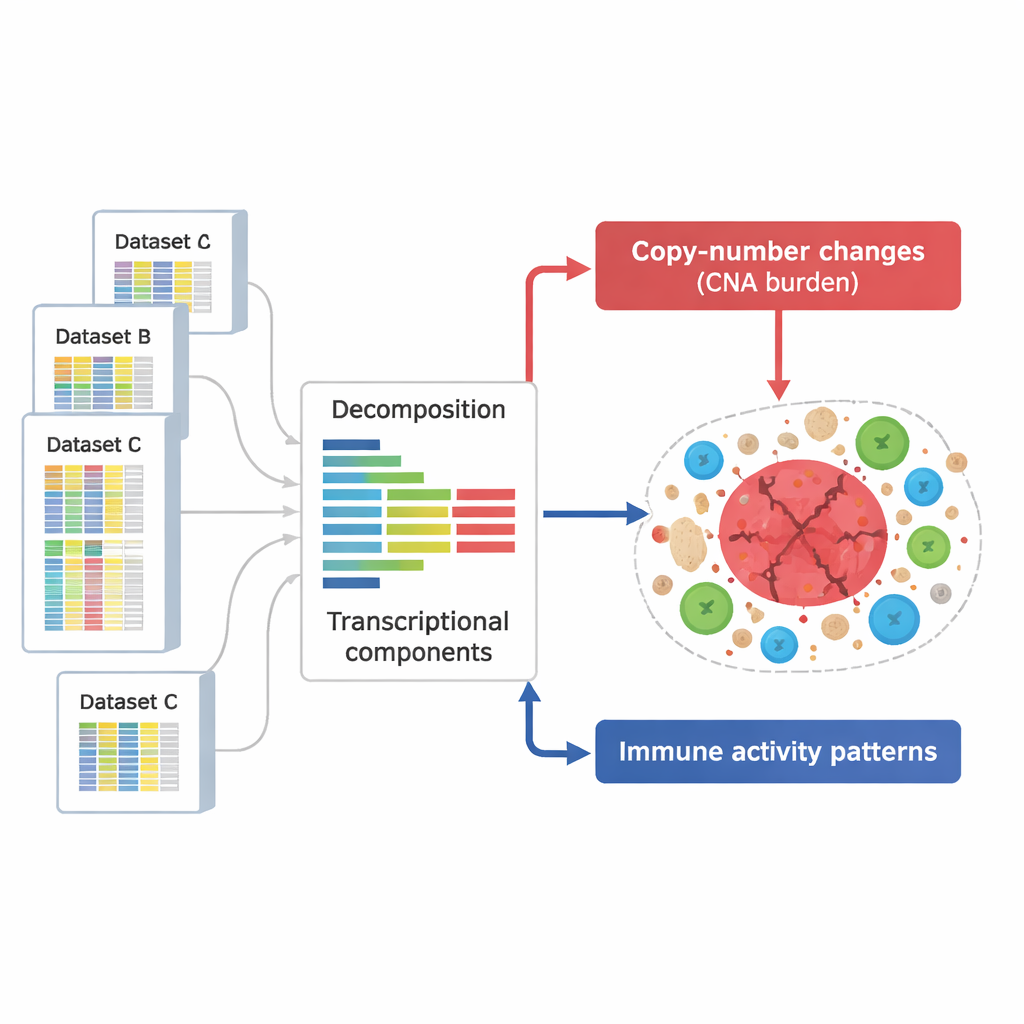
Séparer les signaux de dommages à l’ADN des signaux immunitaires
À partir de ces composants, les scientifiques ont défini deux groupes clés. Un groupe capturait les effets des altérations du nombre de copies – des segments chromosomiques qui sont fréquemment gagnés ou perdus dans les cellules cancéreuses. Ces motifs couvraient presque l’ensemble du génome, indiquant que la plupart des régions touchées par ces altérations laissaient une empreinte détectable sur l’activité génique. Un second groupe de composants était enrichi en gènes impliqués dans les fonctions immunitaires, telles que l’activation des cellules T, l’activité des cellules NK et la présentation d’antigènes. Au total, ils ont identifié 657 composants liés à l’ADN et 283 composants liés à l’immunité, dont beaucoup pouvaient être reproduits dans des jeux de données et des technologies indépendants, ce qui suggère qu’ils représentent des caractéristiques robustes et générales de la biologie tumorale.
Relier les motifs à la réponse au traitement
L’équipe a ensuite cherché à savoir si ces motifs liés à l’immunité pouvaient aider à prédire qui répond aux inhibiteurs des points de contrôle immunitaire, une classe majeure de médicaments d’immunothérapie anticancéreuse. En utilisant des données de 13 études cliniques couvrant 1 167 patients atteints de sept types de cancer, ils ont entraîné des modèles informatiques pour distinguer les répondeurs des non-répondeurs uniquement à partir de l’activité des composants immunitaires dans des échantillons tumoraux pré-traitement. Certains modèles ont montré de bonnes performances même lorsqu’ils étaient testés sur des groupes de patients complètement indépendants ; par exemple, un modèle entraîné sur une cohorte de cancer du sein a correctement prédit les réponses dans une cohorte séparée de cancer du sein et a montré une performance utile dans plusieurs autres cancers. Un petit ensemble de motifs immunitaires, y compris ceux liés aux réponses à l’interféron, aux cellules NK et à l’activation des cellules T, a le plus contribué à ces prédictions.
Comment le chaos génétique remodelé l’immunité tumorale
Avec ce cadre en place, les chercheurs ont systématiquement relié la charge globale d’altérations du nombre de copies – une mesure de l’étendue des gains et pertes d’ADN d’une tumeur – à l’activité de chaque motif immunitaire à travers de nombreux types de cancer. La plupart des motifs immunitaires montraient une relation inverse : les tumeurs avec une forte charge d’altérations de l’ADN avaient tendance à présenter une faible activité des composants associés à des fonctions immunitaires bénéfiques, comme la présentation d’antigènes et l’infiltration par des cellules immunitaires clés. Cependant, une minorité notable de motifs évoluait en sens inverse. Les tumeurs à forte charge d’altérations affichaient souvent des signaux accrus provenant de types cellulaires immunosuppresseurs, y compris des cellules T régulatrices et certains macrophages, ainsi que des cellules inflammatoires qui peuvent favoriser la croissance tumorale plutôt que sa destruction. Des analyses spatiales de coupes tumorales ont confirmé que les régions avec de fortes modifications de l’ADN coïncidaient fréquemment avec une faible activité des motifs immunitaires utiles et avec des zones « excluant l’immunité » où les cellules immunitaires restaient cantonnées aux marges tumorales.
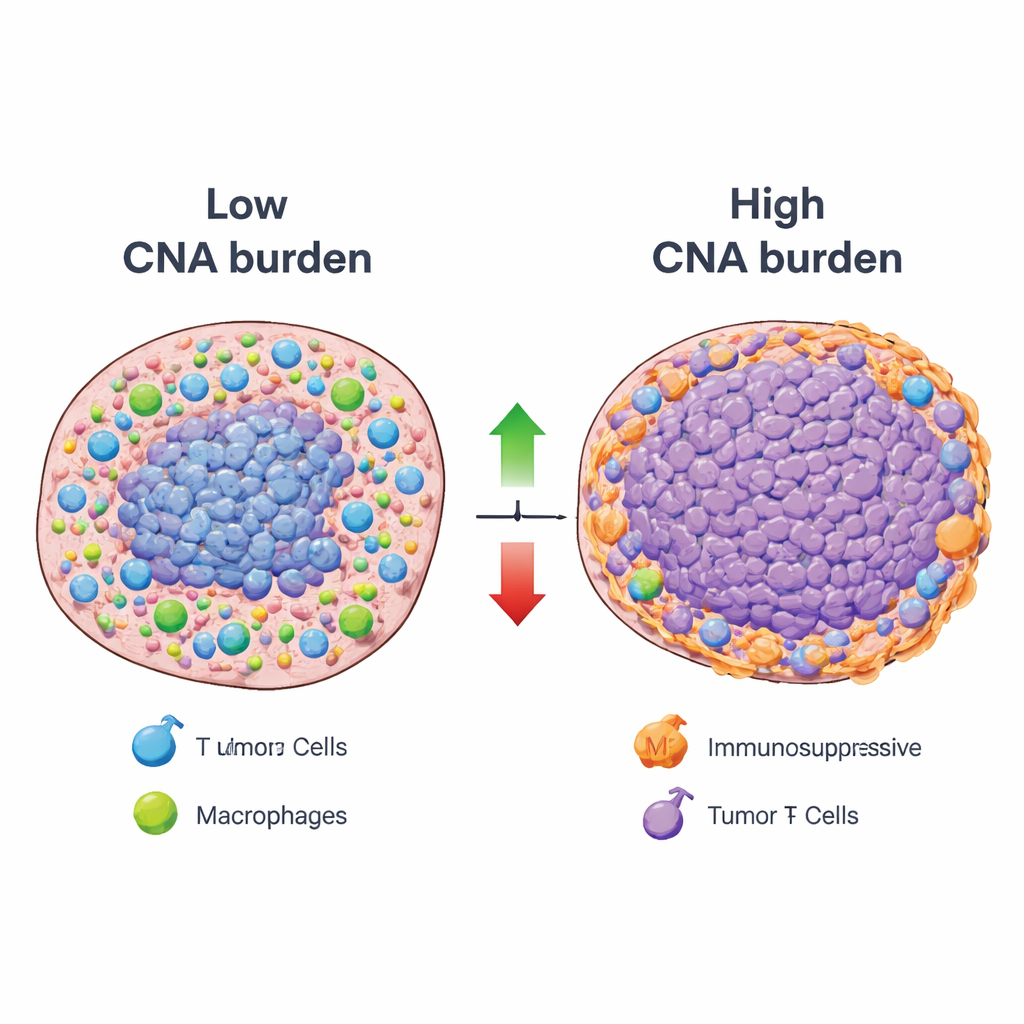
Ce que cela signifie pour les traitements futurs du cancer
En termes clairs, l’étude montre que les tumeurs chargées de gains et pertes d’ADN à grande échelle tendent à atténuer les réponses immunitaires utiles et à favoriser des environnements immunitaires suppressifs ou promoteurs de la tumeur. Pourtant, elles ne sont pas immunologiquement silencieuses ; au contraire, elles affichent des états immunitaires spécifiques et récurrents qui peuvent être vulnérables à des thérapies ciblées, comme des médicaments bloquant la signalisation IL‑17 ou IL‑23 ou des stratégies qui reprogramment certains macrophages. En cartographiant ces relations ADN–immunité à travers les cancers et en rendant la ressource disponible publiquement, ce travail offre un guide détaillé expliquant pourquoi certaines tumeurs génétiquement instables résistent aux immunothérapies actuelles et suggère de nouvelles stratégies de traitements combinés pour aider le système immunitaire à surmonter cette résistance.
Citation: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Mots-clés: immunothérapie du cancer, altérations du nombre de copies, microenvironnement tumoral, inhibiteurs des points de contrôle immunitaire, transcriptomique