Clear Sky Science · fr
Inférence par simulation des dynamiques de migration cellulaire dans des environnements spatiaux complexes
Comment les cellules immunitaires se frayent un chemin dans des tissus encombrés
Nos cellules immunitaires doivent souvent se faufiler à travers des tissus denses et labyrinthiques pour atteindre les foyers d’infection ou les nœuds lymphatiques. Cette étude pose une question apparemment simple mais aux grandes implications : comment ces cellules naviguent‑elles dans des environnements aussi encombrés, et comment peut‑on inférer de manière fiable leurs comportements à partir de données microscopiques bruitées ? En combinant des « labyrinthes » de laboratoire précisément conçus avec des simulations informatiques avancées et des outils d’apprentissage automatique modernes, les auteurs présentent une nouvelle façon de décoder les règles qui guident le mouvement cellulaire dans des milieux complexes.
Construire un minuscule labyrinthe pour les cellules immunitaires
Pour étudier comment l’environnement façonne le mouvement, les chercheurs se sont concentrés sur les cellules dendritiques — sentinelles du système immunitaire qui doivent migrer des tissus périphériques vers les nœuds lymphatiques, guidées par des attractifs chimiques appelés chimiokines. Ils ont fabriqué une puce micro‑usinée : une « forêt de piliers » plate composée de poteaux régulièrement espacés en caoutchouc de silicone (PDMS), avec des interstices étroits de 10 micromètres qui imitent les espaces serrés des tissus réels. Un côté de la puce a été chargé de dizaines de milliers de cellules dendritiques ; le côté opposé contenait une source de la chimiokine CCL19, créant un gradient stable à travers les piliers. À l’aide de la microscopie en mode time‑lapse, ils ont suivi les noyaux de cellules individuelles toutes les 30 secondes pendant qu’elles tentaient de se diriger vers la source de chimiokine. 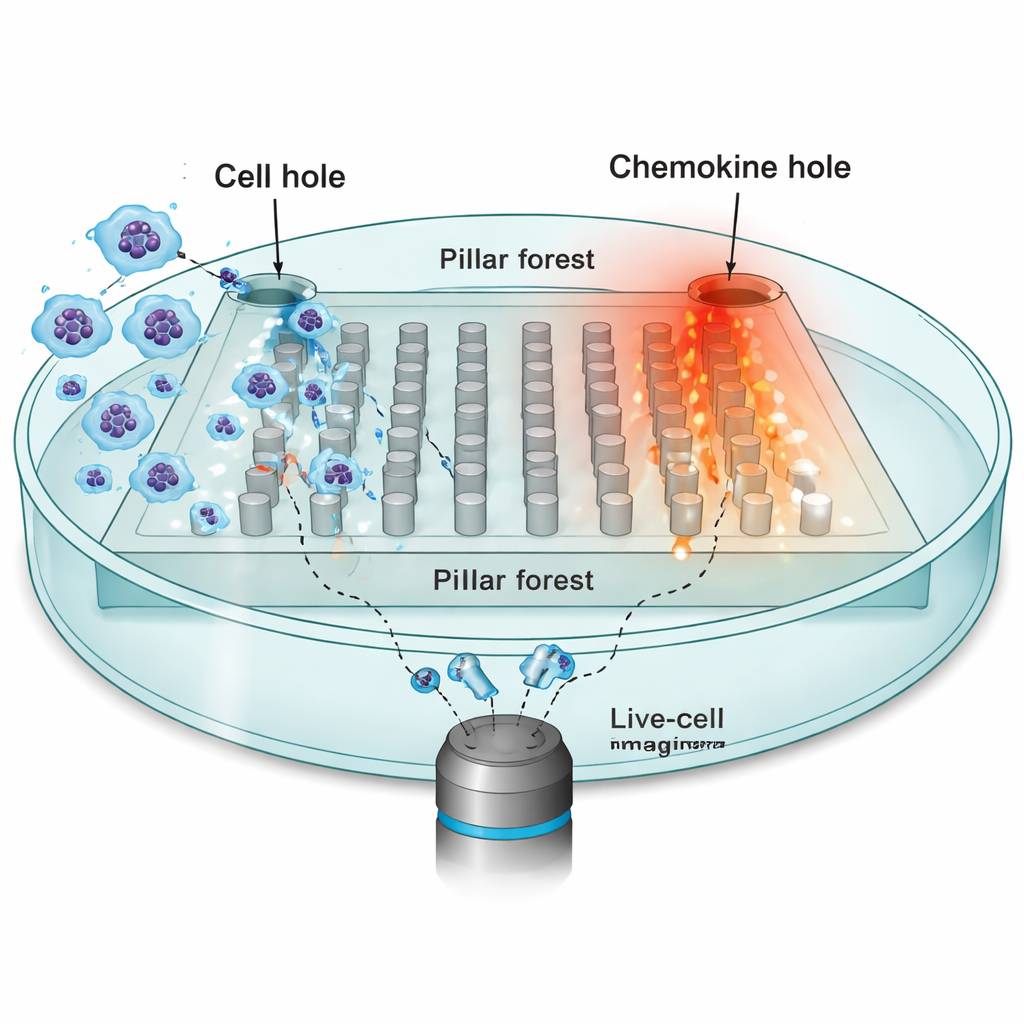
Transformer la biologie en expérience virtuelle
Pour donner du sens à cette diversité, l’équipe a construit un modèle computationnel détaillé de la migration cellulaire en utilisant un cadre connu sous le nom de modèle de Potts cellulaire. Plutôt que de traiter une cellule comme un point simple, cette approche représente chaque cellule comme une tache étendue sur une grille, lui permettant de changer de forme, de se faufiler entre les piliers et de répondre à des signaux chimiques. Le modèle inclut quatre ingrédients clés : l’intensité de l’attraction de la cellule par le gradient de chimiokine (mdir), son degré de persistance dans la direction de mouvement actuelle (mrand), la fréquence de réorientation (capturée par un taux λ), et sa taille effective (a). En ajustant ces paramètres et en exécutant des simulations, le modèle produit des trajectoires synthétiques qui peuvent être comparées directement aux chemins enregistrés dans la forêt de piliers.
Pourquoi les mesures choisies à la main sont insuffisantes
Traditionnellement, les chercheurs résument ce type de données de mouvement avec quelques statistiques familières — la distance parcourue (déplacement), la vitesse, et l’évolution de la direction au fil du temps (angles de virage). Les auteurs ont d’abord utilisé ces mesures manuelles dans une technique appelée calcul bayésien approximatif (ABC), qui recherche des jeux de paramètres faisant ressembler les trajectoires simulées aux trajectoires expérimentales. Ils ont constaté que, si ces résumés capturent des tendances générales, ils passent à côté d’une grande partie de la structure fine des données. En conséquence, certains paramètres du modèle, en particulier ceux gouvernant la persistance aléatoire et le timing des réorientations, restent mal contraints voire biaisés. De plus, l’ABC a exigé des centaines de milliers de simulations et de nombreuses heures de calcul pour atteindre des ajustements acceptables.
Laisser les réseaux neuronaux apprendre ce qui compte
Pour dépasser ces limites, l’étude s’est tournée vers une famille de méthodes plus récente appelée estimation postérieure neuronale (NPE). Ici, un réseau neuronal est entraîné directement sur de nombreuses paires de données simulées et de paramètres sous‑jacents. Une partie du réseau apprend automatiquement son propre ensemble compact de « caractéristiques résumées » à partir d’ensembles entiers de trajectoires cellulaires ; une autre partie apprend comment ces caractéristiques correspondent aux valeurs probables des paramètres. Crucialement, ces caractéristiques apprises sont optimisées explicitement pour une inférence précise des paramètres, et non pour l’interprétabilité humaine. Les auteurs ont ensuite réutilisé ces résumés appris dans un cadre ABC, créant une pipeline hybride qui combine la robustesse de l’ABC avec la flexibilité des réseaux neuronaux. 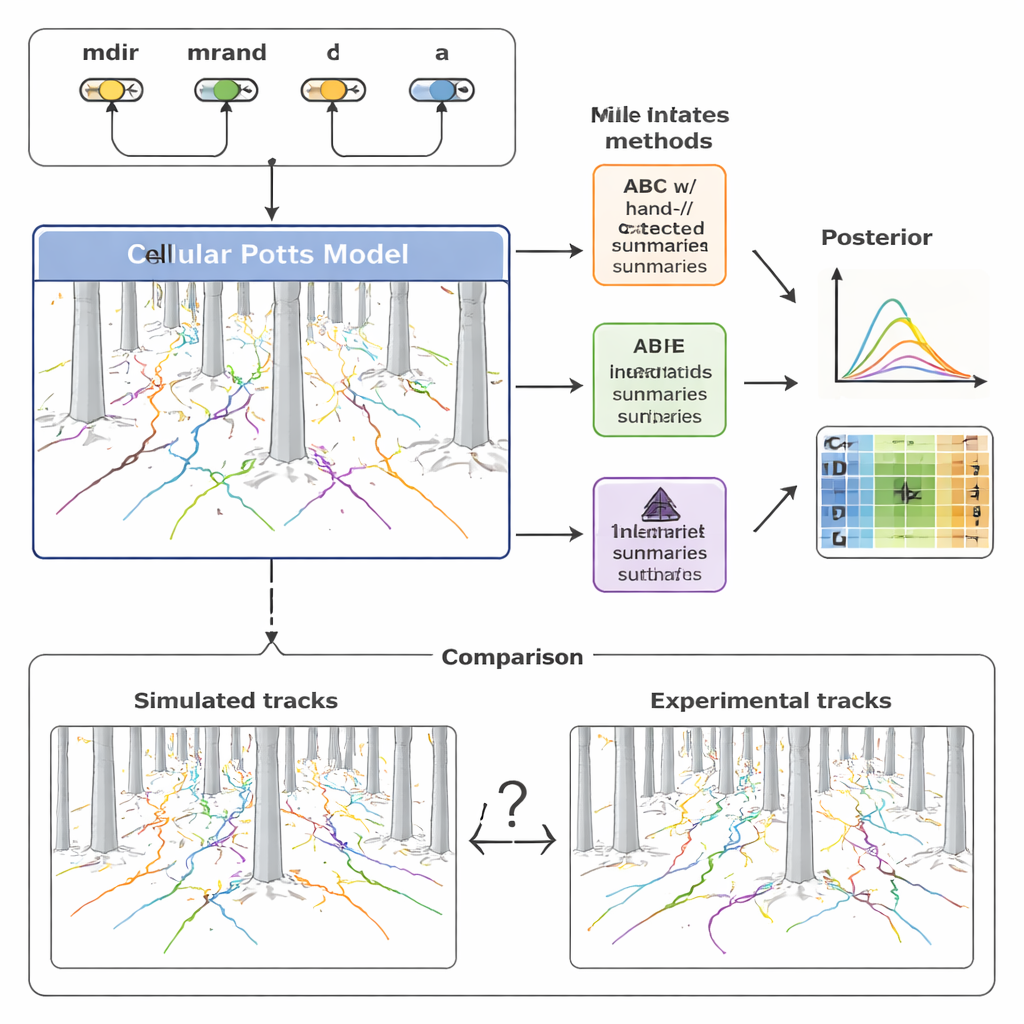
Ce que la nouvelle approche révèle sur la navigation cellulaire
Avec ce modèle calibré, les chercheurs ont exploré comment les signaux de chimiokine et les obstacles physiques façonnent conjointement la migration. La taille cellulaire inférée suggère que les cellules dendritiques se contractent et se déforment effectivement pour passer dans les interstices de 10 micromètres, cohérent avec leur flexibilité connue. Les simulations indiquent que le mouvement aléatoire persistant est un moteur majeur de l’étendue de dispersion des cellules, même en l’absence d’orientation chimique, et que la forêt de piliers peut piéger des cellules lorsque des indices directionnels forts et la persistance agissent ensemble. De manière surprenante, le modèle prédit qu’un signal de chimiokine brièvement actif tôt peut, dans certains cas, aider davantage de cellules à atteindre la cible qu’un signal constant, parce qu’une attraction prolongée peut maintenir les cellules à tournoyer à l’intérieur des obstacles plutôt que de leur permettre d’en sortir.
Pourquoi cela compte pour la biologie et la modélisation
Pour les non‑spécialistes, le message principal est double. D’une part, la migration des cellules immunitaires dans les tissus ne se réduit pas à suivre une traînée chimique ; elle émerge d’une interaction subtile entre les indices de guidage, les tendances intrinsèques de mouvement des cellules et la configuration physique de leur environnement. D’autre part, extraire ces règles à partir d’images exige de laisser l’ordinateur apprendre quelles patrons dans les données sont les plus informatifs, plutôt que de se reposer uniquement sur des mesures simples conçues par des humains. En intégrant des expériences micro‑ingénierées, des simulations résolvant la forme et une inférence basée sur des réseaux neuronaux, ce travail fournit un modèle puissant pour étudier comment des types cellulaires variés se déplacent dans des environnements complexes, avec des applications potentielles allant de la compréhension de la surveillance immunitaire à la conception de meilleures thérapies contre le cancer.
Citation: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
Mots-clés: migration cellulaire, cellules dendritiques, gradients de chimiokines, inférence basée sur la simulation, forêts de piliers microfluidiques