Clear Sky Science · fr
Contrôle de la croissance des gliomes optiques médié par l’asthme via les interactions lymphocytes T–microglie : un modèle mathématique
Quand des troubles respiratoires se relient aux tumeurs cérébrales
L’asthme et les tumeurs cérébrales semblent appartenir à des mondes différents : l’un affecte notre respiration, l’autre notre vision, la pensée et le mouvement. Pour autant, les cliniciens ont observé un schéma troublant — les enfants asthmatiques semblent moins susceptibles de développer certains types de tumeurs du nerf optique. Cet article explore comment une maladie pulmonaire chronique pourrait, de manière inattendue, protéger le cerveau, en utilisant un modèle mathématique pour retracer les conversations chimiques cachées entre cellules immunitaires et cellules tumorales.
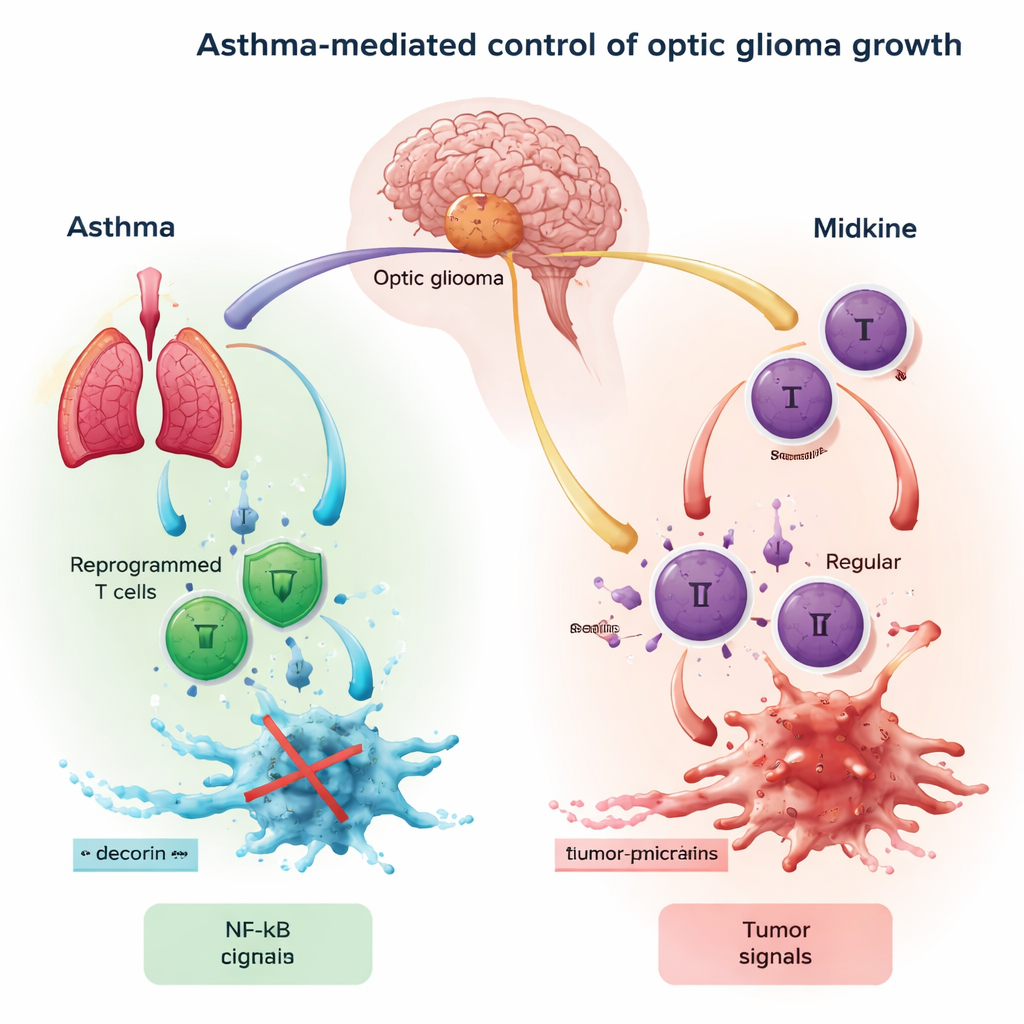
Une tumeur à croissance lente mais aux enjeux élevés
Les gliomes optiques sont généralement des tumeurs à croissance lente qui se forment le long du nerf optique, le plus souvent chez des enfants porteurs d’une affection génétique appelée neurofibromatose de type 1 (NF1). Même si ces tumeurs sont considérées comme « de bas grade », elles peuvent néanmoins provoquer une perte de vision et des troubles hormonaux. Dans la NF1, une mutation désactive une régulation et conduit à l’hyperactivité d’une protéine de signalisation appelée RAS. Cette hyperactivité stimule la production d’une autre molécule, la midkine, qui agit comme un haut-parleur dans le nerf optique, attirant des cellules immunitaires et remodelant le microenvironnement de façons qui favorisent généralement la tumeur plutôt que de la combattre.
Une conversation nourrissant la tumeur entre nerf et cellules immunitaires
Les auteurs se concentrent sur une chaîne d’événements reliant le nerf optique, les cellules immunitaires et la croissance tumorale. La midkine provenant du nerf optique active d’abord les lymphocytes T, un type de globules blancs, les incitant à libérer un signal appelé CCL4. Ce signal se lie ensuite à des récepteurs (CCR5 et CCR8) sur les microglies, les cellules immunitaires résidentes du cerveau. Lorsque suffisamment de CCL4 s’accroche à ces récepteurs, cela active un commutateur maître à l’intérieur des microglies connu sous le nom de NF-κB. Une fois activé, NF-κB stimule la production d’un autre signal, CCL5, qui encourage les cellules du gliome optique à croître, migrer et échapper à l’attaque immunitaire. En pratique, l’axe midkine–CCL4–NF-κB–CCL5 forme un signal circulaire « go » pour l’expansion tumorale.
Comment l’asthme reprogramme les lymphocytes T en freins tumoraux
L’asthme est surtout connu comme une maladie d’inflammation chronique des voies aériennes. Mais chez les personnes asthmatiques, certains lymphocytes T sont « reprogrammés » dans un état différent : ils perdent une grande partie de leur pouvoir cytotoxique direct et sécrètent à la place des molécules qui remodelent leur environnement. L’une de ces molécules est la décorine, une petite protéine dotée de propriétés anti-tumorales reconnues. L’idée centrale de ce travail est que des lymphocytes T primés par l’asthme peuvent migrer du poumon vers le cerveau et libérer de la décorine dans le voisinage du gliome optique. La décorine entre en compétition avec CCL4 pour le récepteur CCR8 sur les microglies, bloquant ainsi en partie la conversation qui nourrit la tumeur et réduisant l’activité de NF-κB et la production de CCL5 au sein des cellules immunitaires cérébrales.
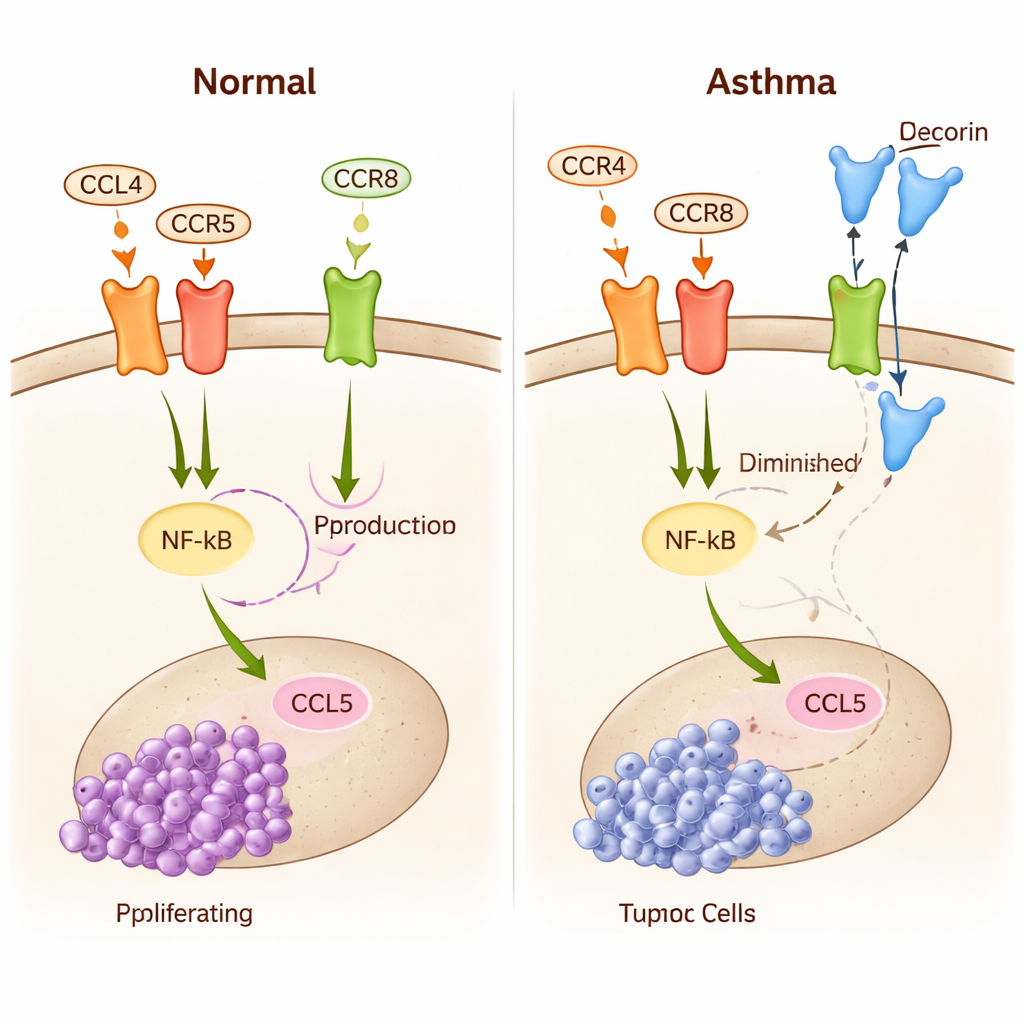
Utiliser les mathématiques pour suivre un réseau invisible
Parce que ce réseau de signalisation est trop complexe pour être saisi uniquement par l’intuition, les chercheurs ont construit un modèle mathématique détaillé reposant sur des équations différentielles. Le modèle suit les niveaux des molécules clés (midkine, CCL4, décorine, NF-κB, CCL5), l’activité des récepteurs sur les microglies et la croissance des cellules tumorales au fil du temps. Ils ont utilisé des données expérimentales pour calibrer l’intensité de chaque interaction, puis simulé de nombreux scénarios. Le modèle montre comment de petits changements dans l’affinité de liaison — la facilité avec laquelle CCL4 ou la décorine se fixent à leurs récepteurs — peuvent basculer les microglies entre deux modes : un état pro-tumoral avec NF-κB et CCL5 élevés, et un état anti-tumoral avec une forte liaison de la décorine et des signaux CCL4 faibles. Un indice simple fondé sur le rapport entre récepteurs liés à la décorine et récepteurs liés à CCL4 prédit avec précision si la tumeur a tendance à croître ou à stagner.
Concevoir des traitements immunitaires plus intelligents
Au-delà d’expliquer pourquoi l’asthme pourrait protéger contre le gliome optique, le modèle est utilisé pour explorer des stratégies thérapeutiques. Il suggère que des traitements augmentant les niveaux de décorine ou affaiblissant l’emprise de CCL4 sur ses récepteurs pourraient ralentir la croissance tumorale. Les auteurs testent numériquement des approches comme des perfusions répétées de lymphocytes T producteurs de décorine ou l’utilisation du messager immunitaire IL-2 pour étendre ces cellules bénéfiques dans l’organisme. Fait intéressant, les simulations révèlent que non seulement la dose totale, mais aussi le calendrier des traitements importe : des administrations modérées et bien espacées peuvent maintenir les microglies dans l’état anti-tumoral aussi efficacement que des doses plus élevées et moins fréquentes, avec potentiellement moins d’effets indésirables.
Ce que cela signifie pour les patients et les familles
Pour les non-spécialistes, le message central est que l’inflammation chronique de l’asthme, habituellement perçue comme nuisible, peut parfois reconfigurer le système immunitaire de façons qui freinent certaines tumeurs cérébrales. En transformant les lymphocytes T en « usines » de décorine, l’asthme semble déplacer l’équilibre dans le nerf optique d’un environnement favorable à la croissance vers un environnement plus hostile au cancer. Il ne s’agit nullement de proposer l’asthme comme thérapie, mais les mécanismes mis en lumière ici pourraient inspirer de nouveaux traitements qui reproduisent ses aspects protecteurs — en recourant à des thérapies par lymphocytes T sur mesure ou à des médicaments mimant l’action bloquante de la décorine — pour protéger les enfants à risque de gliome optique.
Citation: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Mots-clés: gliome optique, asthme, décorine, lymphocytes T, modélisation mathématique