Clear Sky Science · fr
Polysaccharides et barrière de mucus du côlon : revue des interactions biophysiques et impacts fonctionnels
Pourquoi la muqueuse glissante de l’intestin compte
Au cœur de votre gros intestin se trouve un bouclier visqueux et invisible : une couche de mucus qui maintient des trillions de microbes à distance de vos propres cellules. Cet article de synthèse examine comment des sucres complexes appelés polysaccharides — provenant des aliments, des algues, des champignons et de produits médicaux — interagissent avec cette barrière muqueuse. Comprendre ce dialogue entre l’alimentation et le mucus aide à expliquer pourquoi certaines fibres sont bénéfiques pour la santé intestinale, comment certains traitements peuvent protéger contre la colite et d’autres maladies intestinales, et comment des systèmes de délivrance de médicaments plus intelligents pourraient un jour déposer des médicaments précisément là où ils sont le plus nécessaires.
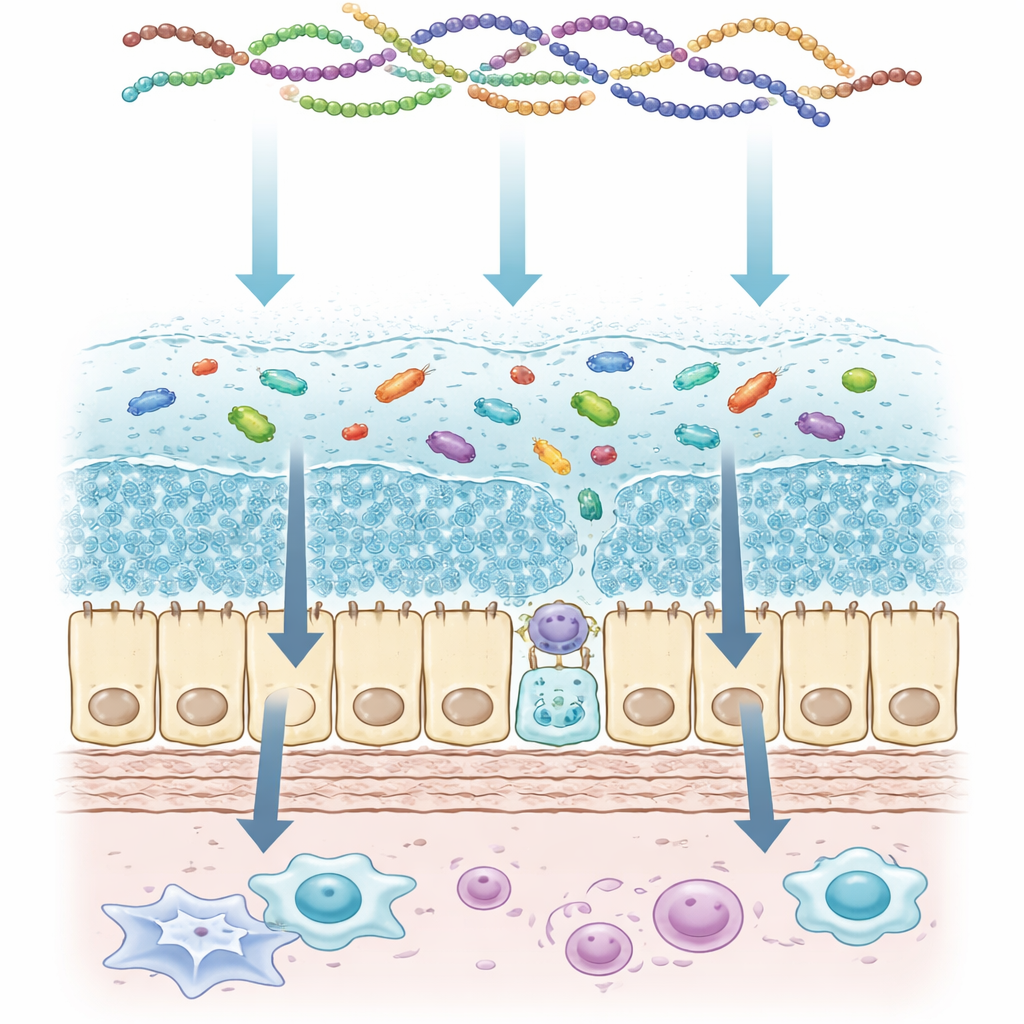
La couverture de sécurité à deux couches du côlon
Les auteurs commencent par décrire l’architecture du mucus colique comme une structure à deux étages. Au plus près de la paroi intestinale se trouve une couche interne dense presque exempte de bactéries et qui agit comme un bouclier serré. Au‑dessus s’étend une couche externe plus lâche qui sert d’habitat contrôlé pour les microbes bienveillants. Des cellules spécialisées appelées cellules caliciformes produisent et libèrent en continu de grandes molécules de mucus, qui se déroulent rapidement et gélifient lorsqu’elles atteignent la surface intestinale. Ces molécules formatrices de gel sont largement décorées de branches sucrées, qui donnent au mucus son épaisseur, sa capacité de rétention d’eau et sa charge négative. Lorsque cette structure se dégrade — par inflammation, infection ou défauts génétiques — les bactéries se rapprochent de la paroi, des signaux immunitaires se déclenchent et des troubles intestinaux chroniques peuvent apparaître.
Des sucres différents, des modes d’adhérence différents
Les polysaccharides sont des longues chaînes de sucres simples, mais leur comportement dans le mucus dépend de détails tels que la taille, le degré de ramification et la charge électrique. Les chaînes neutres comme les amidons résistants et l’inuline s’intègrent principalement dans la matrice muqueuse par liaisons hydrogène et enchevêtrement physique. Les chaînes chargées négativement, issues des pectines, alginates et gommes d’algues, peuvent s’associer faiblement ou se repousser avec le mucus déjà négatif, selon les ions locaux et le motif fin de charges sur les deux partenaires. Les chaînes chargées positivement, en particulier la chitine/chitosane provenant de crustacés et de champignons, sont fortement attirées par le mucus et peuvent former des complexes étroits avec lui. La revue explique que ces interactions ne sont pas gouvernées par une seule force mais par un mélange d’attraction électrostatique, de liaisons hydrogène, de contacts hydrophobes et de forces de van der Waals subtiles qui déterminent ensemble la profondeur de pénétration d’un polysaccharide dans le gel et la fermeté de son adhérence.
Murs intestinaux modèles sur puces, boîtes et tranches
Pour démêler ces interactions complexes, les chercheurs s’appuient sur une boîte à outils de modèles expérimentaux. Les cultures cellulaires planes peuvent être enrichies en cellules sécrétrices de mucus pour examiner comment des polysaccharides spécifiques modifient la production de mucus, son épaisseur ou sa perméabilité. Des organoïdes tridimensionnels issus de cellules souches construisent des tubes intestinaux miniatures qui sécrètent leur propre mucus, tandis que des plateformes microfluidiques « gut‑on‑a‑chip » ajoutent un écoulement réaliste, des étirements et des bactéries vivantes. Les dispositifs ex vivo maintiennent des tissus intestinaux fraîchement isolés en vie pendant de courtes périodes, préservant les couches naturelles de mucus et les cellules immunitaires. Chaque modèle présente des compromis : les boîtes simples sont faciles mais artificielles, les puces et organoïdes sont plus réalistes mais techniquement exigeants. En comparant les résultats obtenus avec ces systèmes, les scientifiques peuvent distinguer les effets physiques directs des polysaccharides sur le mucus des effets indirects médiés par les microbes et le système immunitaire.
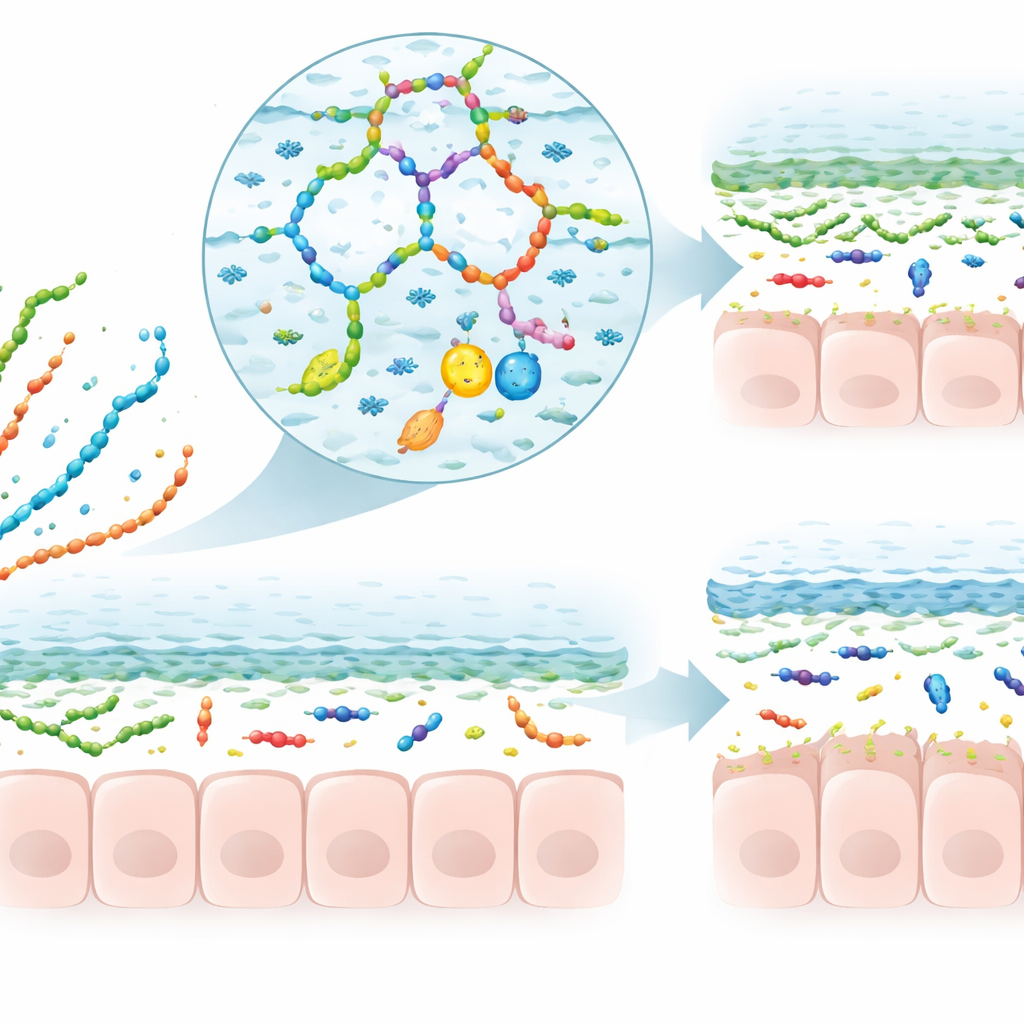
Façonner le mucus, les microbes et la réponse immunitaire
La revue examine ensuite les conséquences fonctionnelles lorsque les polysaccharides rencontrent le mucus. Certaines chaînes chargées positivement peuvent temporairement assouplir ou réorganiser le gel, influençant la facilité de déplacement des particules et des médicaments à travers lui. D’autres forment des réseaux mixtes avec le mucus qui épaississent ou stabilisent la couche. De nombreux polysaccharides alimentaires ne sont pas digérés par l’hôte mais fermentés par les bactéries intestinales, qui les transforment en acides gras à chaîne courte et autres petites molécules. Ces produits de fermentation signalent aux cellules caliciformes d’augmenter la production de mucus, modulent les décorations sucrées du mucus et soutiennent une communauté microbienne qui tend à se maintenir dans la couche externe. Dans des modèles animaux de colite, certains polysaccharides végétaux et fongiques augmentent le nombre de cellules caliciformes, restaurent l’épaisseur du mucus et maintiennent les bactéries plus éloignées de la paroi intestinale, souvent en parallèle d’une inflammation et d’un stress oxydatif réduits.
Concevoir aliments et thérapies qui collaborent avec le mucus
En conclusion, les auteurs soutiennent que les polysaccharides peuvent être délibérément conçus ou sélectionnés pour soutenir la barrière muqueuse plutôt que de l’endommager involontairement. En reliant des traits structuraux spécifiques — tels que la charge et le poids moléculaire — à des résultats mesurables comme l’épaisseur du mucus, la viscosité et la pénétrabilité, ils proposent des lignes directrices pour choisir des polysaccharides qui renforcent la barrière, transportent les médicaments plus efficacement vers le côlon ou orientent en douceur le microbiote vers des activités favorables à la santé. Pour les non‑spécialistes, le message central est que le film visqueux qui tapisse le côlon n’est pas un simple dépôt passif ; c’est une interface active où la chimie de notre alimentation, nos microbes résidents et nos défenses immunitaires se rencontrent. Des polysaccharides conçus avec soin pourraient devenir des outils clés pour préserver cette interface et maintenir l’équilibre de nos intestins.
Citation: Cheong, KL., Biney, E., Wang, M. et al. Polysaccharides and the colon mucus barrier: a review of biophysical interactions and functional impacts. npj Sci Food 10, 98 (2026). https://doi.org/10.1038/s41538-026-00750-6
Mots-clés: barrière de mucus du côlon, polysaccharides alimentaires, microbiote intestinal, libération de médicaments mucoadhésive, maladie inflammatoire de l’intestin