Clear Sky Science · fr
Le lycopène atténue la ferroptose hépatique induite par la toxine T-2 en ciblant l’axe Nrf2/mitophagie chez la souris
Pourquoi une toxine fongique présente dans les céréales courantes compte
De nombreux aliments de base, notamment le blé et le maïs, peuvent être contaminés par une toxine produite par des moisissures appelée toxine T-2. Ce contaminant invisible résiste à la cuisson et au traitement, et une exposition prolongée peut endommager silencieusement des organes vitaux, en particulier le foie. L’étude résumée ici pose deux questions urgentes : comment la toxine T-2 nuit-elle précisément au foie, et un composé alimentaire naturel — le lycopène, le pigment rouge des tomates et d’autres fruits — peut‑il aider à protéger contre ces dommages ?
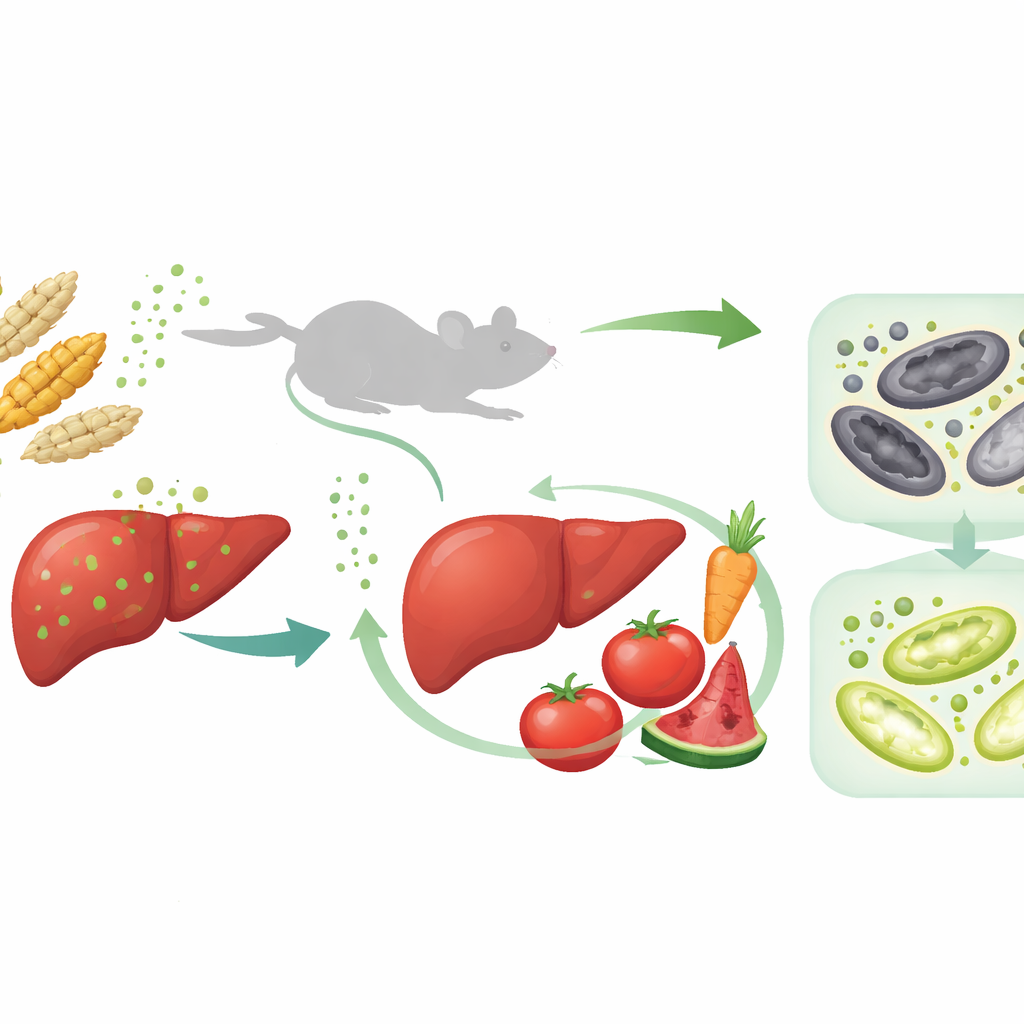
Comment la toxine endommage le foie
Les chercheurs ont d’abord administré à des souris des doses graduées de toxine T-2 pendant quatre semaines pour reproduire une exposition alimentaire continue. À mesure que les niveaux de toxine augmentaient, les animaux prenaient moins de poids, leurs foies devenaient hypertrophiés et d’un jaune pâle, et les analyses sanguines montraient une hausse des enzymes hépatiques indicatrices de lésions. Au microscope, le tissu hépatique apparaissait gonflé et désorganisé, avec des vacuoles intracellulaires et des signes de mort cellulaire. Une analyse protéomique à grande échelle des échantillons de foie a révélé que de nombreuses voies les plus altérées concernaient le métabolisme du fer, le métabolisme lipidique et une forme spécifique de mort cellulaire appelée ferroptose, entraînée par le fer et l’oxydation incontrôlée des lipides.
Surcharge en fer et une mort cellulaire semblable à la rouille
En approfondissant, l’équipe a mesuré des marqueurs classiques de la ferroptose. Dans les foies exposés à la toxine, la teneur en fer augmentait, tandis que les molécules indiquant des dommages lipidiques augmentaient et que l’activité d’une enzyme protectrice clé, GPx‑4, diminuait. Les protéines qui stockent normalement le fer en toute sécurité à l’intérieur des cellules augmentaient, mais le principal « exporteur » de fer des cellules hépatiques diminuait, suggérant que le fer restait piégé à l’intérieur. Lorsque les scientifiques ont administré à certaines souris un médicament qui bloque spécifiquement la ferroptose, la structure et la fonction hépatique se sont améliorées : l’œdème a diminué, les scores de lésion ont baissé et les signes chimiques de dommage oxydatif se sont atténués. Cela a clairement relié la toxicité hépatique de la toxine T‑2 à une forme de mort cellulaire, entraînée par le fer, semblable à la rouille.
Mitrochondries, nettoyage cellulaire et un interrupteur de défense
L’équipe s’est ensuite intéressée aux mitochondries, les centrales énergétiques des cellules, qui sont à la fois source et cible du stress oxydatif. Chez les souris traitées par la toxine, la production d’énergie mitochondriale a diminué tandis que la libération de cytochrome c et le niveau global d’espèces réactives de l’oxygène ont augmenté, et la microscopie électronique montrait des mitochondries réduites et structurellement endommagées. Parallèlement, le système de contrôle qualité cellulaire — la mitophagie, un processus sélectif de « nettoyage » qui élimine les mitochondries défectueuses — a été activé via une voie impliquant les protéines PINK1 et Parkin. Lorsque les chercheurs ont utilisé des souris dépourvues de Parkin, incapables donc de lancer la mitophagie normale, la toxine T‑2 a provoqué une accumulation de fer encore plus importante, des signaux de ferroptose plus forts et des dommages hépatiques plus sévères. Cela montre que la mitophagie joue un rôle protecteur, limitant les lésions induites par la toxine.
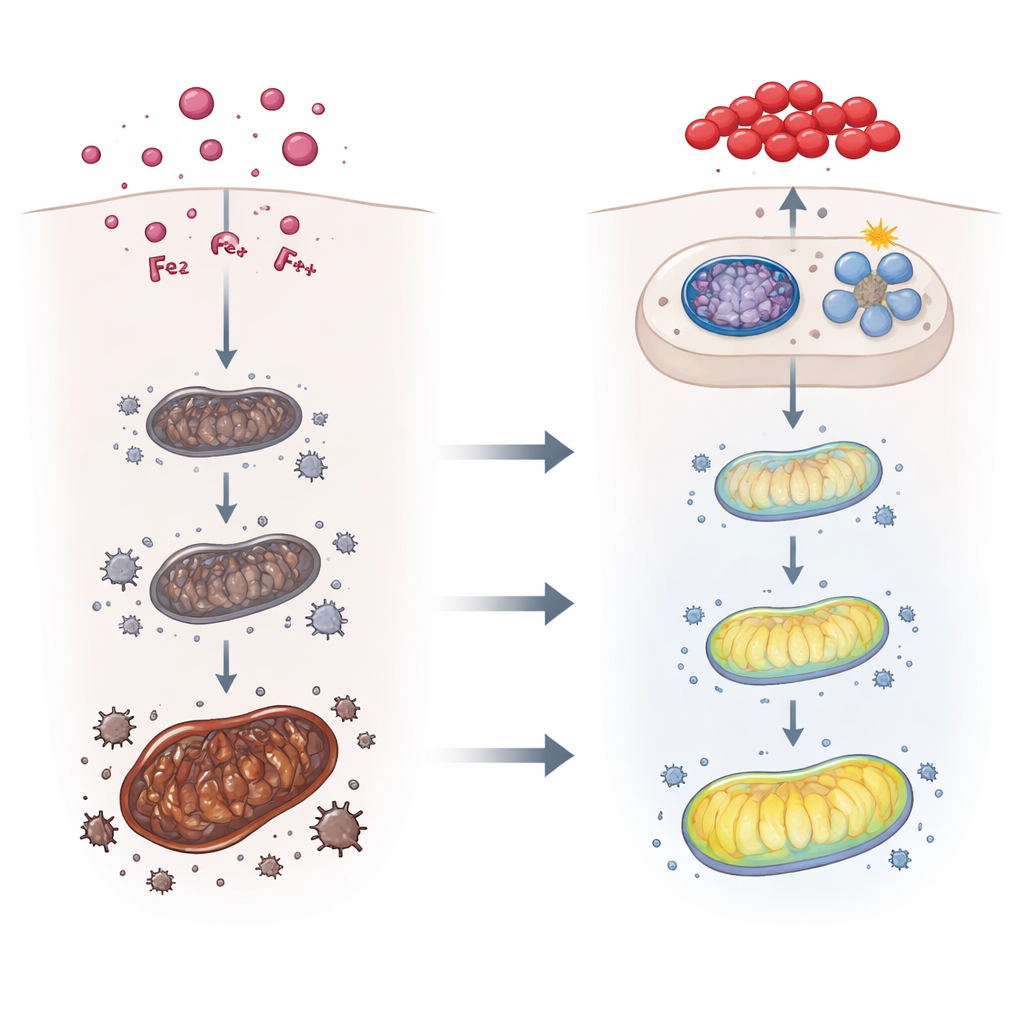
Une voie de protection intégrée et le rôle du lycopène
Comme l’équilibre du fer, le stress oxydatif et la mitophagie semblaient liés, les auteurs ont cherché un régulateur en amont et se sont focalisés sur Nrf2, un interrupteur maître qui active les gènes antioxydants et de détoxification. La toxine T‑2 activait partiellement Nrf2, mais lorsque des souris ont reçu un composé connu pour activer Nrf2, l’export du fer hépatique s’est amélioré, les marqueurs de ferroptose ont diminué et la mitophagie a augmenté, ce qui a atténué l’impact de la toxine. L’équipe s’est ensuite demandé si le lycopène pouvait agir comme un booster naturel de Nrf2. La modélisation informatique a suggéré que le lycopène peut se lier physiquement à la fois à Nrf2 et à sa protéine répresseur Keap1 de manière à favoriser l’activation de Nrf2. Chez les souris vivantes, un traitement au lycopène avant et pendant l’exposition à la toxine a amélioré le poids corporel, restauré l’aspect du foie et les analyses sanguines, réduit l’accumulation de fer et les dommages oxydatifs, et activé davantage Nrf2 ainsi que la voie de mitophagie PINK1–Parkin.
Ce que cela signifie pour la sécurité alimentaire et l’alimentation
En termes simples, l’étude montre que la toxine T‑2 blesse le foie en piégeant un excès de fer à l’intérieur des cellules, en endommageant les mitochondries et en déclenchant la ferroptose. L’organisme réagit en activant Nrf2 et la mitophagie pour éliminer les mitochondries endommagées et rééquilibrer le fer, mais cette défense peut être dépassée. Le lycopène semble renforcer ce bouclier interne, aidant le foie à exporter le fer, à nettoyer les mitochondries défectueuses et à résister à la mort cellulaire ferroptotique. Bien que des travaux supplémentaires soient nécessaires avant de traduire ces résultats chez l’humain, la recherche suggère que certains composés végétaux, comme le lycopène, pourraient un jour faire partie de stratégies visant à réduire l’impact sanitaire des toxines d’origine alimentaire inévitables.
Citation: Yang, X., Song, W., Lu, Z. et al. Lycopene mitigates T-2 toxin-induced hepatic ferroptosis by targeting the Nrf2/mitophagy axis in mice. npj Sci Food 10, 94 (2026). https://doi.org/10.1038/s41538-026-00736-4
Mots-clés: toxine T-2, lycopène, lésion hépatique, ferroptose, mitophagie