Clear Sky Science · fr
Divergence structurale des polysaccharides de Lentinula edodes associée à des voies anti‑hyperuricémie distinctes
Les shiitakes et un problème de santé en expansion
Un taux élevé d’acide urique dans le sang, appelé hyperuricémie, devient de plus en plus fréquent dans le monde et est surtout connu pour provoquer la goutte douloureuse. Il est aussi associé à des lésions rénales, des troubles hépatiques et une inflammation chronique. De nombreux médicaments actuels abaissent efficacement l’acide urique mais peuvent entraîner des effets indésirables sérieux, d’où un fort intérêt pour des options alimentaires plus sûres. Cette étude examine si des sucres naturels (polysaccharides) extraits du shiitake (Lentinula edodes) peuvent aider à contrôler l’acide urique et protéger les organes — et comment de subtiles différences dans leur structure moléculaire modifient leurs modes d’action.
Deux proches parents du champignon : similaires, mais différents
Les chercheurs ont isolé deux polysaccharides principaux du shiitake, nommés LEP20 et LEP50, en utilisant une séparation par éthanol de polarité graduée pour les trier selon leur taille et leur conformation. Des analyses chimiques détaillées, comprenant chromatographie et résonance magnétique nucléaire, ont montré que les deux sont des chaînes de glucose, mais avec des architectures très différentes. LEP20 est un β‑D‑glucane (1→3) avec des ramifications fréquentes, formant une structure plus rigide et hélicoïdale souvent observée dans les fibres fongiques actives sur le système immunitaire. LEP50 est un α‑D‑glucane (1→4) avec moins de ramifications, plus proche des amidons que nous digérons plus facilement. Ces contrastes structuraux — orientation des liaisons, schéma de ramification et masse moléculaire — prédisposent les deux composés à agir par des voies biologiques distinctes, bien qu’ils proviennent du même champignon.
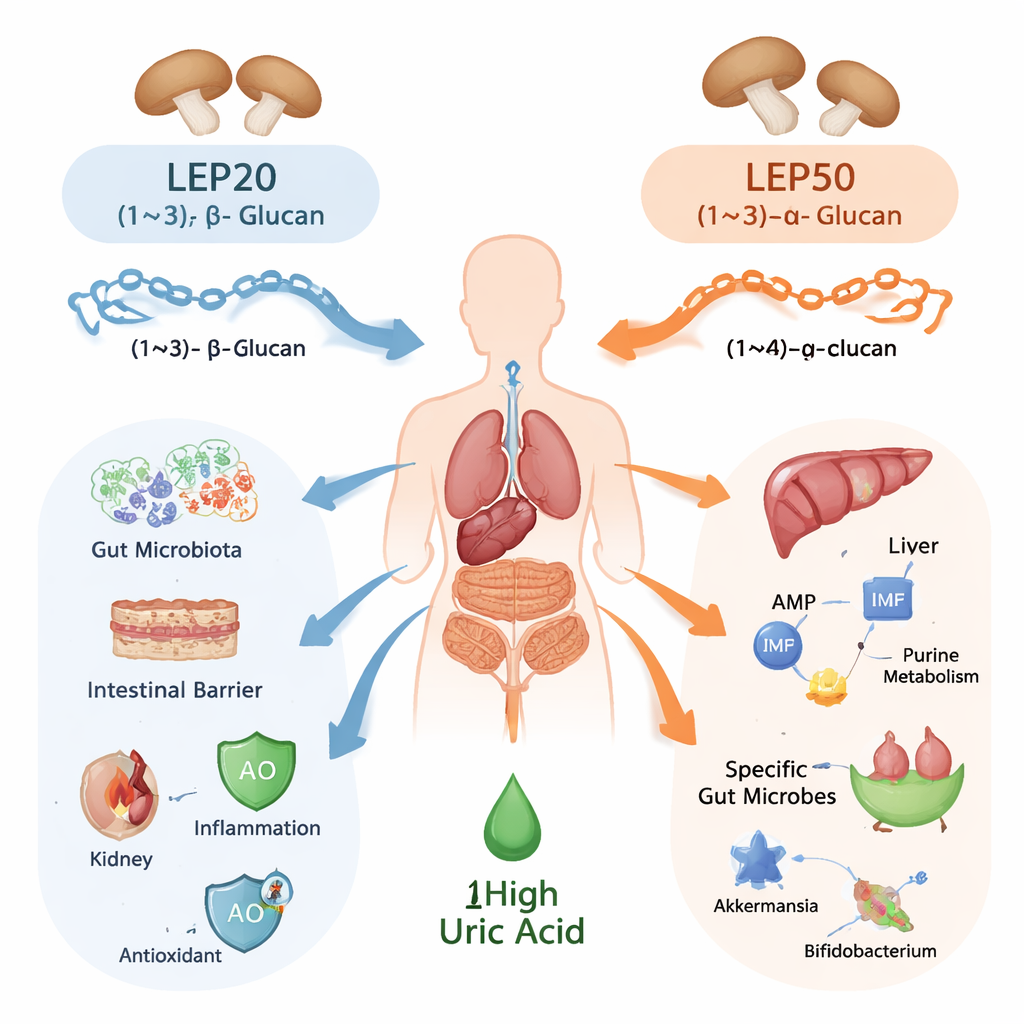
Protection des reins, du foie et de l’intestin
Pour tester leurs effets, l’équipe a utilisé des rats traités avec des produits chimiques reproduisant l’hyperuricémie humaine. LEP20 et LEP50 ont tous deux considérablement réduit le taux d’acide urique sanguin et diminué l’activité de la xanthine oxydase, l’enzyme hépatique qui convertit les purines en acide urique. Ils ont aussi amélioré les marqueurs classiques de la fonction rénale (créatinine et urée) et des dommages hépatiques (ASAT et ALAT), et l’examen tissulaire a montré moins de fibrose, d’œdème et d’infiltration inflammatoire dans ces organes. Dans les reins, les deux polysaccharides ont orienté favorablement la gestion de l’acide urique : ils ont réduit l’expression des transporteurs qui réabsorbent l’acide urique vers le sang et augmenté ceux qui le sécrètent pour l’élimination. LEP20 s’est avéré systématiquement plus puissant que LEP50 pour réduire l’inflammation, renforcer les défenses antioxydantes et restaurer l’architecture microscopique des tissus rénaux et hépatiques.
L’intestin comme centre de contrôle
Étant donné que l’intestin et son microbiote influencent fortement l’acide urique et l’inflammation, les chercheurs ont examiné l’intestin en détail. Les rats hyperuricémiques présentaient une muqueuse abîmée, une diminution des protéines de jonction serrée qui scellent normalement la barrière et des niveaux accrus de molécules inflammatoires. Le traitement par l’un ou l’autre polysaccharide a partiellement inversé ces altérations, LEP20 offrant à nouveau une meilleure protection. Grâce au séquençage de l’ADN, l’équipe a montré que les deux composés remodelaient le microbiote intestinal, mais de façon différente. LEP20 favorisait la croissance de bactéries bénéfiques productrices d’acides gras à chaîne courte comme Blautia et Lactobacillus, tout en supprimant des souches potentiellement nuisibles. Ce changement a accru les niveaux d’acides microbien clés — en particulier le butyrate — connus pour renforcer la barrière intestinale et réduire l’inflammation. LEP50 a aussi amélioré le microbiote, mais a davantage influencé des espèces et des fonctions liées au métabolisme des purines, la voie chimique qui génère l’acide urique à partir des sources alimentaires et endogènes.
Des routes différentes pour abaisser l’acide urique
Pour relier ces modifications microbiennes à la chimie corporelle, l’équipe a profilé des centaines de petites molécules dans les selles des rats. LEP20 a principalement modifié des voies liées aux lipides et au tryptophane et augmenté des métabolites associés à la protection antioxydante et aux effets anti‑inflammatoires. LEP50, en revanche, a eu un impact plus net sur le métabolisme des purines et des nucléotides. Notamment, il a diminué l’hypoxanthine, un précurseur direct que la xanthine oxydase convertit en acide urique, et augmenté certains composés liés aux acides biliaires qui pourraient favoriser l’élimination de l’acide urique. En corrélant microbes, métabolites et marqueurs de santé, les scientifiques ont observé que les bactéries « bénéfiques » et leurs produits s’associaient à un acide urique plus bas, de meilleurs tests rénaux et hépatiques et des profils de transporteurs d’acide urique plus favorables, tandis que les bactéries « nocives » et les produits de dégradation des purines s’associaient à des résultats plus défavorables.
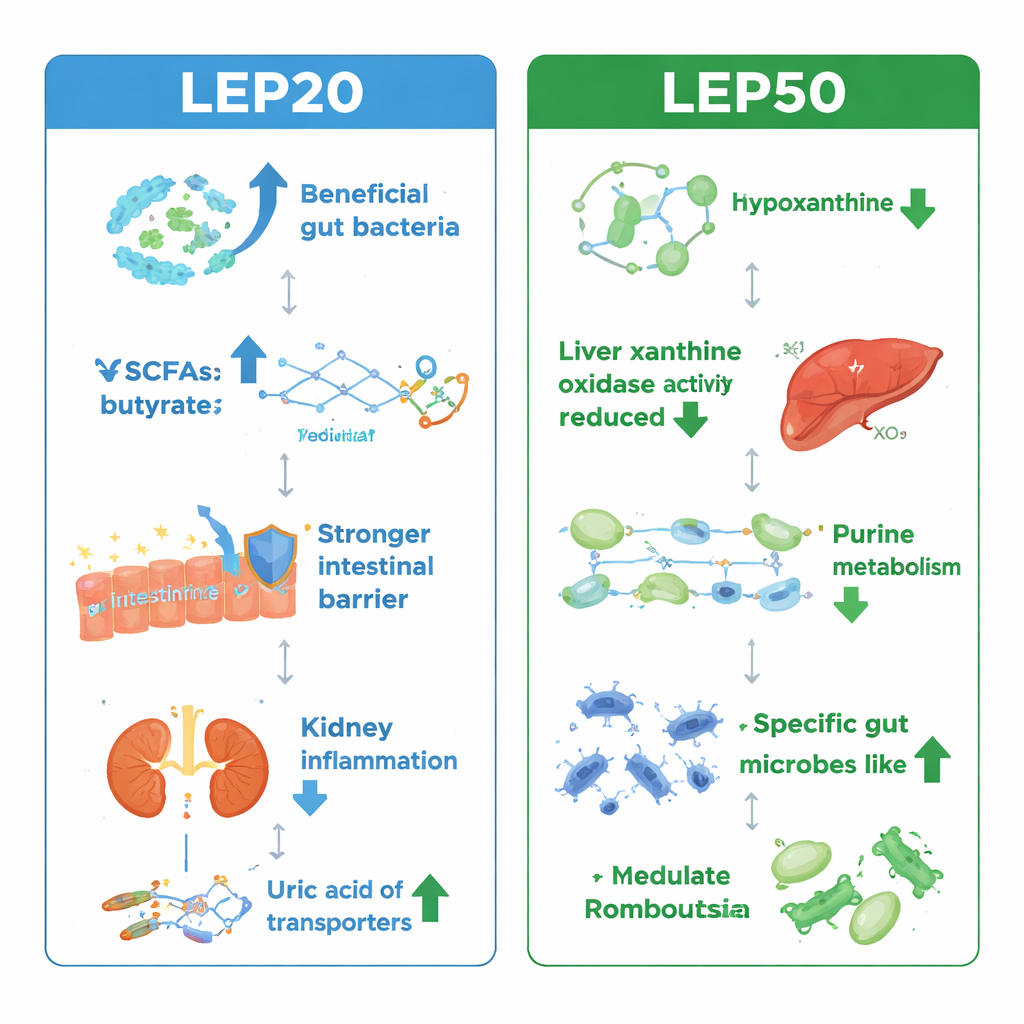
Ce que cela signifie pour les personnes à acide urique élevé
Globalement, l’étude montre que deux fibres proches issues du shiitake peuvent à la fois atténuer l’hyperuricémie et protéger les reins, le foie et l’intestin — mais qu’elles le font par des voies principales différentes. Le type β‑glucane LEP20 tend à renforcer la barrière intestinale, calmer l’inflammation et augmenter la capacité antioxydante via des microbes bénéfiques et leurs acides gras à chaîne courte. Le type α‑glucane LEP50 influence plus directement le métabolisme des purines et la production d’acide urique. Pour le grand public, la conclusion est que tous les « polysaccharides de champignon » ne sont pas interchangeables : leur structure à grande finesse compte et détermine leur interaction avec le microbiome et le métabolisme de l’hôte. Cette compréhension pourrait orienter la conception de futurs aliments fonctionnels ou compléments combinant des fibres fongiques spécifiques pour mieux gérer, de façon plus sûre et efficace, l’hyperuricémie et les affections associées.
Citation: Xiong, X., Liu, P., Liu, L. et al. Structural divergence of lentinula edodes polysaccharides is associated with distinct anti-hyperuricemia pathways. npj Sci Food 10, 64 (2026). https://doi.org/10.1038/s41538-026-00714-w
Mots-clés: hyperuricémie, champignon shiitake, polysaccharides, microbiote intestinal, acide urique