Clear Sky Science · fr
La métabolomique aidée par apprentissage automatique décrypte le remodelage adaptatif des biofilms de Bacillus en réponse au stress de la pasteurisation
Pourquoi les consommateurs de lait devraient s’en préoccuper
Le lait pasteurisé est conçu pour être sûr et se conserver plus longtemps, pourtant certaines bactéries résistantes peuvent survivre au traitement thermique et former discrètement des communautés visqueuses — appelées biofilms — à l’intérieur des équipements de transformation. Cette étude pose une question inquiétante aux conséquences très pratiques : la pasteurisation peut‑elle parfois aggraver ces biofilms, et si oui, quels changements chimiques internes aux bactéries en sont responsables ?
Microbes tenaces dans les laiteries modernes
Le lait est riche en nutriments et soutient une industrie florissante de produits laitiers réfrigérés et à basse température. Mais il abrite aussi Bacillus, un groupe de bactéries qui forment de robustes spores et adhèrent aux surfaces métalliques. Ces microbes forment des biofilms — couches protectrices de cellules et de substances collantes — qui résistent au nettoyage, ralentissent le transfert de chaleur et augmentent le risque de détérioration voire d’intoxination alimentaire. Les auteurs ont isolé 14 souches de Bacillus à partir de lait cru de fermes chinoises et ont testé leur capacité à former des biofilms avant et après une étape de pasteurisation simulée à 75 °C pendant 15 secondes. De façon surprenante, si de nombreuses souches formaient des biofilms plus faibles après chauffage, plusieurs sont devenues au contraire des constructrices plus fortes et plus adhérentes.
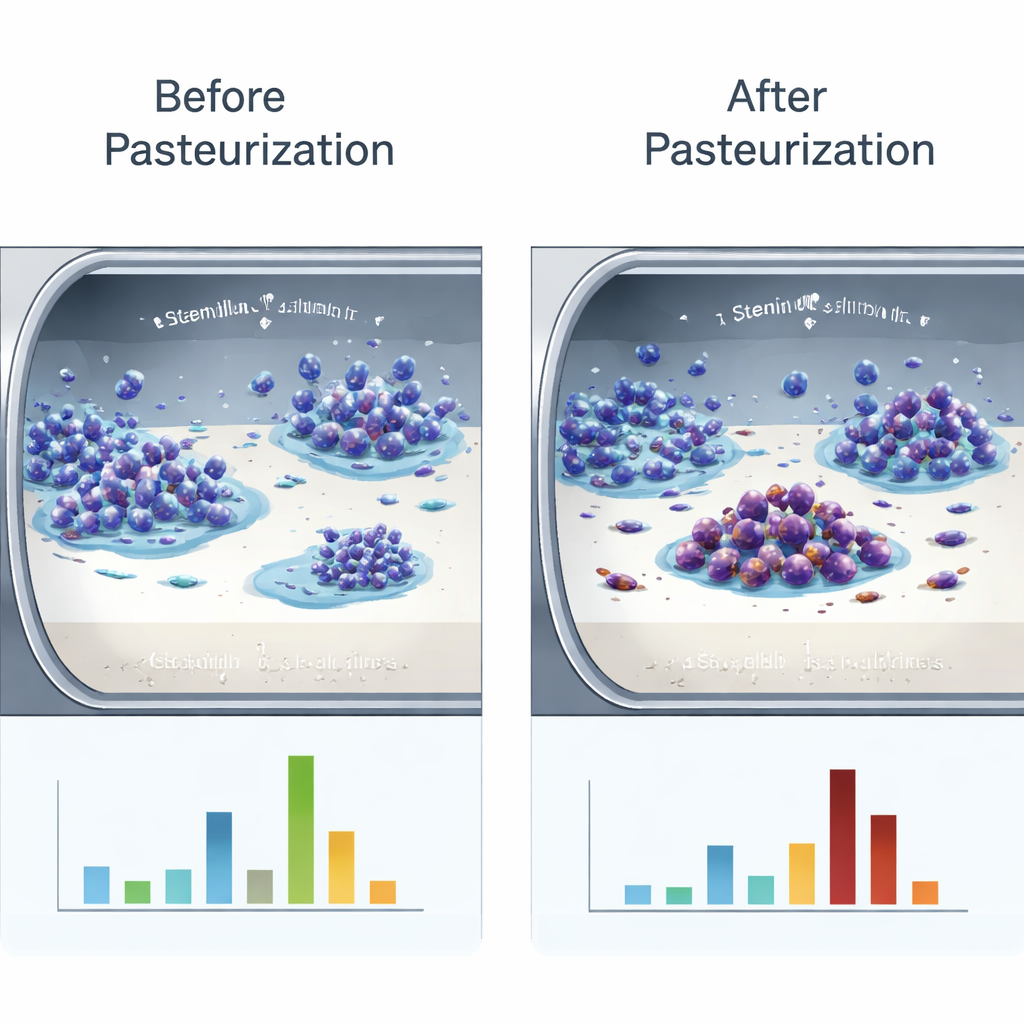
Un chauffage qui renforce certains biofilms et affaiblit d’autres
Pour reproduire les conditions des équipements laitiers, les chercheurs ont cultivé des souches sélectionnées sur des coupons en acier inoxydable 304 immergés dans du lait stérile. Ils ont ensuite coloré et mesuré l’ensemble des résidus — bactéries et dépôts de lait — laissés sur le métal. Deux souches, une de Bacillus cereus (BC01) et une de Bacillus subtilis (BS01), sont passées d’une adhésion faible à une adhésion forte après pasteurisation, tandis que des souches proches (BC02 et BS02) ont montré la tendance inverse. Les images au microscope électronique ont révélé comment l’architecture du biofilm changeait : chez les souches renforcées par la chaleur, le maillage fibrillaire habituel des substances polymériques extracellulaires s’est fusionné en agrégats épais et compacts qui emprisonnaient davantage de cellules et de protéines du lait, formant un enrobage plus résistant et étendu. Chez les souches affaiblies par la chaleur, la matrice est devenue clairesemée et fragmentée.
Quand l’adhérence superficielle défie les règles
La sagesse conventionnelle veut que plus une spore est hydrophobe (repoussant l’eau), mieux elle adhère et plus un biofilm se forme facilement. L’équipe a testé l’hydrophobicité des spores à l’aide d’un système huile‑eau et a trouvé l’opposé de ce que prédisent les manuels. Après pasteurisation, les souches qui ont gagné en vigueur de biofilm exhibaient en réalité une hydrophobicité de spore plus faible, tandis que celles qui perdaient leur capacité à former un biofilm devenaient plus hydrophobes. Même au sein des biofilms, les spores des formateurs robustes étaient moins hydrophobes que leurs homologues libres en suspension. Cette contradiction a pointé vers un moteur plus profond : des basculements induits par la chaleur dans le métabolisme et l’activité génique susceptibles d’emporter les simples propriétés physiques comme l’adhérence de surface.
Reprogrammation chimique sous stress thermique
En utilisant la métabolomique non ciblée — un large inventaire des petites molécules intracellulaires — combinée à une analyse par apprentissage automatique, les auteurs ont cartographié comment la chaleur remodelait la chimie du biofilm de chaque souche. Les quatre souches ont montré de grands changements touchant des centaines de métabolites, en particulier dans les systèmes de transport et les voies des acides aminés, mais les détails divergeaient nettement. Chez BC01, le chauffage semblait activer une enzyme appelée glutaminase, épuisant le pool de la nutriment du lait L‑glutamine et de l’acide aminé histidine. Ce basculement fournissait à la fois des éléments de construction pour la matrice du biofilm et levait des freins naturels à la formation de biofilm. Les niveaux de xanthosine, un composé qui incite normalement les bactéries à s’éloigner des biofilms, ont aussi diminué, favorisant probablement un mode de vie attaché et stable. Chez BS01, la chaleur a réduit l’arginine et plusieurs D‑acides aminés, la dopamine et l’acide arachidonique — molécules connues d’autres études pour déstabiliser les biofilms ou bloquer leur formation. Des quantités plus faibles de ces inhibiteurs, conjointement à un métabolisme énergétique modifié, ont aidé à faire pencher l’équilibre vers des biofilms plus robustes. En revanche, BC02 et BS02 ont souffert de pénuries de précurseurs polysaccharidiques clés et de composants du cycle énergétique, et chez BS02, des métabolites anti‑biofilm tels que la D‑tryptophane et la D‑arabinose ont augmenté, sapant collectivement la croissance des biofilms.
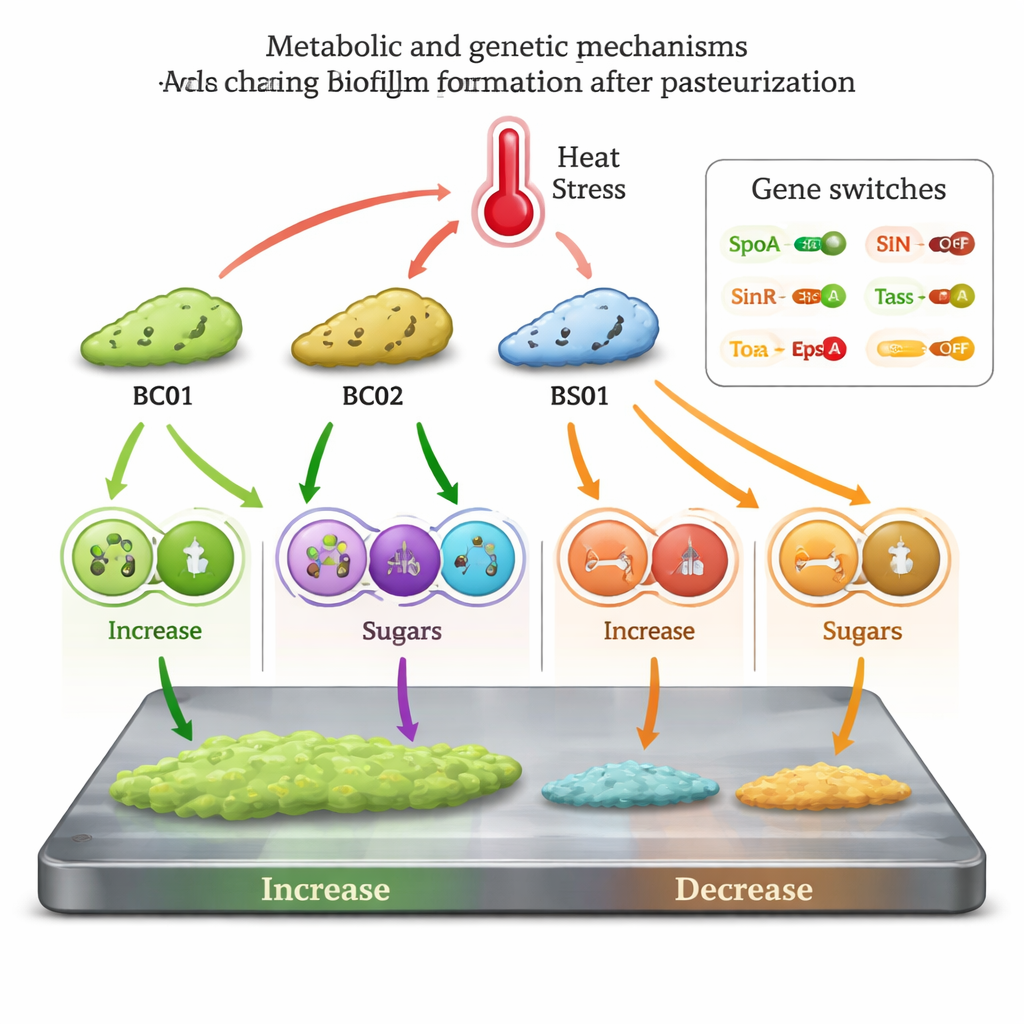
Gènes qui basculent l’interrupteur du biofilm
Pour relier la chimie au comportement, l’équipe a mesuré des gènes clés liés aux biofilms. Dans les souches renforcées par la chaleur BC01 et BS01, des régulateurs maîtres qui favorisent la formation de biofilm (Spo0A, TasA et EpsA) étaient surexprimés, tandis que SinR, un gène qui maintient normalement les gènes du biofilm sous contrôle, était réprimé. Le schéma inverse apparaissait dans BC02 et BS02. Ensemble, les données métaboliques et l’expression génique soutiennent un modèle selon lequel la pasteurisation agit comme un signal de stress que certaines lignées de Bacillus exploitent : elles reprogramment leur métabolisme, réduisent certains composés naturels anti‑biofilm et actionnent des commutateurs génétiques pour produire plus de matrice et des enrobages plus épais, même si leur activité globale ralentit.
Ce que cela signifie pour un lait plus sûr
Pour les consommateurs, le message n’est pas que le lait pasteurisé est dangereux, mais que les microbes survivant au traitement thermique peuvent être plus adaptables qu’on ne l’imagine. Plutôt que de se contenter de renforcer la ténacité des spores, la pasteurisation peut pousser certaines souches de Bacillus dans un mode de « repli » où elles construisent des biofilms plus solides à l’intérieur des tuyaux et des cuves. En identifiant des métabolites et des voies géniques spécifiques qui entraînent ce changement, l’étude suggère de nouvelles approches pour riposter : au lieu de compter uniquement sur des températures plus élevées ou des temps de chauffe plus longs, les transformateurs pourraient un jour ajouter des bloqueurs métaboliques bénins ou adapter les procédures de nettoyage pour perturber le système chimique qui soutient ces biofilms. En substance, comprendre comment la chaleur remodèle la chimie bactérienne ouvre la voie à des stratégies plus intelligentes pour maintenir les produits laitiers à la fois nutritifs et réellement propres.
Citation: Liang, L., Wang, P., Zhao, X. et al. Metabolomics aided by machine learning decodes adaptive remodeling of Bacillus biofilms in response to pasteurization stress. npj Sci Food 10, 62 (2026). https://doi.org/10.1038/s41538-026-00712-y
Mots-clés: lait pasteurisé, biofilms de Bacillus, sécurité alimentaire, transformation laitière, métabolisme bactérien