Clear Sky Science · fr
Thérapie cellulaire double dérivée du tissu adipeux favorise l’artériogenèse et la préservation du membre par intégration vasculaire dans l’ischémie critique des membres
Sauver des jambes en faisant pousser de nouveaux vaisseaux sanguins
Lorsque les artères des jambes se bouchent progressivement, les personnes peuvent souffrir de douleurs invalidantes, d’ulcères rebelles et même être confrontées à l’amputation. Ce stade sévère, appelé ischémie critique des membres, est notoirement difficile à traiter car de nombreux patients ne peuvent pas subir de pontage ou d’autres procédures standard. L’étude résumée ici explore une nouvelle stratégie : utiliser deux types de cellules proches des cellules souches, prélevées dans la graisse d’un patient, pour aider l’organisme à générer de nouveaux vaisseaux robustes capables de sauver les tissus privés d’oxygène du membre.
Une maladie fréquente avec des options limitées
La maladie artérielle périphérique survient lorsque les artères des jambes se rétrécissent, privant les tissus d’un apport sanguin suffisant. À son stade le plus grave, l’ischémie critique des membres, les personnes peuvent souffrir de douleurs continues, d’orteils noircis et d’un risque élevé de perdre une partie du membre. Les thérapies actuelles, comme les hypolipémiants, l’angioplastie ou le pontage chirurgical peuvent aider, mais beaucoup de patients ne répondent pas ou sont trop malades pour ces interventions. Les tentatives antérieures utilisant un seul type de cellule souche ont surtout favorisé des vaisseaux fragiles et très fins qui n’apportent pas un flux suffisant pour sauver de manière fiable le membre. Les chercheurs ont donc cherché à construire un « système de plomberie » plus complet en combinant deux types cellulaires coopératifs.
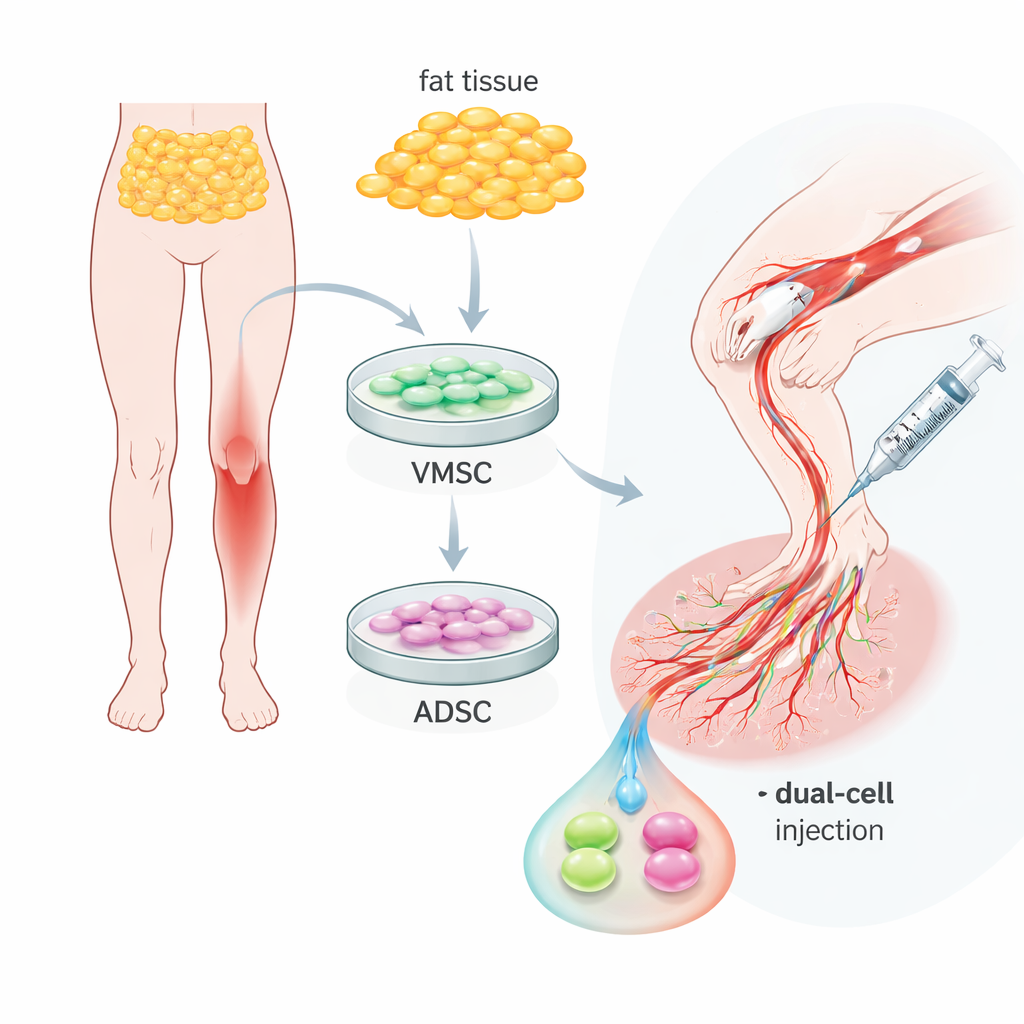
Deux types cellulaires utiles dans la graisse corporelle ordinaire
L’équipe s’est concentrée sur le tissu adipeux — la graisse corporelle ordinaire — pouvant être prélevé par des procédures relativement mineures. À partir du même échantillon, ils ont isolé deux populations cellulaires apparentées mais distinctes. Un groupe, qualifié de cellules souches multipotentes vasculaires, se comportait comme des cellules précoces de la paroi vasculaire : elles présentaient des marqueurs de surface typiques des cellules endothéliales et pouvaient s’organiser en tubes de type capillaire en culture. Le second groupe, des cellules souches dérivées de l’adipose, ressemblait davantage à des cellules de soutien qui entourent les vaisseaux, portant des marqueurs observés dans les cellules musculaires lisses et les cellules périvasculaires. Les deux types pouvaient bien se multiplier et se différencier en adipocytes, ostéocytes ou chondrocytes, confirmant leur plasticité, mais leurs rôles naturels autour des vaisseaux étaient clairement différents et complémentaires.
Travailler ensemble sous stress
Pour reproduire l’environnement agressif et inflammatoire d’un membre malade, les chercheurs ont exposé les cellules à un signal inflammatoire puissant. Les deux types cellulaires ont survécu et ont ajusté leur comportement en libérant des mélanges de facteurs de croissance et d’enzymes qui favorisent la migration cellulaire et la remodelation du tissu environnant. Cultivées seules sur un gel favorisant la formation de vaisseaux, les cellules de type endothélial pouvaient former des tubes basiques, tandis que les cellules de soutien restaient majoritairement en amas. Cependant, mélangées dans un rapport deux pour un, les tubes devenaient plus denses, plus continus et plus résistants au stress inflammatoire. Cela suggère que, ensemble, les deux types cellulaires peuvent former non seulement davantage de vaisseaux, mais aussi des réseaux plus matures et stables.
Tester la thérapie double-cellulaire dans des membres de souris malades
Les scientifiques sont ensuite passés à un modèle murin d’ischémie critique des membres obtenu en sectionnant une artère principale de la patte. Dans le muscle du membre privé de circulation, ils ont injecté les cellules humaines mélangées. Sur quatre semaines, les souris non traitées perdaient fréquemment des orteils voire des pieds entiers, et leurs muscles présentaient des cicatrices et une forte inflammation. En revanche, les animaux ayant reçu le traitement double-cellulaire ont majoritairement conservé leurs membres. Les mesures du flux sanguin ont montré que la circulation dans les membres traités retrouvait environ 70 % de la normale, contre moins de 20 % chez les témoins. L’imagerie microscopique et tridimensionnelle a révélé la raison : les muscles traités contenaient beaucoup plus de vaisseaux de taille moyenne et large — des branches de type artériole — avec de solides « manchons » de cellules de soutien, plutôt qu’un enchevêtrement de capillaires minuscules et instables.
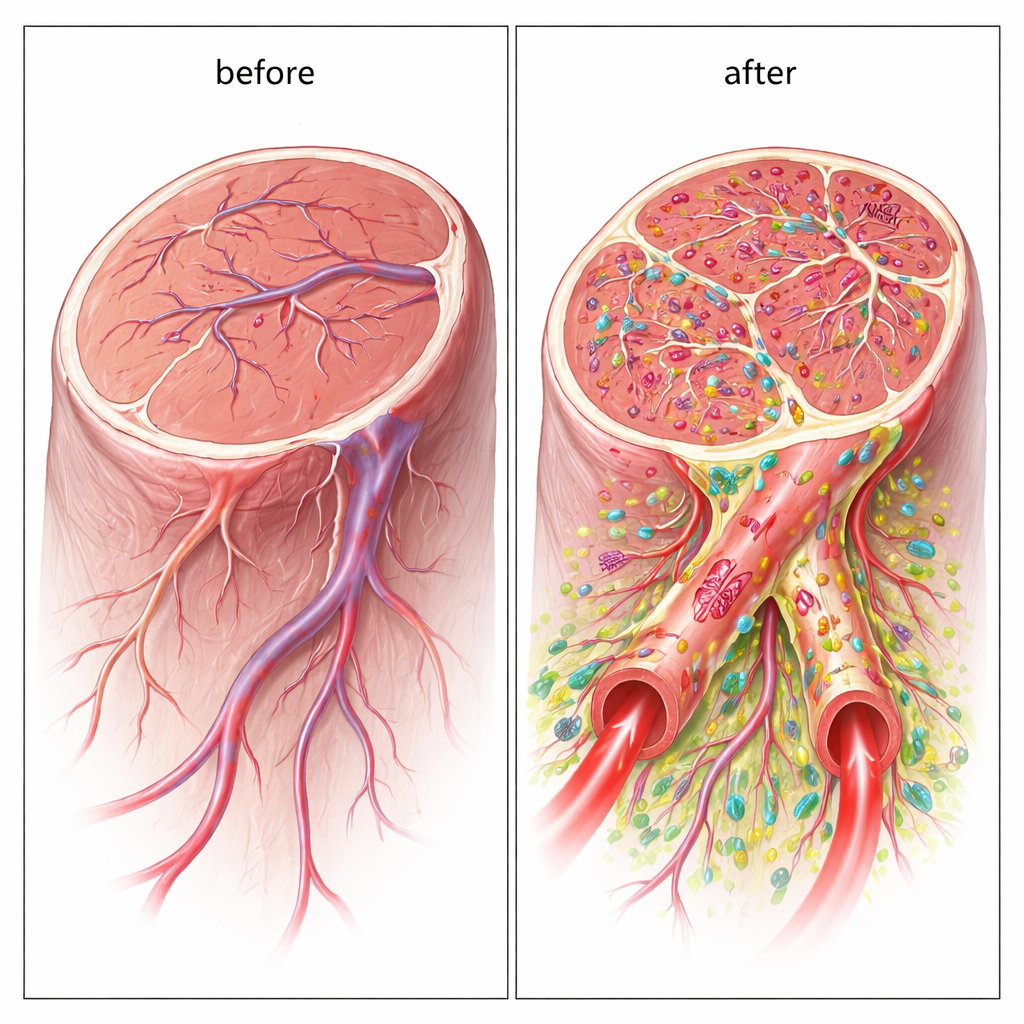
Des vaisseaux hybrides construits à partir de cellules donneuses
Fait important, les nouveaux vaisseaux n’étaient pas seulement induits par les cellules : ils contenaient réellement les cellules humaines transplantées comme partie intégrante de leurs parois. À l’aide de marqueurs spécifiques à l’humain, les chercheurs ont montré que les cellules de type endothélial contribuaient à la formation de la couche interne, tandis que les cellules de soutien entouraient l’extérieur. Beaucoup de ces vaisseaux hybrides étaient suffisamment larges pour fonctionner comme de véritables conduits sanguins, et des traceurs fluorescents ont confirmé que le sang y circulait. Cette construction directe de vaisseaux larges et perfusés distingue l’approche double-cellulaire de la plupart des thérapies cellulaires antérieures, qui reposent principalement sur des signaux chimiques plutôt que sur une intégration structurelle durable.
Ce que cela pourrait signifier pour les patients
Pour un non-spécialiste, le message est que les chercheurs pourraient apprendre à « re-canalyser » des membres en voie de mort en utilisant les propres cellules adipeuses du patient. En associant deux types cellulaires — l’un formant le tube interne et l’autre construisant le soutien externe — la thérapie génère des artères et des artérioles solides et bien tapissées plutôt que des bourgeonnements fragiles. Chez la souris, cela a suffi à restaurer le flux sanguin et à prévenir la perte du membre. Bien que des travaux supplémentaires soient nécessaires pour établir la sécurité et l’efficacité à long terme chez l’humain, l’étude ouvre la voie à un avenir où une simple récolte de graisse peu invasive pourrait fournir des mélanges cellulaires personnalisés pour reconstruire la circulation chez les patients à haut risque d’amputation.
Citation: Kim, D.Y., Hwang, D.Y., Park, G. et al. Adipose-derived dual cell therapy enhances arteriogenesis and limb preservation through vascular integration in critical limb ischemia. npj Regen Med 11, 13 (2026). https://doi.org/10.1038/s41536-026-00458-x
Mots-clés: ischémie critique des membres, thérapie par cellules souches, cellules dérivées du tissu adipeux, néovascularisation, maladie artérielle périphérique