Clear Sky Science · fr
Nouveau hydrogel chargé en andrographolide coordonné par des ions cuivre active l’axe Rac1/JNK1 pour améliorer la cicatrisation des plaies diabétiques
Pourquoi les plaies tenaces comptent
Pour de nombreuses personnes atteintes de diabète, une petite ampoule au pied peut dégénérer en une plaie chronique qui refuse de se refermer, menant parfois à une amputation. Ces lésions difficiles à guérir sont alimentées par l’infection, une inflammation incontrôlée et un apport sanguin insuffisant. L’article résumé ici décrit un nouveau pansement gélifié qui vise à traiter simultanément ces trois problèmes, en utilisant un composé végétal et un oligo-élément pour inciter la peau endommagée à renouer avec un processus de réparation sain.
Un pansement intelligent construit à partir d’un gel
Les chercheurs ont mis au point un matériau souple et riche en eau, connu sous le nom d’hydrogel, conçu pour être appliqué directement sur la plaie. Il est composé de gélatine (une protéine issue du collagène) et d’une forme modifiée de chitosane, un polymère à base de sucres. Les ions cuivre jouent le rôle de petits connecteurs, reliant les composants en un réseau flexible tout en complexant une molécule végétale appelée andrographolide, reconnue pour ses effets anti-inflammatoires, antimicrobiens et hypoglycémiants. Cette coordination au cuivre améliore fortement la solubilité aqueuse du médicament et permet de le maintenir uniformément dans le gel au lieu de former des cristaux, ce qui est crucial pour une libération régulière dans la plaie.
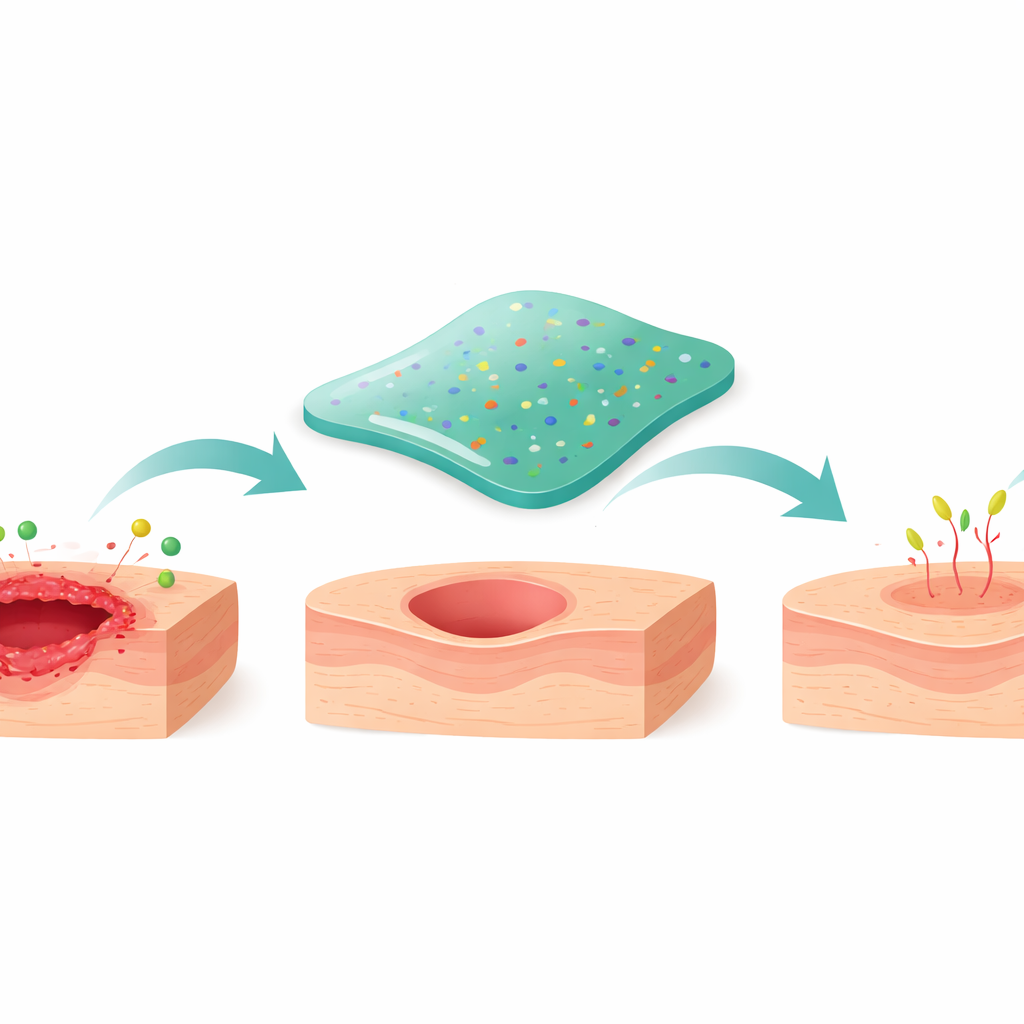
Conçu pour rester en place et s’auto-réparer
Un pansement doit adhérer à une peau humide et mobile, absorber les liquides et rester intact. Des tests physiques détaillés ont montré que la version optimisée du gel (appelée ASFH-L) se comporte comme un solide mou : elle peut se déformer pour épouser la surface de la plaie tout en résistant à l’écoulement. Au microscope, elle présente une structure poreuse interconnectée suffisamment large pour laisser passer nutriments et cellules, sans être si lâche qu’elle se désagrège. Lorsqu’il est étiré ou brièvement endommagé, ses liaisons à base de cuivre se reforment, conférant à l’hydrogel une capacité d’« auto‑réparation » qui permet à un morceau coupé de se ressouder en quelques minutes. Sur peau de porc humide, ASFH-L est resté fixé malgré des flexions et torsions répétées sous l’eau, ce qui suggère qu’il pourrait protéger des plaies réelles sans réapplication fréquente.
Lutter contre les germes et aider la migration des cellules cutanées
Les plaies diabétiques chroniques sont souvent colonisées par des bactéries. Dans des tests en laboratoire contre des agents fréquents tels que Staphylococcus aureus et Escherichia coli, toutes les versions de l’hydrogel ont ralenti la croissance bactérienne, et celles contenant davantage d’andrographolide ont produit des zones d’inhibition plus larges. Parallèlement, les extraits d’ASFH-L se sont montrés compatibles avec les cellules cutanées humaines, maintenant leur viabilité et même stimulant leur prolifération sur une période de 24 heures à des doses appropriées. Lorsque des cellules cutanées ont été cultivées en conditions de forte glycémie, qui réduisent habituellement leur capacité de migration, l’ajout des extraits de l’hydrogel a accéléré leur progression dans des zones rayées in vitro. Cette augmentation de la motilité est importante, car la fermeture d’une plaie dépend de la migration des cellules cutanées pour recouvrir la zone exposée.
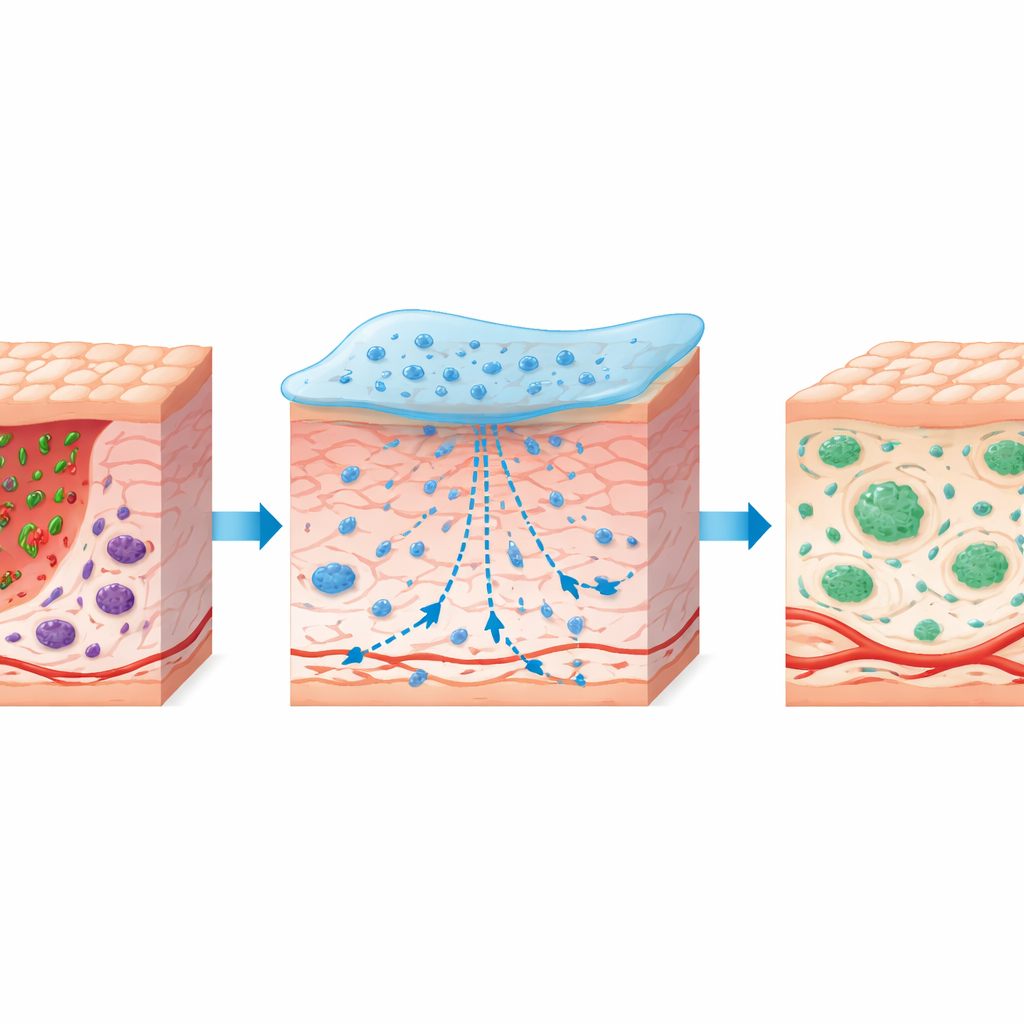
Orienter l’organisme de l’inflammation vers la réparation
Chez des souris diabétiques présentant des plaies circulaires sur le dos, l’hydrogel ASFH-L a accéléré la fermeture par rapport aux témoins non traités et à un gel similaire dépourvu du composé végétal. Les plaies traitées présentaient une nouvelle peau externe plus épaisse, des fibres de collagène mieux ordonnées et même une repousse des follicules pileux. L’imagerie du flux sanguin et les colorations tissulaires ont révélé des réseaux plus denses de petits vaisseaux et davantage de cellules de soutien de type musculaire autour d’eux, suggérant une meilleure distribution des nutriments. Au niveau immunitaire, le pansement a modulé le comportement des macrophages — cellules de première ligne qui peuvent soit entretenir l’inflammation (type M1) soit l’apaiser et soutenir la reconstruction (type M2). ASFH-L a réduit la population pro-inflammatoire M1 et augmenté le groupe pro-réparateur M2, tout en diminuant des signaux nocifs tels que IL‑1β et TNF‑α et en augmentant le messager apaisant IL‑10. Ce basculement coordonné reflète la transition naturelle d’une phase initiale de « nettoyage » vers une véritable réparation tissulaire, qui est souvent bloquée dans les plaies diabétiques.
Un interrupteur moléculaire pour la guérison
Pour comprendre comment un composé végétal dans un gel pouvait orchestrer ces effets, l’équipe a utilisé la modélisation informatique, l’exploration de bases de données et des mesures biophysiques. Ils ont découvert que l’andrographolide peut se lier directement à une petite protéine de signalisation appelée Rac1 et, via celle‑ci, activer une cascade de molécules (JNK1, Jun et Fos) qui régulent collectivement le mouvement cellulaire, la croissance, l’inflammation et la néo‑angiogenèse. Les simulations ont montré une liaison stable et énergétiquement favorable entre l’andrographolide et Rac1, et des expériences de surface ont confirmé cette interaction en temps réel. Dans les plaies des souris, les gènes et protéines de l’axe Rac1/JNK1/Jun/Fos étaient plus actifs dans le groupe traité par l’hydrogel. En termes simples, le pansement ne se contente pas de recouvrir la plaie ; il délivre un ingrédient botanique qui déclenche un interrupteur de réparation intrinsèque aux cellules.
Ce que cela pourrait signifier pour les patients
Ce travail présente un pansement « intelligent » qui combine contrôle des infections, apaisement immunitaire et stimulation de la formation de vaisseaux sanguins en une seule plateforme hydrogel auto‑réparatrice. En utilisant des ions cuivre pour solubiliser et libérer lentement l’andrographolide, le matériau transforme un composé végétal difficile à administrer en une thérapie locale pratique. Chez des animaux diabétiques, cette approche accélère la fermeture, organise le tissu cicatriciel et rééquilibre la réponse immunitaire, tout en s’appuyant sur une voie moléculaire définie. Bien que des essais cliniques chez l’homme restent nécessaires, le concept ouvre la voie à des pansements futurs qui font bien plus que couvrir une plaie — ils guident activement le tissu endommagé à travers chaque étape du processus de réparation.
Citation: Ye, P., Dai, Y., Zhang, Q. et al. Novel copper-ion coordinated andrographolide-loaded hydrogel activates Rac1/JNK1 axis for enhancing diabetic wound healing. npj Regen Med 11, 14 (2026). https://doi.org/10.1038/s41536-026-00457-y
Mots-clés: cicatrisation des plaies diabétiques, pan, pan, andrographolide, polarisation des macrophages, angiogenèse