Clear Sky Science · fr
Inhibition de CDK8 sauve la réparation osseuse altérée par ischémie
Pourquoi la circulation compte quand un os se brise
La majorité des fractures finissent par se consolider, mais pour des millions de personnes chaque année, ce processus s’interrompt. Une mauvaise irrigation sanguine autour d’une fracture — appelée ischémie — augmente fortement le risque que la cassure cicatrise lentement, mal, ou pas du tout. Cette étude explore pourquoi cela se produit au niveau cellulaire et teste un traitement expérimental par voie orale qui semble orienter la réparation loin d’un tissu cicatriciel vers une véritable régénération osseuse.
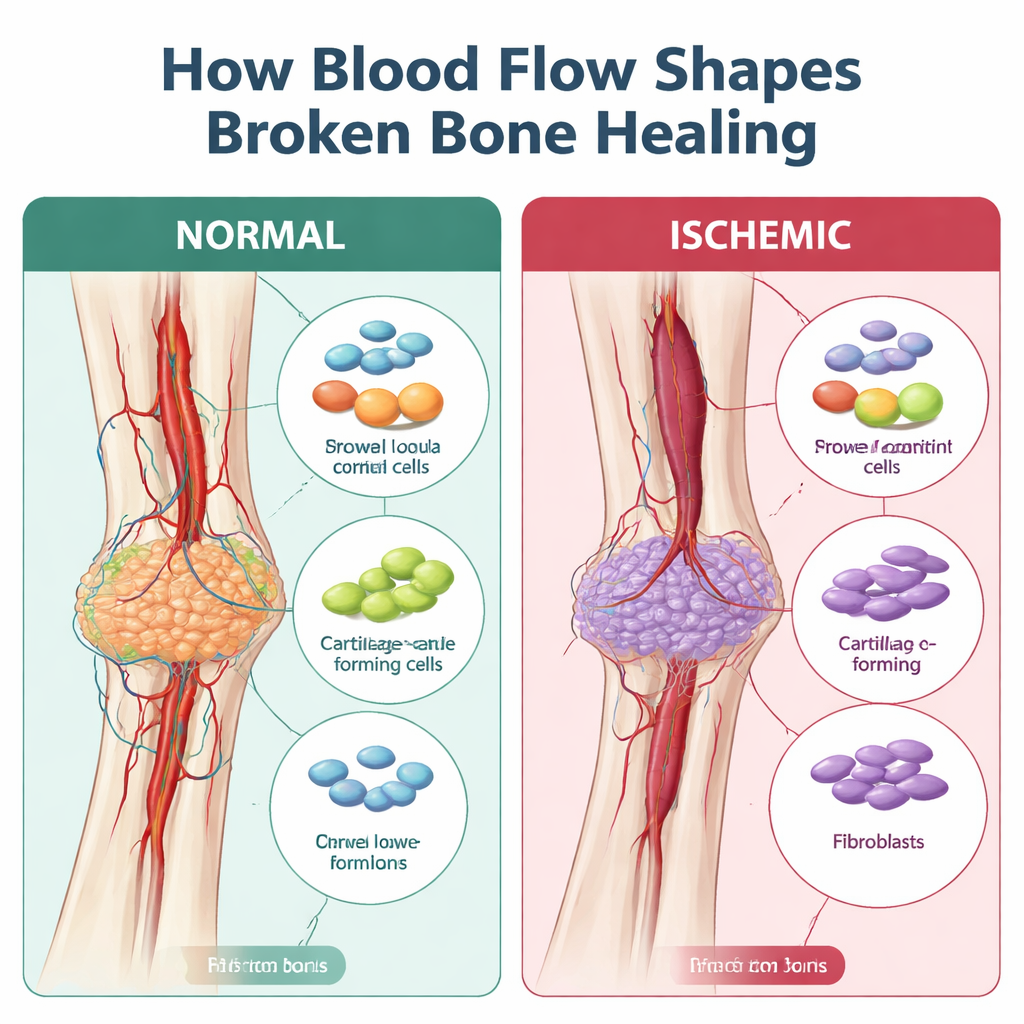
Quand la guérison tourne à la cicatrice plutôt qu’à la reconstruction
L’os guérit normalement en formant un pont mou de cartilage qui est progressivement remplacé par de l’os dur. Ce pont, appelé cal, dépend d’un apport de cellules souches ou de soutien, de cellules immunitaires et de vaisseaux sanguins qui coordonnent la réparation. Dans les fractures ischémiques, des travaux antérieurs ont montré que le cal tend à être plus petit, plus faible et rempli de tissu fibreux, davantage comme une cicatrice que comme une nouvelle masse osseuse solide. Ce qui manquait était une cartographie détaillée des cellules qui dévient, et du moment où elles le font, au cours de cet écart par rapport à une guérison normale.
Les cellules uniques révèlent une bifurcation vers la fibrose
Les chercheurs ont utilisé un modèle murin dans lequel une artère de la jambe est lésée chirurgicalement au moment de la fracture, reproduisant fidèlement la perte de flux sanguin observée dans les blessures sévères ou chez les personnes souffrant de maladies vasculaires ou qui fument. Ils ont ensuite appliqué le séquençage de l’ARN à cellule unique, une technique qui lit les gènes actifs dans des milliers de cellules individuelles, aux cals de fracture quatre et sept jours après la lésion. Dans les fractures bien perfusées, le cal précoce était rempli de cellules immunitaires qui laissaient bientôt place à l’expansion de cellules stromales — les cellules de soutien qui deviendront cartilage et os. En conditions ischémiques, en revanche, il y avait beaucoup moins de cellules formant du cartilage et de l’os et beaucoup plus de fibroblastes, les cellules qui déposent du tissu fibreux. Une analyse computationnelle des « trajectoires » a montré que, au lieu de mûrir progressivement de progéniteurs précoces en cartilage, les cellules stromales dans l’os ischémique divergeaient souvent vers un état de type fibroblaste, ce qui correspond au cal plus cicatriciel observé au microscope.
Un frein moléculaire sur les cellules ossifiantes
En examinant l’activité génique de ces cellules, l’équipe a identifié un fort signal de stress cellulaire dans les cals ischémiques, incluant des niveaux élevés de protéines de choc thermique. Parmi les changements les plus marquants figurait une hausse d’activité d’un gène appelé Cdk8, qui code pour une enzyme régulatrice située dans un complexe transcriptionnel majeur et pouvant ralentir ou rediriger la façon dont les cellules répondent aux signaux. Cdk8 est connu pour bloquer la différenciation cellulaire dans d’autres contextes. Ici, il était particulièrement élevé dans les progéniteurs stromaux précoces de l’os ischémique. Des cellules stromales mésenchymateuses humaines cultivées en conditions de faible oxygène — imitant le mauvais apport sanguin — ont également augmenté l’expression de CDK8, reliant directement la pénurie d’oxygène à ce possible « frein » sur la formation de cartilage et d’os.
Éteindre CDK8 pour sauver la réparation
Les chercheurs ont ensuite testé si bloquer CDK8 pouvait libérer les cellules stromales pour reprendre une réparation appropriée. En culture cellulaire, le traitement des progéniteurs murins et humains par des inhibiteurs sélectifs de CDK8 a stimulé des gènes clés du cartilage et augmenté la production de matrice cartilagineuse, tout en favorisant aussi la minéralisation lorsque les mêmes cellules étaient dirigées vers une voie osseuse. L’équipe a ensuite testé un inhibiteur oral de CDK8/19 appelé SNX631-6 chez des souris présentant des fractures ischémiques. Administré durant la fenêtre précoce de formation du cartilage, le médicament a augmenté la quantité de cartilage dans le cal. Lorsque le traitement a été prolongé pendant la transition ultérieure du cartilage vers l’os, les cals présentaient plus d’os total, une teneur minérale plus élevée et une taille globale plus importante sur les scans micro–CT et les coupes tissulaires, indiquant une réparation structurelle plus robuste.
De l’éclairage en laboratoire à de possibles nouvelles thérapies
Pris ensemble, les résultats suggèrent que l’ischémie oriente les cellules réparatrices vers un destin stressé et fibrotique en partie en augmentant CDK8, ce qui limite leur capacité à devenir cartilage et os. Bloquer cette enzyme semble relâcher ce frein, permettant la formation de davantage de cartilage tôt et la déposition de plus d’os plus tard, même lorsque l’apport sanguin est compromis. Parce que des inhibiteurs de CDK8 sont déjà testés chez des patients cancéreux, ils pourraient un jour être réutilisés pour aider les personnes à haut risque de mauvaise consolidation — comme les personnes âgées, les fumeurs ou celles atteintes de maladies vasculaires — à régénérer un os solide plutôt qu’un tissu cicatriciel fragile.
Citation: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Mots-clés: réparation des fractures osseuses, ischémie, inhibiteur de CDK8, cellules stromales mésenchymateuses, fibrose