Clear Sky Science · fr
Engraissement de cellules épithéliales alvéolaires de type II de type sauvage chez des souris déficientes en la protéine surfactante C
Pourquoi réparer les minuscules sacs aériens est important
La respiration peut sembler facile, mais elle repose sur un film délicat appelé surfactant qui tapisse des millions de minuscules sacs aériens dans nos poumons. Quand le surfactant manque ou est défectueux, comme dans certaines maladies pulmonaires infantiles rares, les enfants peuvent souffrir de problèmes respiratoires persistants et de cicatrices du poumon. Aujourd’hui, la seule vraie guérison est la transplantation pulmonaire, une option limitée par la pénurie de donneurs et des risques sérieux. Cette étude explore une idée différente : réparer les poumons endommagés en transplantant des cellules productrices de surfactant saines, ouvrant potentiellement la voie à des traitements plus ciblés et moins agressifs.
Quand les « gardiens » du poumon dysfonctionnent
À l’intérieur de chaque sac aérien (alvéole) se trouvent des cellules spécialisées, sortes de « gardiennes », appelées cellules alvéolaires de type II. Elles produisent et recyclent le surfactant, qui empêche l’affaissement des alvéoles et facilite la respiration. Chez certains enfants, des mutations dans des gènes nécessaires à la production du surfactant, y compris le gène de la protéine surfactante C (SFTPC), perturbent ces cellules. Le résultat est une maladie pulmonaire interstitielle de l’enfant (chILD), caractérisée par une inflammation et un épaississement du tissu pulmonaire, des cicatrices et parfois une insuffisance respiratoire. Les médecins ne peuvent offrir que des traitements de soutien et de l’oxygène ; pour les cas les plus graves, la transplantation pulmonaire reste le dernier recours. Les auteurs ont cherché à tester si remplacer une partie de ces cellules défaillantes par des cellules saines pouvait ralentir ou inverser les lésions pulmonaires.
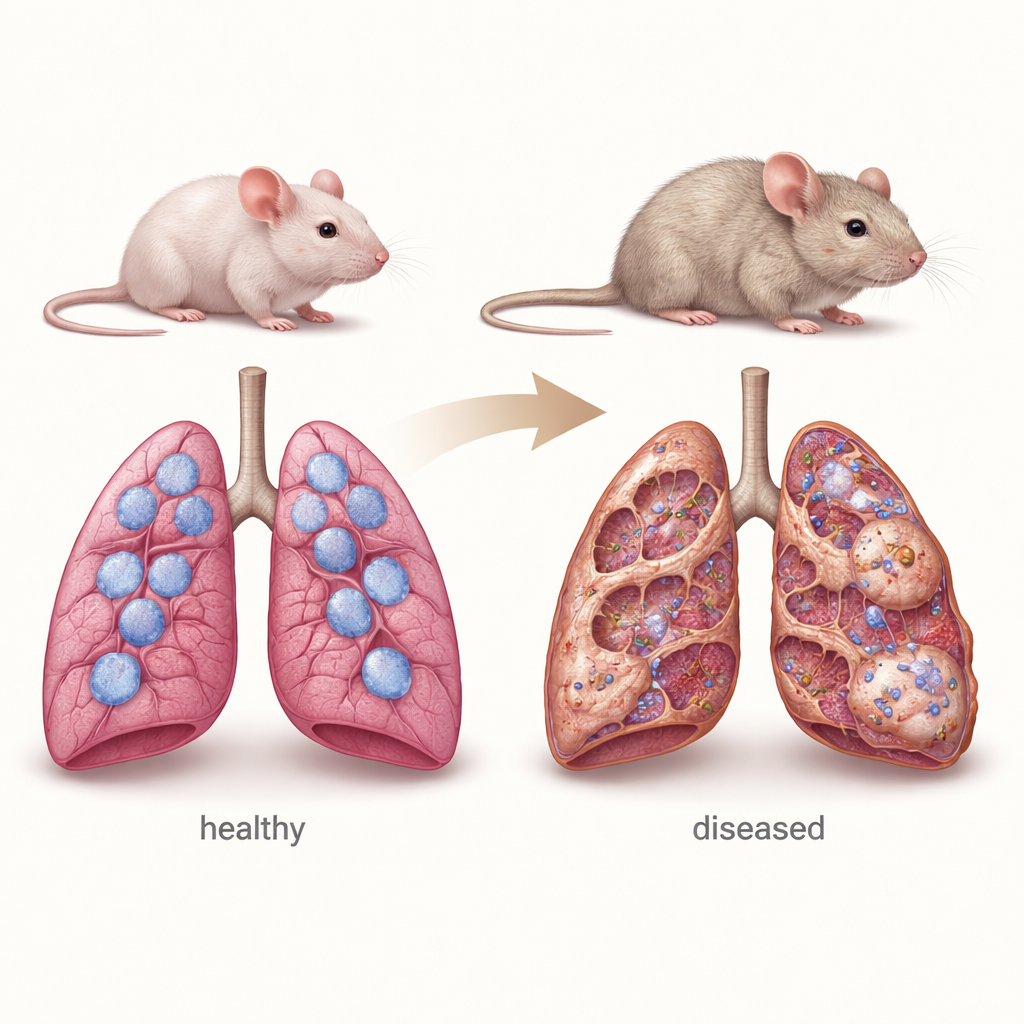
Un modèle murin pour la maladie pulmonaire infantile
Pour reproduire les caractéristiques clés de la chILD, les chercheurs ont utilisé des souris totalement dépourvues du gène Sftpc. Ces animaux naissent avec des poumons apparemment normaux, mais en vieillissant ils développent des signes de maladie pulmonaire chronique : épaississement des cloisons entre alvéoles, tissu cicatriciel supplémentaire riche en collagène, prolifération des cellules de type II et accumulation de cellules immunitaires. Des mesures détaillées ont montré que l’architecture pulmonaire se détériore progressivement entre 4 et 12 mois, ressemblant à la progression lente observée chez de nombreux patients humains. L’équipe a également constaté que ces souris sont particulièrement sensibles à la chimiothérapie bleomycine, médicament souvent utilisé en laboratoire pour provoquer des lésions pulmonaires et une fibrose, ce qui souligne la vulnérabilité de leurs poumons déficients en surfactant.
Préparer des poumons endommagés à recevoir de nouvelles cellules
Transplanter avec succès de nouvelles cellules dans un organe déjà saturé n’est pas trivial. Les auteurs ont testé si une faible dose soigneusement choisie de bleomycine pouvait agir comme un traitement de « conditionnement » — endommageant certaines cellules résidentes défectueuses et libérant de l’espace pour les nouvelles sans détruire le poumon. Chez les souris déficientes en Sftpc, même de petites quantités de bleomycine aggravèrent la fibrose et abaissèrent les niveaux de plusieurs marqueurs importants des cellules de type II, confirmant la lésion. Pourtant, à la dose la plus faible, les dégâts restaient limités et la réponse réparatrice propre du poumon demeurait active. Cet équilibre a suggéré une fenêtre dans laquelle les cellules transplantées pourraient avoir la meilleure chance de s’ancrer, de survivre et de contribuer à la guérison.
Des cellules surfactantes saines s’installent et se mettent au travail
L’équipe a ensuite isolé des cellules de type II saines chez des souris normales et a administré un million de ces cellules directement dans les voies respiratoires de souris déficientes en Sftpc dix jours après une faible dose de bleomycine. À l’aide d’un mélange de marquages protéiques et de tests génétiques, ils ont montré que les cellules donneuses s’engrafaient efficacement, en particulier chez les animaux plus jeunes. Ces cellules transplantées produisaient la protéine surfactante C mature — complètement absente chez l’hôte — indiquant qu’elles n’étaient pas seulement présentes mais fonctionnelles. Les nouvelles cellules ont persisté pendant au moins deux mois. Fait important, les souris ayant reçu les greffes cellulaires présentaient moins de lésions pulmonaires et moins de régions gravement endommagées comparées aux souris traitées uniquement par la bleomycine, suggérant que même un remplacement partiel des cellules malades peut atténuer les dommages en cours.
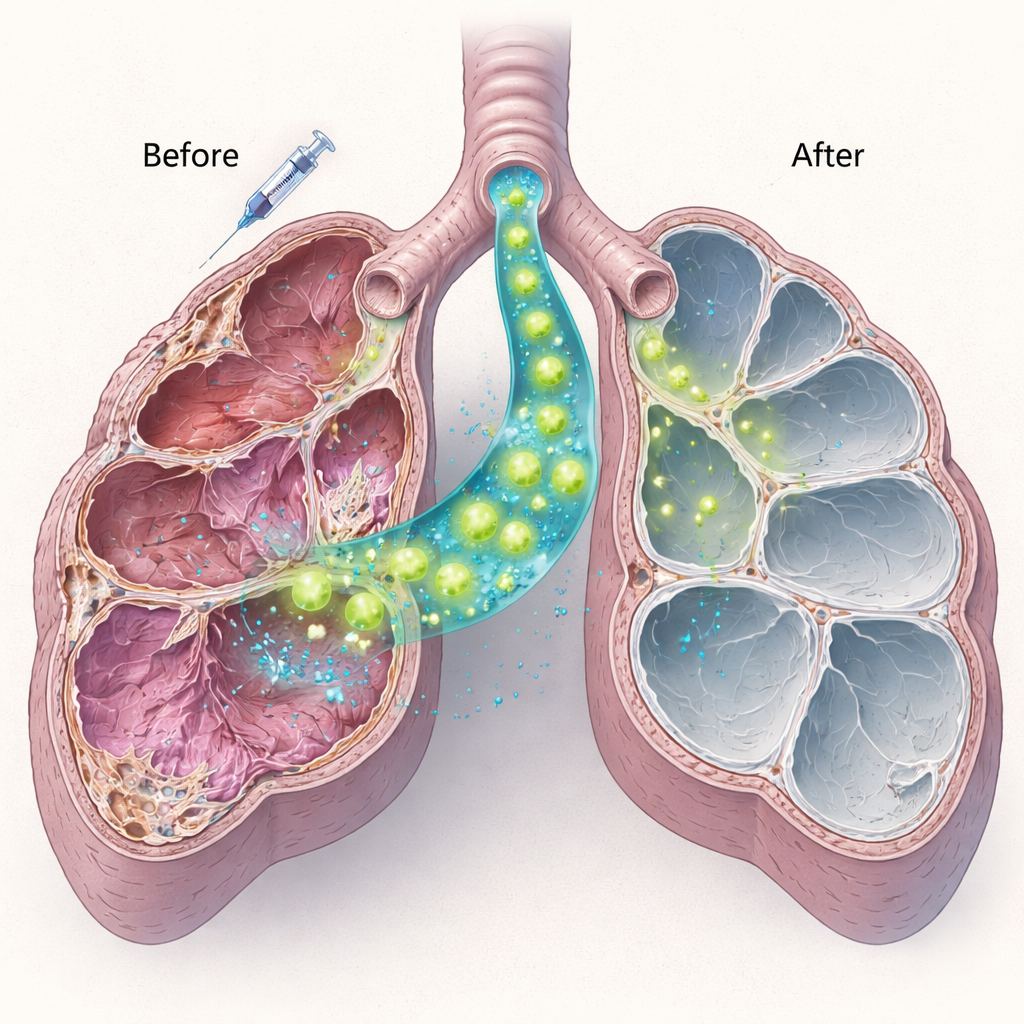
Du proof-of-concept aux thérapies futures
Pour un public non spécialiste, le message clé est que cette étude démontre une voie réaliste pour réparer, plutôt que remplacer, les poumons dans certaines maladies génétiques infantiles. En montrant qu’un nombre modeste de cellules productrices de surfactant saines peut s’enraciner dans un poumon chroniquement malade, produire la protéine manquante et réduire les lésions, ce travail offre une base pour des thérapies futures basées sur des cellules pulmonaires corrigées par génie génétique ou dérivées de cellules souches. De nombreux obstacles subsistent, y compris la recherche de méthodes plus sûres pour préparer les poumons humains à ce type de traitement et garantir un bénéfice durable. Néanmoins, cette recherche déplace la conversation de la gestion des symptômes vers la possibilité de reconstruire la machinerie pulmonaire elle‑même pour une respiration saine.
Citation: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Mots-clés: maladie pulmonaire interstitielle de l’enfant, protéine surfactante C, cellules alvéolaires de type II, thérapie cellulaire, fibrose pulmonaire