Clear Sky Science · fr
La carte sensorielle olfactive est perturbée dans un modèle murin transgénique de la maladie de Parkinson surexprimant l’α-synucléine humaine de type sauvage
Pourquoi la perte de l’odorat importe dans la maladie de Parkinson
Beaucoup de personnes considèrent la maladie de Parkinson comme un trouble moteur, mais chez la plupart des patients, la première fonction à se détériorer est l’odorat. Cette perte peut apparaître des décennies avant les tremblements ou la raideur, ce qui en fait un signal précoce puissant. L’étude décrite ici pose une question simple mais encore sans réponse : qu’est-ce qui dysfonctionne précisément dans le circuit olfactif du cerveau au tout début des changements liés à la maladie de Parkinson ? En explorant cette question dans un modèle murin soigneusement conçu, les chercheurs dévoilent comment une protéine clé de la maladie perturbe la « carte olfactive » interne du cerveau et pointent vers une nouvelle source facilement accessible d’indices précoces de la maladie.
La carte olfactive du cerveau
Nos nez contiennent des millions de cellules spécialisées qui répondent chacune à des molécules odorantes particulières. Ces cellules envoient de longues fibres fines vers l’avant du cerveau, où elles convergent en petits noyaux appelés glomérules à l’intérieur du bulbe olfactif. Chaque type d’odeur active un motif spécifique de glomérules, formant une carte sensorielle précise qui permet au cerveau de distinguer le café de la cannelle ou la fumée d’un parfum. Chez les souris en bonne santé, les cellules portant un récepteur odorant donné (appelé M72) et un autre (appelé P2) projettent de manière fiable vers seulement deux glomérules bien définis par bulbe, créant une carte très ordonnée et reproductible.
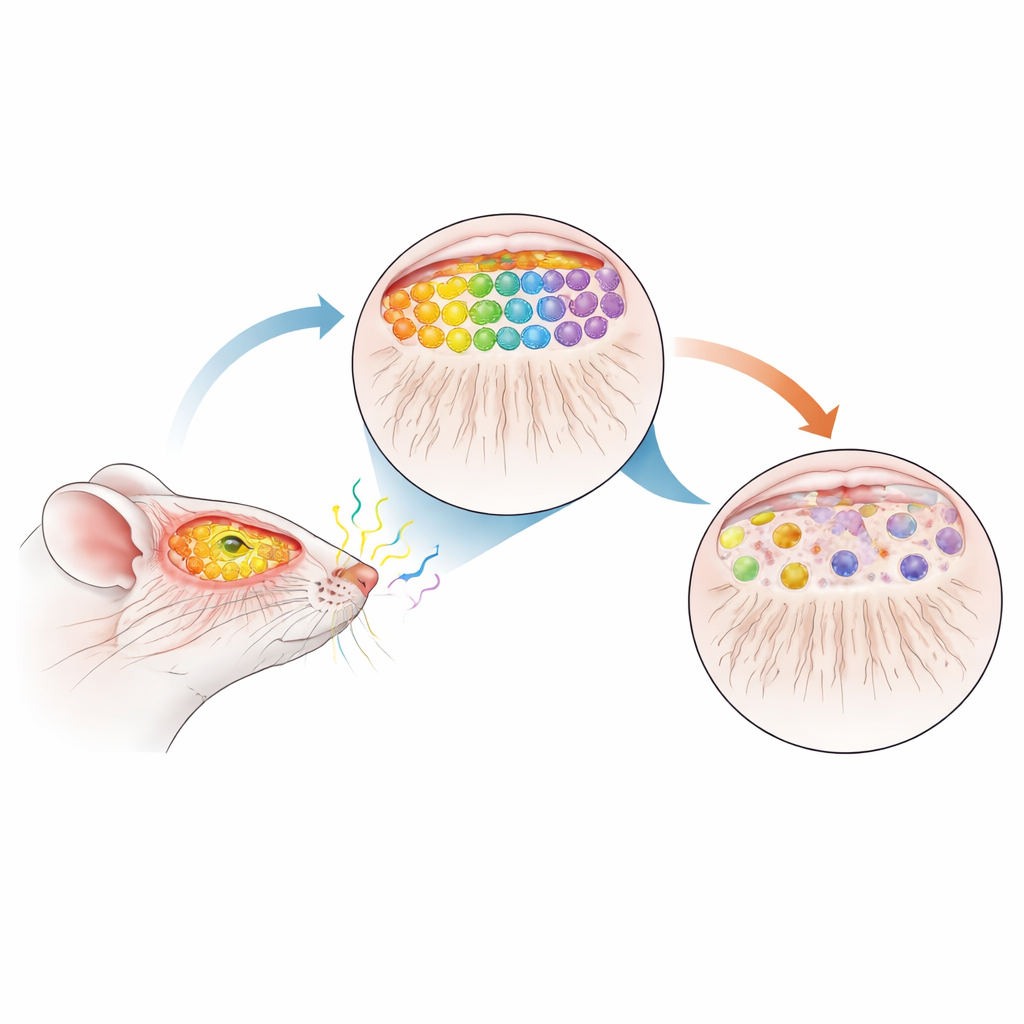
Une souris substitut pour la phase précoce de la maladie de Parkinson
Pour voir comment la maladie de Parkinson pourrait perturber cette carte, l’équipe a utilisé des souris qui produisent en excès l’α-synucléine humaine normale, la même protéine qui s’agrège dans le cerveau des personnes atteintes de Parkinson. Ils ont ensuite croisé ces animaux avec des souris marquées pour M72 et P2 afin de pouvoir suivre visuellement des populations cellulaires olfactives sélectionnées et leurs connexions. Fait important, l’excès d’α-synucléine ne s’exprime qu’après la naissance et s’accumule progressivement avec l’âge, reproduisant la course lente et progressive de la maladie humaine. À 12 mois — approximativement l’âge d’un milieu de vie chez la souris et comparable à une phase prodromique, ou pré-diagnostic, chez l’humain — les chercheurs ont examiné en détail les systèmes olfactifs des animaux.
Quand la carte olfactive se délite
En colorant les neurones marqués et en suivant leurs trajets, les scientifiques ont observé un effondrement frappant de la carte olfactive chez les souris surexprimant l’α-synucléine. Le nombre de neurones M72 et P2 dans le nez a fortement diminué — environ trois quarts de perte pour M72 et près de la moitié pour P2 — tandis que leurs fibres vers le bulbe étaient fortement réduites. Plutôt que de converger proprement vers deux glomérules robustes, les fibres restantes formaient souvent plusieurs glomérules plus petits de tailles et de positions variables. Ces noyaux « supplémentaires » n’apparaissaient pas à des emplacements cohérents d’une souris à l’autre, signalant une perte de la précision topographique normale. Un marqueur large des terminaisons des cellules olfactives, VGLUT2, était également réduit d’environ 44 % dans le bulbe, indiquant que cette dégénérescence dépassait largement les deux types de récepteurs marqués.
Relier des circuits brisés à la perte d’odorat
Les dommages structurels se traduisaient par des déficits olfactifs mesurables. Les souris âgées surexprimant l’α-synucléine mettaient plus de temps à trouver de la nourriture cachée, présentaient une moindre capacité à distinguer une odeur d’une autre et ne montraient pas de préférence pour des zones marquées par leur propre odeur — des tests comportementaux qui révèlent ensemble une hyposmie et une altération de la discrimination odorante. Elles nécessitaient aussi des concentrations d’odeur beaucoup plus élevées pour répondre, révélant une sensibilité réduite. Ces déficits n’apparaissaient pas chez les souris plus jeunes, chez lesquelles les neurones marqués et leurs cartes semblaient encore en grande partie normaux, liant la chronologie de la perte fonctionnelle à la détérioration ultérieure de la carte sensorielle plutôt qu’au développement précoce. Notamment, bien que la protéine problématique fût abondante dans le bulbe olfactif, elle n’était pas détectable dans l’épithélium sensoriel du nez lui-même, ce qui oriente vers des changements au sein du circuit du bulbe — en particulier dans les cellules mitrales qui relaient l’information olfactive — comme principaux moteurs de la perturbation de la carte.
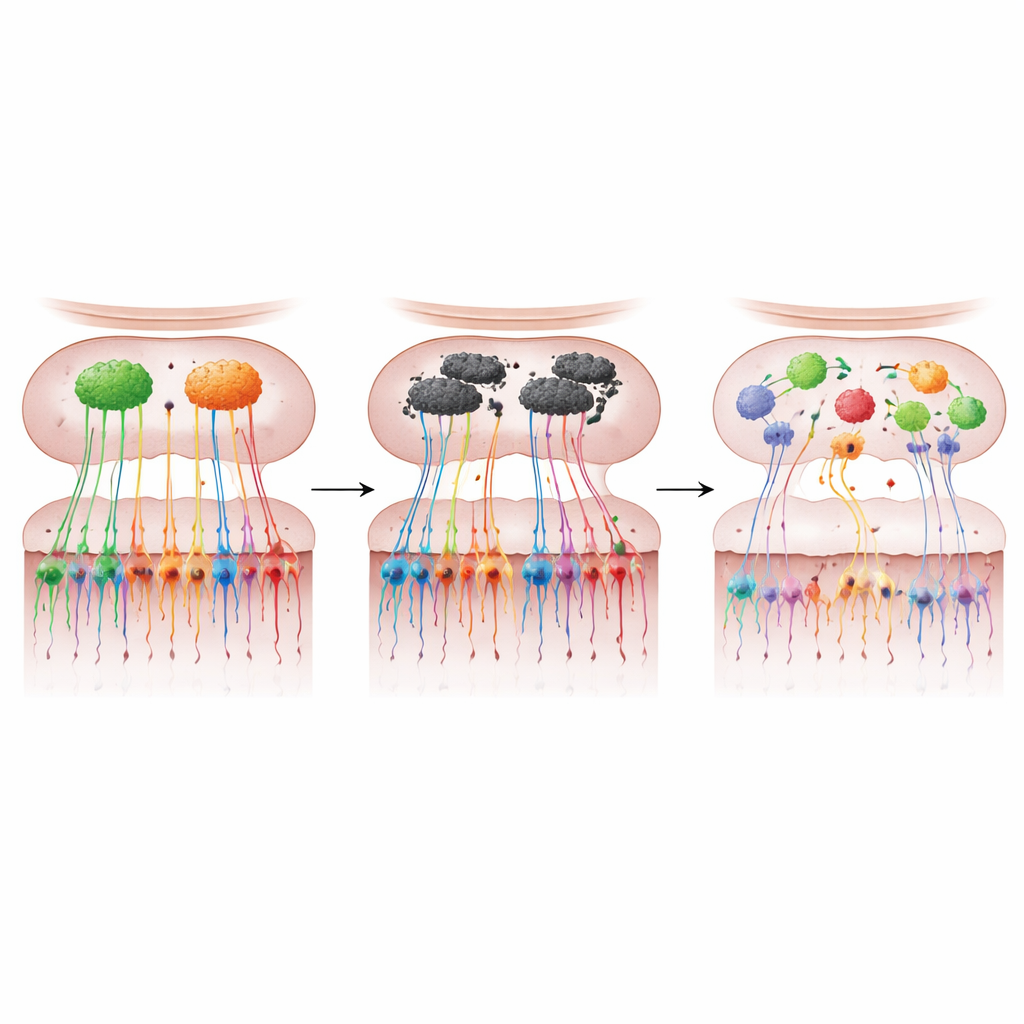
Les cellules olfactives comme fenêtres sur la maladie précoce
Pris ensemble, ces résultats soutiennent un message clair pour un public non spécialiste : dans ce modèle murin proche de la maladie de Parkinson, la surexpression d’α-synucléine dans le bulbe olfactif entraîne à la fois une perte et un mauvais câblage des neurones olfactifs, déformant la carte des odeurs du cerveau et provoquant des troubles olfactifs précoces. Parce que les cellules sensorielles du nez sont liées au plan de développement du cerveau tout en pouvant être échantillonnées par des écouvillonnages ou des biopsies peu invasifs, les auteurs soutiennent que des changements similaires chez l’humain pourraient constituer un biomarqueur précoce puissant de la maladie de Parkinson. Cartographier les empreintes moléculaires de ces cellules, suggèrent-ils, pourrait non seulement aider à identifier des individus à risque des années avant l’apparition des symptômes moteurs, mais aussi offrir une nouvelle compréhension de la façon dont la maladie débute et se propage — et de la manière dont elle pourrait être ralentie ou prévenue.
Citation: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Mots-clés: Maladie de Parkinson, dysfonction olfactive, alpha-synucléine, carte sensorielle, biomarqueurs